La Leucémie Myélomonocytaire Chronique (LMMC) est définie dans la classification de l'Organisation Mondiale de la Santé (OMS) 2022 comme une hémopathie myéloïde clonale maligne appartenant aux syndromes frontières des néoplasmes myélodysplasiques (SMD)/ myéloprolifératifs (NMP), dont elle constitue l'entité la plus fréquente. Il s'agit d'une hémopathie agressive avec un âge médian au diagnostic de 70 ans et une médiane de survie estimée à 34 mois. Son pronostic est hétérogène avec un risque de transformation aiguë (TA) en LAM évalué entre 20 et 30 %. Bien que des altérations génétiques récurrentes aient été identifiées, les mécanismes biologiques de la TA restent mal compris et les options thérapeutiques actuelles sont souvent inefficaces.
Notre étude, menée dans 8 centres du GFM, a inclus 142 patients avec LMMC ayant évolué en LAM entre le 1er janvier 2007 et le 31 décembre 2023. L'objectif principal était de réaliser une analyse de l'évolution clonale entre la phase LMMC et la phase LAM à partir des données de cytogénétiques et de biologie moléculaire recueillies dans les dossiers de patients. Secondairement, nous avons cherché à décrire les modalités de traitement et leur impact sur le délai de TA et la survie et à identifier des paramètres associés à une progression rapide vers la TA. Enfin, nous avons mené une analyse sur les cellules souches et progéniteurs hématopoïétiques par cytométrie en flux et réalisé des analyses protéogénomiques à l'échelle unicellulaire.
L'âge médian au diagnostic de LMMC était de 68 ans [47-92], et de 71 ans [47-93] pour celui de la LAM secondaire, avec une nette prédominance masculine (76 %). La médiane de suivi de la cohorte était de 38 mois et le délai médian de TA était de 25 mois. Au stade LMMC, 79 % des patients présentaient une LMMC-1 et 39 % d'entre eux, une forme proliférative de la maladie telle que définie par l'OMS 2022. Au stade LAM, 92 patients (65 %) ont présenté une LAM de pronostic défavorable telle que définie par l'European Leukemia Net (ELN 2022) et 48 (34 %) étaient non classables. La survie médiane après TA était de 5 mois [3-162].
On dénombrait 70 % de caryotype normaux au diagnostic de la LMMC et les principales anomalies retrouvées étaient par ordre de fréquence : les anomalies du chromosome 7 (5 %), la trisomie 8 isolée (5 %), la perte du Y (4.5 %). Au stade de LAM, nous avons recensé seulement 48 (42 %) caryotypes normaux et les principales anomalies correspondaient à des caryotypes complexes (20 %), des anomalies de structure (17 %), à des anomalies du chromosome 7 (11 %), et des trisomie 8 isolées (9 %).
Les mutations les plus fréquemment rencontrées lors de la phase chronique étaient TET2, SRSF2, ASXL1, RUNX1, NRAS, CBL, ONMT3A, JAK2, SF3B1, et FLT3. Comparativement à la phase chronique, une augmentation significative du nombre médian de mutations (n= 7 ; p = 0,0009) et du nombre médian de gènes mutés (n=4 ; p inférieure à 0,0001), a été observé en phase LAM. Les mutations les plus fréquemment observées à la TA étaient TET2, SRSF2, ASXL1, RUNX1, NRAS, FLT3, STAG2, SF3B1, KRAS, et SF3B1.
Au total, un changement de profil génétique a été observé dans 90 % des cas. Les mutations de RUNX1, NRAS, FLT3, NPM1, CEBPA, BCOR et BCORL1 étaient plus fréquemment acquises lors de la progression. Enfin, de façon générale, l'acquisition de nouvelles mutations était quasiexclusivement sous-clonale sans disparition des clones portant les mutations drivers de LMMC.
En 1ère ligne de traitement de la LMMC, près de la moitié des patients était sous surveillance simple, 20 % ont reçus des HMA, 14 % une cytoréduction par hydroxyurée et 13 % des patients ont eu des soins de supports seuls (EPO, agonistes de la TPO ou transfusions). Les différentes modalités de traitement de la LMMC n'ont pas influencé le délai de TA.
Au stade LAM, un quart des patients ont reçu des soins de support. Après 2020, un tiers des patients ont été traités par l'association azacitidine- vénétoclax tandis que 14 % des patients ont reçu un HMA seul et près de 10 % une chimiothérapie intensive avec un schéma « 3+7 ». Toutefois, le bénéfice en termes de survie pour les LAM secondaires restait médiocre.
En analyse univariée, la présence au diagnostic de LMMC d'un tabagisme actif ou sevré, d'une splénomégalie, d'une anémie inférieure à 10g/dL, d'une leucocytose supérieure à 13 G/L, d'une blastose périphérique étaient associés à un délai de TA plus rapide. De même, la présence d'une forme proliférative, d'une cytogénétique à haut risque, d'une mutation de NRAS, EZH2, RUNX1, FLT3, ou U2AF1, ainsi que les scores Mayo, CPSS et CPSS-mol étaient pronostiques.
Nous avons identifié des facteurs de risque de transformation et pronostiques du délai de TA confirmés en analyse multivariée : le tabagisme actif ou sevré, l'anémie inférieure à 10 g/dL, et la présence d'une mutation de NRAS.
En analysant des échantillons successifs d'un patient atteint de LMMC à différents stades (LMMC-1, LMMC-2 et LAM-s), nous avons étudié l'évolution des cellules souches et progéniteurs hématopoïétiques (CSPH) par cytométrie en flux.
Nous avons mis en évidence une modification progressive de l'architecture des CSPH au cours de la transformation aiguë, caractérisée par une augmentation marquée des progéniteurs LMPP (CD45RA +, cogo-) au détriment du compartiment souche (CD45RA-, cogo+).
L'analyse protéogénomique unicellulaire a permis d'identifier et de quantifier précisément les différentes sous-populations cellulaires ainsi que les clones mutés, avec des résultats prometteurs.
Notre étude rapporte la plus grande cohorte française de patients atteints de LMMC transformée. Nos résultats ont montré que les traitements actuels de la LMMC restent limités et n'affectent pas le délai de transformation aiguë. Ils soulignent l'intérêt d'effectuer un suivi moléculaire dans les LMMC à haut risque et de développer de nouveaux traitements en raison de l'inefficacité des thérapies actuelles au stade de LAM post-LMMC.
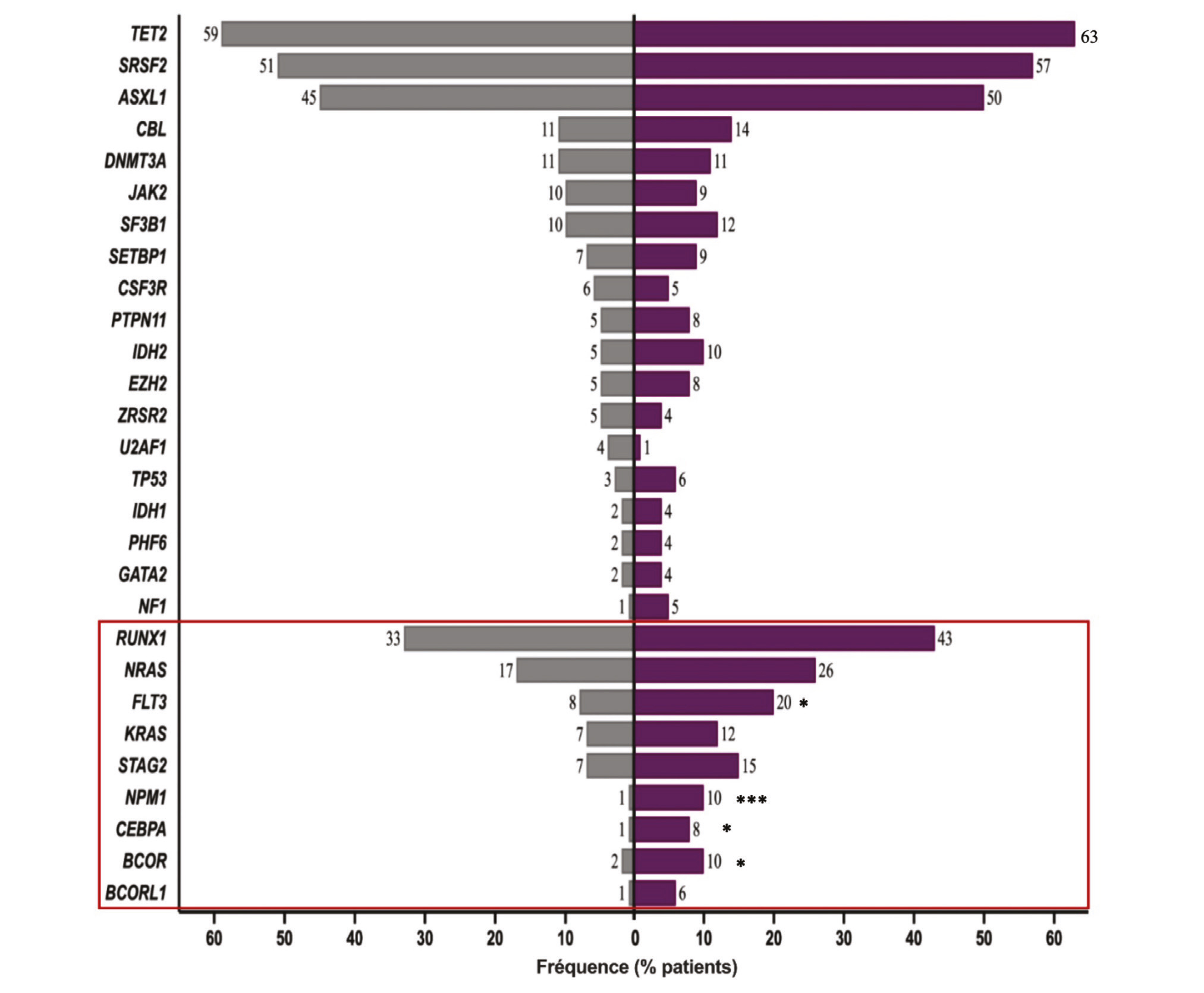
Figure 3. Fréquence des mutations au diagnostic de LMMC et de LAM.
Histogrammes représentant la distribution des mutations retrouvées aux 2 phases (Graphpad, Prism10). La couleur grise est utilisée pour représenter la phase chronique de LMMC, tandis que la couleur violette représente la phase LAM. Les mutations préférentiellement acquises à la TA sont représentées dans l'encadré rouge. 1 étoile : p inférieure à 0.05 2 étoiles : p inférieure à 0.01 3 étoiles : p inférieure à 0.001 et 4 étoiles : p inférieure à 0.0001

Leila CYSIQUE
Cheffe de clinique en hématologie
CHU de Guadeloupe

