La prise en charge de la leucémie aiguë lymphoblastique avec chromosome de Philadelphie (LAL Ph+) et les transformations aiguës lymphoblastiques de leucémie myéloïde chronique (TA-LMC) a été profondément transformée par l'introduction des inhibiteurs de tyrosine kinase (ITK). L'imatinib, puis les ITK de deuxième et de troisième génération, ont permis d'améliorer significativement les taux de réponse et la survie. Néanmoins, 20 à 30 % des patients rechutent, principalement en raison de résistances acquises liées à des mutations du domaine tyrosine kinase (TKD) de BCR::ABL1, en particulier la mutation T315I. Le ponatinib, ITK de troisième génération actif sur cette mutation, est actuellement considéré comme l'ITK le plus efficace dans la LAL Ph+ en situation de rechute ou de résistance.
L'asciminib (ASC) est un inhibiteur de type STAMP (Specifically Targeting the ABL Myristoyl Pocket) qui se distingue des autres ITK par son mécanisme d'action. Il se lie au site de myristoylation de la protéine ABL1, stabilisant celle-ci dans une conformation inactive et inhibant ainsi l'activité kinase constitutive de BCR::ABL1. Bien que l'ASC ait été approuvé par la FDA pour le traitement de première ligne de la LMC, les données concernant son utilisation dans la LAL Ph+ et la TA-LMC après échec des ITK, y compris le ponatinib, restent limitées. Cette étude vise à évaluer, en conditions de vie réelle, l'efficacité et la tolérance de l'ASC chez des patients atteints de LAL Ph+ ou de TA-LMC en rechute ou réfractaires (R/R).
Il s'agit d'une étude observationnelle rétrospective multicentrique (EWALL-OBS22), conduite dans 19 centres en France, conformément à la Déclaration d'Helsinki. Les patients inclus étaient âgés de 18 ans ou plus et avaient reçu de l'ASC, seul ou en association, pour une LAL Ph+ ou une TA-LMC en rechute ou refractaire après au moins une ligne de traitement à base d'ITK. L'ASC a été initialement fourni via un programme d'accès compassionnel jusqu'en novembre 2019, puis prescrit hors autorisation de mise sur le marché. La caractère réfractaire était évalué après l'induction et la première ligne de rattrapage.
Les critères de réponse incluaient la rémission complète (RC) et la rémission complète avec récupération hématologique incomplète (RCi). La négativité de la maladie résiduelle mesurable (MRD) était définie par un rapport BCR::ABL1/ABL1 inférieur à 0,01 % dans la moelle osseuse. La survie globale (OS) et la survie sans événement (EFS) étaient calculées à partir du début de l'ASC, les événements étant définis par l'échec du traitement, la rechute ou le décès. Les analyses statistiques ont utilisé les méthodes de Kaplan- Meier, le test du log-rank et les modèles de régression de Cox.
Au total, 41 patients ont été inclus entre novembre 2019 et avril 2024, dont 33 atteints de LAL Ph+ et 8 de TA-LMC. L'âge médian était de 56 ans (19–84 ans) et 34 % des patients présentaient des comorbidités, principalement cardiovasculaires. Vingt-trois patients ont reçu l'ASC dans le cadre d'un programme d'accès précoce et 18 hors AMM.
Au moment de l'initiation de l'ASC, la majorité des patients était en situation avancée : 24 en rechute hématologique, 7 en rechute moléculaire, 5 réfractaires à la ligne précédente et 1 en rechute isolée du système nerveux central (SNC). Quatre patients en rémission complète, traités par ASC uniquement en raison d'une intolérance à tous les ITK disponibles, ont été exclus de l'analyse d'efficacité. La plupart des patients (78 %) recevaient l'ASC en troisième ligne ou au-delà (médiane de 3 lignes), et 93 % avaient déjà été exposés au ponatinib. Dix-huit patients avaient rechuté après une greffe allogénique de cellules souches hématopoïétiques (allo-CSH), dont quatre après une deuxième greffe, et deux patients avaient rechuté après une thérapie par CAR-T cells.
Une analyse des mutations TKD avant l'initiation de l'ASC était disponible chez 35 patients et révélait la présence d'une mutation dans 77 % des cas. La mutation T315I était la plus fréquente (67 %), suivie de mutations composites chez huit patients. D'autres mutations, plus rares, incluaient E255V, E255K, F311L, F317L et Y253H.
En cohérence avec le profil mutationnel, l'ASC a été administré à la dose de 200 mg deux fois par jour chez 83 % des patients. Dix patients ont reçu l'ASC en association avec une chimiothérapie, et onze en association avec d'autres traitements, incluant des immunothérapies dirigées contre les cellules B (blinatumomab ou inotuzumab), un autre ITK, une infusion de lymphocytes du donneur ou une thérapie par CAR-T cells. Près de la moitié des patients ont reçu l'ASC en monothérapie. Après traitement par ASC, 10 patients ont pu être orientés vers une thérapie cellulaire (allo-CSH et/ou CAR-T).
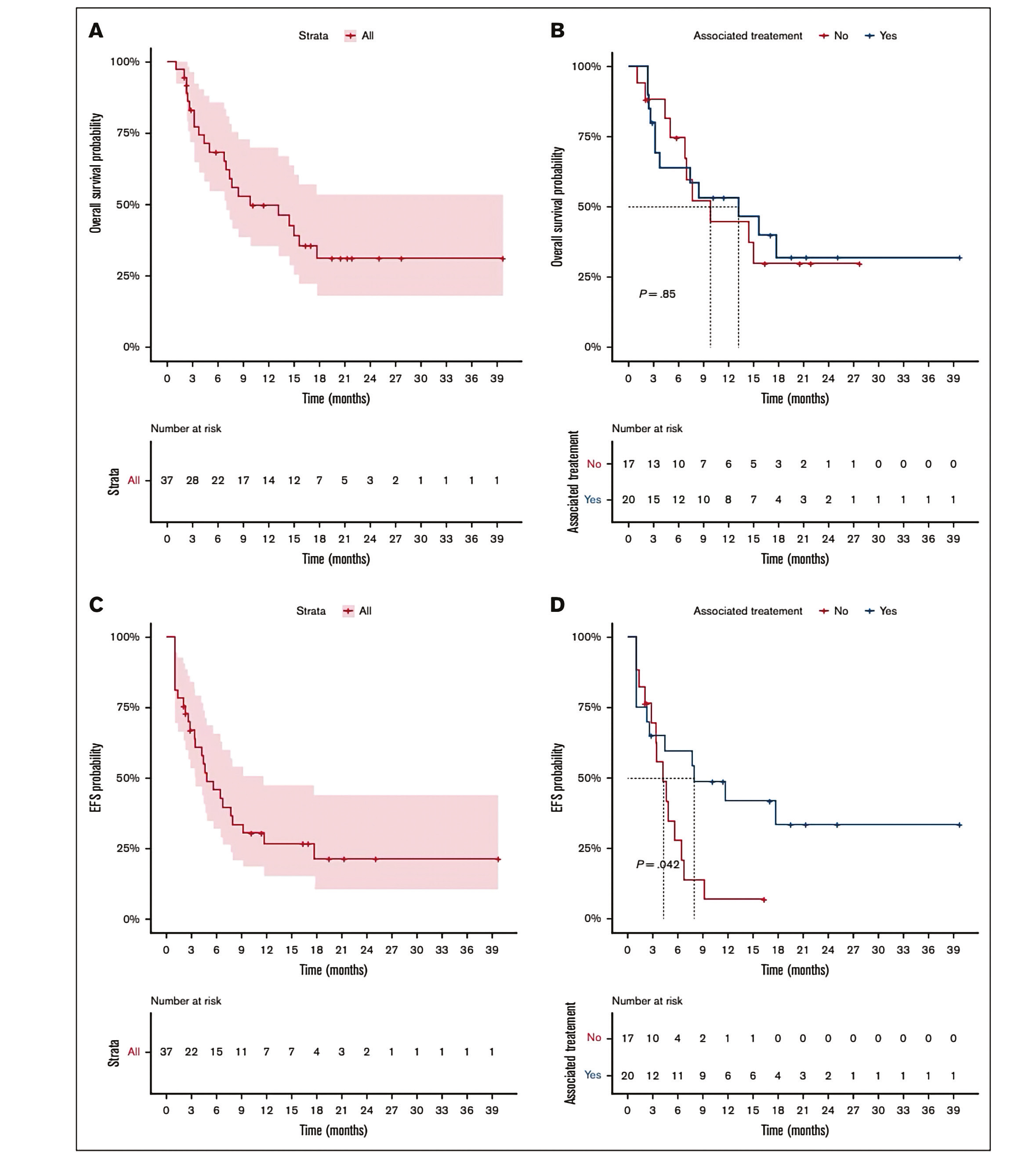
Figure 1. Devenir des patients traités par asciminib.
(A) Survie globale des patients avec LAL B Phi+ en R/R. (B) Survie globale des patients traités par asciminib en combinaison (bleu) ou en monothérapie (rouge). (C) Survie sans événement des patients avec LAL B Phi+ en R/R traités par asciminib. (D) Survie sans événement des patients traités par asciminib en combinaison (bleu) ou monothérapie (rouge).
Parmi les 36 patients évaluables, 83 % ont obtenu une RC ou une RCi. Les taux de réponse étaient élevés aussi bien en monothérapie (88 %) qu'en association (79 %). La négativité MRD a été atteinte chez 57 % des patients disposant d'un prélèvement médullaire évaluable. En excluant les patients en rechute moléculaire au début de l'ASC, 79 % des patients ont obtenu une RC ou RCi, avec un taux de négativité MRD de 56 %, sans différence significative entre LAL Ph+ et TA-LMC.
Avec un suivi médian de 7,6 mois, la survie globale médiane était de 9,8 mois et la survie sans événement médiane de 4,9 mois. L'EFS était plus longue lorsque l'ASC était utilisé en association plutôt qu'en monothérapie. La durée médiane de rémission était de 4,9 mois. Seize patients ont rechuté, principalement sous forme de rechutes hématologiques, mais aussi de rechutes moléculaires ou isolées du SNC, soulignant la difficulté du contrôle de l'atteinte neurologique avec les schémas à base d'ASC.
L'analyse des mécanismes de résistance chez les patients rechutant après une réponse à l'ASC a mis en évidence l'émergence de la mutation Q252H, parfois associée à T315I, dont le mécanisme est à investiguer. Sur le plan de la tolérance, 27 % des patients ont présenté des effets indésirables de grade 3-4, principalement des cytopénies, sans arrêt définitif de l'ASC pour intolérance.
Malgré les limites inhérentes au caractère rétrospectif de l'étude, ces données en vie réelle montrent que l'ASC est associé à des taux de réponse élevés et à des résultats de survie encourageants chez des patients lourdement prétraités atteints de LAL Ph+ ou de TA-LMC R/R. L'ASC apparaît ainsi comme une option thérapeutique pertinente, notamment comme traitement de transition vers des approches curatives telles que l'allogreffe ou les thérapies cellulaires. Ces résultats soutiennent le développement futur de stratégies combinant l'ASC à d'autres traitements, en particulier les immunothérapies, dans les leucémies aiguës Ph+.
Source
Chanut M, Cabannes-Hamy A, Balsat M, Sahki N, Raffoux E, Hicheri Y, Lioure B, Laemmel L, Leguay T, Cacheux V, Gallego- Hernanz MP, Pieragostini A, Roth-Guepin G, Gabellier L, Denizon N, Willems L, Cabrera Q, Chantepie S, Coiteux V, Capdupuy C, Carré M, Machet A, Lambert J, Roux S, Nicolini FE, Boissel N, Clappier E, Kim R, Rousselot P. Asciminib for relapsed or refractory Philadelphia chromosome-positive acute lymphoblastic leukemia. Blood Adv. 2025 Sep 23;9(18):4580-4584. doi: 10.1182/ bloodadvances.2025016665. PMID: 40601900; PMCID: PMC12452587.

Mathilde CHANUT
Interne en Hématologie
à l'AP-HP

