
Blinatumomab for mrd-negative acute lymphoblastic leukemia in adults
M.R. Litzow, Z. Sun, R.J. Mattison et al, The New England Journal of Medicine, 2024
Introduction
Ces dernières années de grandes avancées thérapeutiques ont été réalisées dans la leucémie aiguë lymphoblastique B (LAL-B). Elles ont été marquées par le développement de schémas de traitement d'inspiration pédiatrique chez l'adulte 1 , le suivi de la leucémie par la maladie résiduelle (MRD) permettant de guider la stratégie thérapeutique et l'avènement des immunothérapies dont les anticorps bispécifiques 2 et conjugués 3 ainsi que les CAR-T anti-CD194.
Il existe néanmoins dans la LAL-B une hétérogénéité pronostique en fonction de l'âge des patients avec de meilleures réponses aux traitements dans la population pédiatrique en comparaison à la population adulte 5. Les immunothérapies dont le Blinatumomab (anticorps bispécifique anti-CD19 et anti-CD3) apparaissent prometteuses dans toutes les catégories d'âge 6 et confèrent une efficacité thérapeutique et une bonne tolérance clinique notamment chez les sujets plus âgés 7 .
Le Blinatumomab a déjà fait la preuve de son efficacité dans la LAL-B sans chromosome de Philadelphie (Ph-) dans les situations de rechute ou de maladie réfractaire de l'adulte8. Cet essai de phase 3, randomisé (1 :1), ouvert, a pour objectif principal d'évaluer l'intérêt en survie globale de l'ajout du Blinatumomab en première ligne de consolidation chez les patients adultes âgés de 30 à 70 ans, atteints de LAL B Ph -, en rémission complète avec une maladie résiduelle négative (seuil de détection < 0,01%) en cytométrie en fl ux.
Le schéma de traitement comportait 2 inductions de chimiothérapie suivies d'une intensification à l'issue de laquelle la MRD était évaluée, puis une consolidation par blocs et enfin un traitement de maintenance. Les patients avec une MRD négative (MRD-) en post intensifi- cation étaient randomisés dans le groupe Blinatumomab et recevaient les quatre mêmes blocs de consolidations de chimiothérapie, dans lesquels étaient incorporées quatre cures de Blinatumomab à posologie de 28 µg/j durant 28 jours (deux cures avant la première consolidation de chimiothérapie, une entre les blocs 3 et 4 ainsi qu'une cure avant la chimiothérapie de maintenance). La randomisation était stratifiée sur l'âge (inférieur ou supérieur 55 ans), le statut CD20, l'utilisation du rituximab et si l'allogreffe était indiquée en RC.
Résultats
De 2013 à 2019, 488 patients ont été inclus dans cet essai multicentrique (Israël, Canada et USA), et 395 patients (85 %) ont obtenu une RC1 après l'induction. Cent-neuf patients (27 %) n'ont pas poursuivi l'essai pour cause de mortalité, rechute ou effet indésirable. Parmi les 286 patients restants, 62 gardaient une MRD positive en CMF.
Après l'intensification, le groupe d'étude final est constitué de 224 patients présentant une LAL-B en RC avec MRD négative et ont été randomisés en112 patients dans chaque bras.
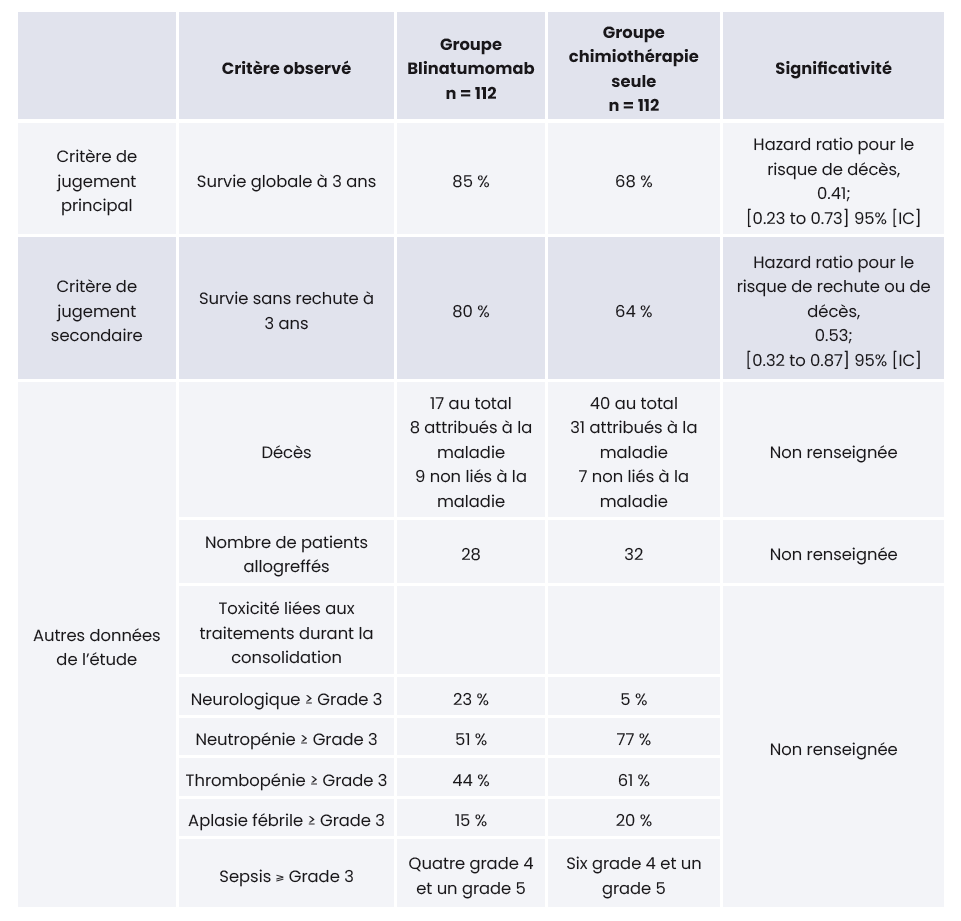
En termes d'efficacité, l'objectif principal a été atteint, la survie globale à 3 ans a été mesurée à 85 % dans le groupe Blinatumomab et 68 % dans le groupe chimiothérapie seule (p=0,002).
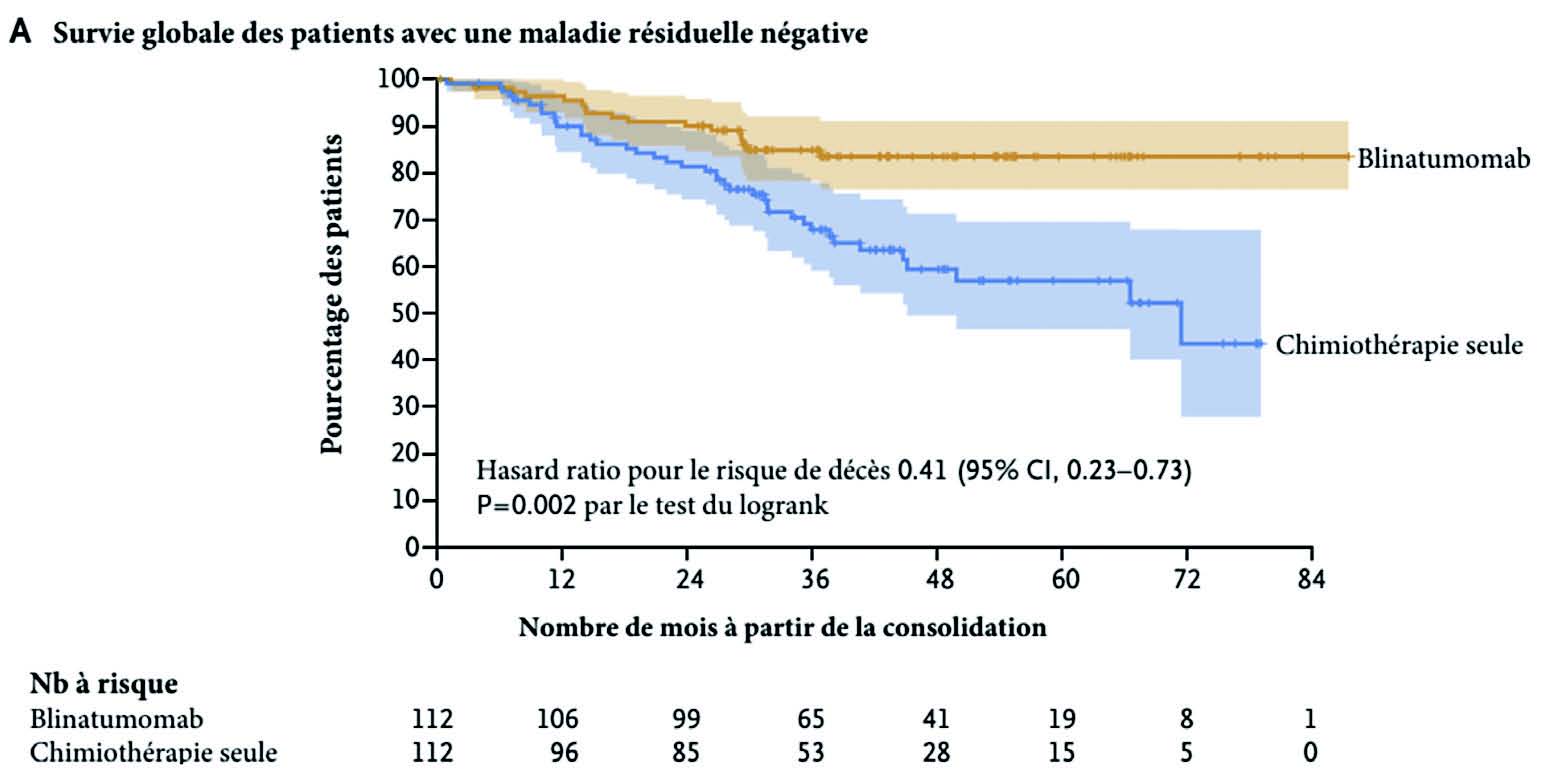
Des résultats similaires ont été obtenus en survie sans rechute à 3 ans avec (80 % dans le groupe Blinatumomab vs 64 % dans le groupe chimiothérapie seule).
Par ailleurs, à titre exploratoire, les analyses en sous-groupe ont montré que le bénéfice apparaissait plus marqué dans la population de moins de 55 ans avec une survie médiane à 3 ans de 95 % dans le groupe Blinatumomab contre 70 % dans le groupe chimiothérapie. Dans la population des patients de plus de 55 ans, la survie médiane à 3 ans était de 70 % dans le groupe Blinatomab contre 65 % dans le groupe chimiothérapie seule.
Concernant les analyses en sousgroupes, il apparaît que les patients de moins de 55 ans ainsi que les patients de risque moléculaire défavorable bénéficient du Blinatumomab de façon significative.
Le profil de toxicité entre les deux groupes semble comparable pour les toxicités hématologiques, et les risques infectieux, avec un surrisque d'évènements neurologiques et psychiatriques dans le groupe Blinatumomab (23 % d'effet secondaire neurologique ≥ grade 3).
Conclusions et perspectives
Cet essai montre l'efficacité en survie globale, du Blinatumomab, en consolidation des LAL B Ph- MRDchez l'adulte de 30 à 70 ans Le Blinatumomab pourrait donc devenir le traitement de consolidation de toutes les LAL B Ph- et non plus seulement dans les groupes avec une maladie résiduelle positive ou pour les patients en rechute de la maladie
Cet essai chez l'adulte est concordant avec un essai pédiatrique publié cette même année dans le NEJM également, évaluant l'ajout du Blinatumomab en survie sans rechute, en première ligne de traitement de la LAL B Ph- chez l'enfant de 1 à 10 ans (phase 3, randomisée en 1 : 1, n=1440). Il est retrouvé avec l'ajout de deux cycles de Blinatumomab en plus de la chimiothérapie standard, une survie sans rechute à trois ans de 96 % contre 87,9 % sans l'immunothérapie9.
Le Blinatumomab est donc bien en passe de devenir un standard de traitement de la LAL B Ph- dans toutes les catégories d'âge.

Enzo FRANKOWSKI
Interne en Hématologie clinique
CHU de Nantes
Références
1. Stock et al., « A pediatric regimen for older adolescents and young adults with acute lymphoblastic leukemia ».
2. Kantarjian et al., « Blinatumomab versus Chemotherapy for Advanced Acute Lymphoblastic Leukemia », 2 mars 2017.
3. Kantarjian et al., « Inotuzumab Ozogamicin versus Standard Therapy for Acute Lymphoblastic Leukemia ».
4. Porter et al., « Chimeric Antigen Receptor T Cells Persist and Induce Sustained Remissions in Relapsed Refractory Chronic Lymphocytic Leukemia »
5. Siegel et al., « Pediatric-Inspired Treatment Regimens for Adolescents and Young Adults With Philadelphia Chromosome– Negative Acute Lymphoblastic Leukemia ».
6. Hogan et al., « Children's Oncology Group AALL1331 »; Litzow et al., « Consolidation Therapy with Blinatumomab Improves Overall Survival in Newly Diagnosed Adult Patients with B-Lineage Acute Lymphoblastic Leukemia in Measurable Residual Disease Negative Remission ».
7. Advani et al., « SWOG 1318 ».
8. Kantarjian et al., « Blinatumomab versus Chemotherapy for Advanced Acute Lymphoblastic Leukemia », 2 mars 2017.
9. Gupta et al., « Blinatumomab in Standard-Risk B-Cell Acute Lymphoblastic Leukemia in Children ».

