Une analyse prospective de l'étude gallium de phase 3
Minimal residual disease status predicts outcome in patients with previously untreated follicular lymphoma: a prospective analysis of the phase III gallium study.
Pott C, Jurinovic V, Trotman J, et al. J Clin Oncol Off J Am Soc Clin Oncol. 2024;42(5):550-61.
Introduction
Rationnel de l'étude
L'étude GALLIUM est un essai clinique randomisé et multicentrique conçu pour évaluer l'efficacité et la sécurité de différents régimes de traitement en première ligne pour les patients atteints de lymphome folliculaire (FL)1. L'objectif principal de cette analyse spécifique est d'examiner la maladie résiduelle minimale/détectable (MRD) en tant que facteur prédictif de l'issue clinique chez ces patients 2.
Méthodes
Les patients ont reçu un traitement initial avec soit de l'obinutuzumab (Ga101) soit du rituximab, en combinaison avec la bendamustine, ou avec une chimiothérapie comprenant cyclophosphamide, doxorubicine, vincristine et prednisone (CHOP), ou cyclophosphamide, vincristine et prednisone (CVP). Ceux qui ont répondu au traitement initial ont ensuite reçu un traitement d'entretien avec le même anticorps anti-CD20. La MRD a été mesurée à 10-5 à des moments définis : à mi-parcours de l'induction (MI) en sanguin, à la fin de l'induction (EOI) en sanguin et médullaire, puis tous les 4 à 6 mois en sanguin exclusivement pendant l'entretien et le suivi. La MRD était mesurée en PCR quantitative (qPCR) pour la détection de la translocation t(14 ;18) et/ou un réarrangement clonal des chaînes lourdes ou légères des immunoglobulines 3.
Résultats
La positivité de la MRD était associée à une survie sans progression (SSP) plus courte à l'IM (rapport de risque [RR], 3,03 [IC à 95 %, 2,07 à 4,45] ; p< 0,0001) et à l'EOT (RR, 2,25 [IC à 95 %, 1,53 à 3,32] ; p< 0,0001). Une analyse multivariée ajustée sur le FLIPI et l'ECOG a confirmé le caractère indépendant de la MRD comme facteur pronostic pour la SSP.
Les répondeurs tardifs (MI positif/EOI négatif) avaient une SSP significativement plus faible que les répon-deurs précoces (MI négatif/EOI négatif ; HR, 3,11 [IC à 95 %, 1,75 à 5,52] ; p= .00011) (figure 1).
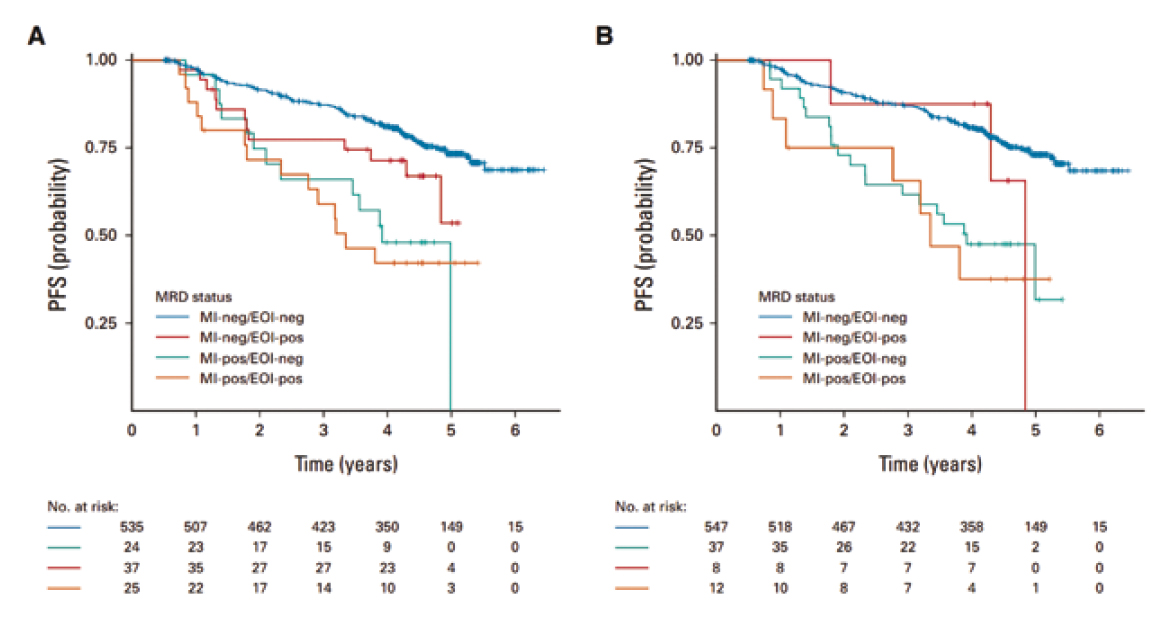
Figure 1 : Survie sans progression à partir de la randomisation en fonction du statut de la MRD à l'EOI. (A) Répondeurs tardifs (MI positif/EOI-négatif) versus répondeurs précoces (MI-négatif/EOI-négatif) : HR, 3,11 ; P =0.00011. (B) Répondeurs tardifs versus répondeurs précoces : HR, 3,04 ; P < 0,0001.
À mi-induction, la positivité de la MRD était plus fréquente chez les patients recevant du CHOP (34/213, 16,0 %) par rapport à ceux recevant de la ben-damustine (20/415, 4,8 % ; P < 0,0001). L'obinutuzumab a semblé jouer un rôle central dans la réponse au traitement, avec des taux de réponse MRD similaires observés dans tous les groupes obinutuzumab et chimiothérapie.
Au cours de la période de maintenance, plus de patients traités par rituximab que par obinutuzumab ont présenté une MRD positive (R-CHOP, 20,7 % contre G-CHOP, 7,0 % ; R-CVP, 21,7 % contre G-CVP, 9,4 %). Pendant toute la durée de la maintenance, la positivité de la MRD a été associée à une rechute clinique. De manière intéressante, au moment de la MI/de l'EOI, le statut MRD a permis de prédire 23 %/25 % des patients qui progresseront dans les 2 ans (POD24) et 93 %/92 % des patients sans POD24, montrant la bonne valeur prédictive positive de ce test.
Discussion
Sous réserve de 23 % de patients non analysables pour la MRD, en suivant en plus de la t(11 :14), le réarrangement clonal de l'Ig avec une approche standardisée basée sur la qPCR spécifique, cette étude a l'avantage de montrer son applicabilité chez un grand nombre de patients.
Le statut de la MRD peut prédire les résultats après l'induction et durant la phase de maintenance, et le statut MRD négatif est essentiel pour un contrôle à long terme de la maladie dans le lymphome folliculaire. Comme déjà montré antérieurement 4, les taux plus élevés de réponses MRD après un traitement à base d'obinutuzumab par rapport à ceux obtenus avec un traitement à base de rituximab indiquent une élimination plus efficace des cellules tumorales.

Bénédicte PIRON
Interne en Hématologie
CHU de Nantes
Références
1. Townsend W, Hiddemann W, Buske C, Cartron G, Cunningham D, Dyer MJS, et al. Obinutuzumab Versus Rituximab Immunochemotherapy in Previously Untreated iNHL: Final Results From the GALLIUM Study. HemaSphere. juill 2023;7(7):e919.
2. Pott C, Jurinovic V, Trotman J, Kehden B, Unterhalt M, Herold M, et al. Minimal Residual Disease Status Predicts Outcome in Patients With Previously Untreated Follicular Lymphoma: A Prospective Analysis of the Phase III GALLIUM Study. J Clin Oncol Off J Am Soc Clin Oncol. 10 févr 2024;42(5):550-61.
3. Rambaldi A, Carlotti E, Oldani E, Della Starza I, Baccarani M, Cortelazzo S, et al. Quantitative PCR of bone marrow BCL2/IgH+ cells at diagnosis predicts treatment response and long-term outcome in follicular non-Hodgkin lymphoma. Blood. 1 mai 2005;105(9):3428-33.
. Seymour JF, Marcus R, Davies A, Gallop-Evans E, Grigg A, Haynes A, et al. Association of early disease progression and very poor survival in the GALLIUM study in follicular lymphoma: benefit of obinutuzumab in reducing the rate of early progression. Haematologica. juin 2019;104(6):1202-8.

