Article présenté
Northend M et al. Early rituximab monotherapy versus watchful waiting for advanced stage, asymptomatic, low tumour burden follicular lymphoma: long-term results of a randomised, phase 3 trial.
Early rituximab monotherapy versus watchful waiting for advanced stage, asymptomatic, low tumour burden follicular lymphoma: long-term results of a randomised, phase 3 trial. Lancet Haematol. 2025;12(5):e335-e345.
Le lymphome folliculaire est l'un des lymphomes non-Hodgkiniens les plus représentés, avec un peu plus de 3000 nouveaux cas diagnostiqués en France sur l'année 2018 (1). La présentation au diagnostic est hétérogène, avec des formes asymptomatiques ou symptomatiques, localisées ou disséminées, de faible ou de forte masse. Il n'existe pas de standard de prise en charge en première ligne, car aucune approche n'a mis en évidence de bénéfice en matière de survie globale. Une association d'anticorps anti-CD20 et chimiothérapie ou de Lénalidomide est habituellement recommandée en traitement initial des formes de forte masse et des formes symptomatiques (2).
Ardesnha et al. a publié en 2014 les résultats du suivi à 4 ans d'un essai randomisé de phase 3 « Watch and Wait » évaluant une surveillance seule contre une monothérapie par Rituximab chez des patients atteints d'un lymphome folliculaire disséminé, de faible masse, asymptomatique et non précédemment traité (3). Une actualisation de cette étude a été rapportée en 2025, avec un suivi à 15 ans (4). Une publication séparée a également évalué la qualité de vie des patients en fonction de la randomisation (5).
L'essai était réalisé en ouvert, avec une randomisation centralisée en 1 :1 :1 dans trois bras : surveillance active, induction par Rituximab, et induction suivie d'une maintenance par Rituximab. Le critère de jugement principal était le délai avant début d'un nouveau traitement spécifique, avec une hypothèse statistique de supériorité au seuil de 2.5 % des bras induction et induction + maintenance par rapport à la surveillance. Le nombre de patients initialement calculé était de 600. Du fait de difficultés de recrutement, le bras induction seule a été fermé précocement. Un nouveau calcul d'eff ectif a été réalisé, prévoyant l'inclusion de 360 patients, randomisés dans les 2 bras restants.
Les patients inclus dans les bras induction et induction + maintenance ont reçu 4 perfusions intraveineuses hebdomadaires de Rituximab, suivies, pour les patients dans le groupe maintenance, de 12 perfusions de Rituximab au rythme d'une perfusion tous les 2 mois. Les patients inclus devaient avoir plus de 18 ans, un Performans Status à 0 ou 1, un lymphome folliculaire de grade 1, 2, ou 3A, de stade II, III ou IV, de faible masse (défini ici par un taux non élevé de LDH, l'absence d'une masse supérieur à 7 cm ou de 3 masses supérieur à 3 cm de diamètre et une rate de moins de 16 cm), asymptomatique, sans compression d'organe, et n'ayant pas reçu de traitement spécifique antérieur.
Entre 2004 et 2009, 463 patients ont été inclus dans 118 centres internationaux, dont 252 avant la modification du design de l'étude. La répartition était de 187 patients dans le bras surveillance, 84 dans le bras induction, et 192 dans le bras induction + maintenance. L'âge médian à l'inclusion était de 60 ans, avec une discrète prédominance féminine (54 %). La première publication rapportait un taux de réponse sur le scanner de réévaluation à 7 mois de 88 % et 59 % de réponses complètes dans le bras induction + maintenance, contre 12 % de régression spontanée et 6 % de régression complète dans le bras surveillance. Le délai médian avant initiation d'un nouveau traitement était de 31 mois dans le groupe surveillance et non atteint pour les patients ayant reçu du Rituximab. Aucune diff érence en matière de survie globale n'était identifiable, avec 28 décès (7 %) à 3 ans.
La tolérance du traitement par Rituximab était bonne, avec de rares cas d'infections (9 dont 5 de grade 3), de réactions allergiques (5 dont 3 de grade 3) et de neutropénie (4 dont 1 de grade 3 et 3 de grade 4). Aucun décès n'a été imputé au traitement.
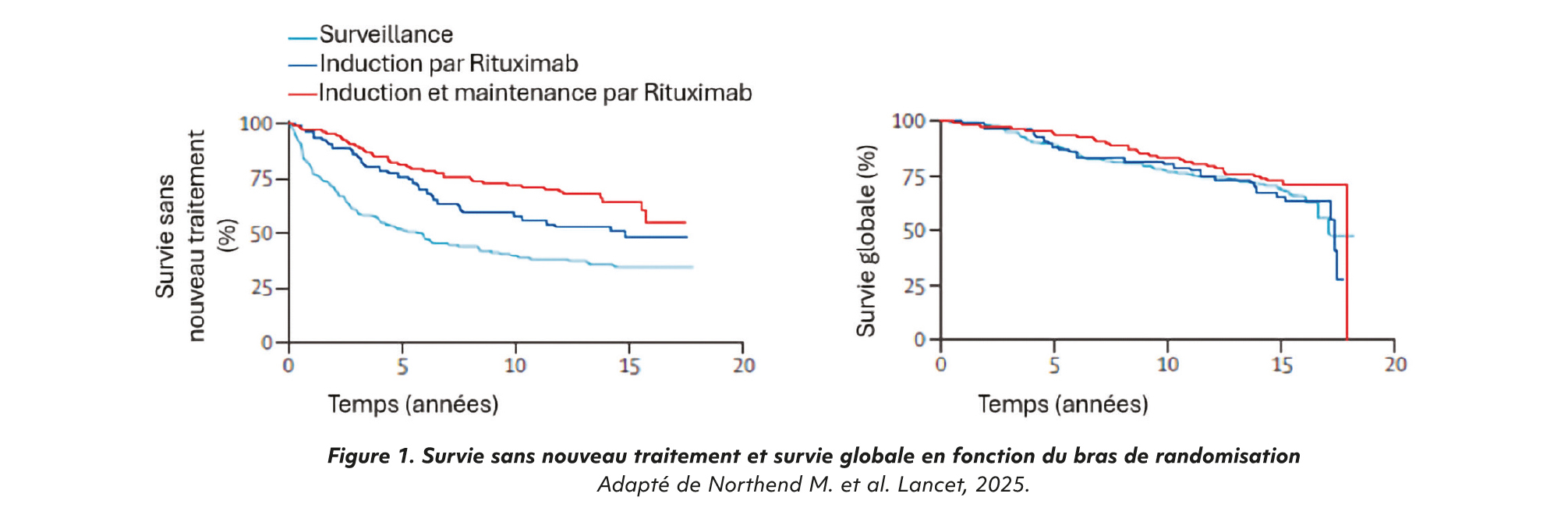
L'actualisation avec un suivi médian à 14.7 ans confirme le bénéfice d'une introduction précoce de Rituximab en matière de délai d'initiation d'un nouveau traitement, sans pour autant montrer de bénéfice en survie globale (Figure 1). Des données étaient disponibles pour 87 % des patients en vie après la fin de l'étude initiale. Parmi les patients randomisés dans le groupe surveillance, 34 % n'avaient pas débuté de traitement à 15 ans, contre 48 % et 65 % dans les groupes induction et induction + maintenance, cette diff érence était significative. L'analyse portant sur les patients randomisés avant la fermeture du bras induction n'a pas permis de mettre en évidence de différence statistiquement significative entre les bras induction et induction + maintenance. Les traitements ultérieurs comprenaient pour l'immense majorité des patients (95 %) un anticorps anti-CD20, le plus souvent associé à une chimiothérapie. Il n'a pas été observé de perte d'efficacité des anti-CD20 après traitement par Rituximab avec une absence de différence significative en matière de délai avant un deuxième nouveau traitement. Une transformation histologique a été observée pour 15 à 20 % des patients et la survenue de second cancer primitif pour 16 à 23 %, sans diff érence significative entre les groupes. La survie globale médiane n'était atteinte dans aucun groupe, avec 28 % de décès dont 48 % liés au lymphome sur l'ensemble de la cohorte.
La qualité de vie des patients a été évaluée lors des 3 premières années après la randomisation. Il n'y avait pas de diff érence significative entre les groupes ni de variation significative dans le temps en termes de bienêtre physique, fonctionnel ou social. L'évaluation du bien-être émotionnel à 7, 13, 25 et 37 mois de la randomisation a montré une amélioration progressive au fil du temps pour l'ensemble de la cohorte, avec une amélioration plus marquée chez les patients randomisés dans le bras induction + maintenance. Les stratégies d'évitement et une connotation péjorative des venues au centre de soin étaient plus souvent rapportées par les patients du groupe surveillance, tandis qu'un sentiment de contrôle plus important était décrit par les patients du bras induction + randomisation. Ces résultats n'étaient pas modifiés par l'exclusion des patients ayant une progression du lymphome.
Les auteurs soulignent le bénéfice d'un traitement par Rituximab en monothérapie par rapport à une stratégie de surveillance en matière de qualité de vie des patients, de délai avant un nouveau traitement, de possibilité d'épargne de chimiothérapie, et ce, avec peu de toxicité liée au traitement et sans perte d'efficacité sur les lignes ultérieures. Le bénéfice d'une maintenance par Rituximab dans ce contexte n'a pas pu être établi du fait de la modification du schéma de l'étude en cours d'inclusion. L'absence de bénéfice en matière de survie globale et de risque de transformation histologique malgré le suivi prolongé et le fait qu'un tier des patients inclus dans le groupe surveillance n'a reçu aucun traitement à 15 ans confirme cependant la faisabilité d'une surveillance seule au diagnostic pour les lymphomes folliculaires de faible masse. La prise en compte des souhaits du patient, et du risque d'anxiété induite par une annonce diagnostic de maladie cancéreuse non suivie de traitement, reste primordiale.
Référence
1. Estimations nationales de l'incidence et de la mortalité par cancer en France métropolitaine entre 1990 et 2018. Volume 2 – Hémopathies malignes. Étude à partir des registres des cancers du réseau Francim.
2. Salles, G. How do I sequence therapy for follicular lymphoma? Hematology 2020, 287–294 (2020).
3. Ardeshna, K. M. et al. Rituximab versus a watch-and-wait approach in patients with advanced-stage, asymptomatic, non-bulky follicular lymphoma: an open-label randomised phase 3 trial. The Lancet Oncology 15, 424–435 (2014).
4. Northend, M. et al. Early rituximab monotherapy versus watchful waiting for advanced stage, asymptomatic, low tumour burden follicular lymphoma: long-term results of a randomised, phase 3 trial. The Lancet Haematology 12, e335–e345 (2025).
5. Marzolini, M. A. V. et al. Quality of life in advanced-stage, asymptomatic, non-bulky follicular lymphoma treated with rituximab shows significant improvement compared with watchful-waiting. British Journal of Haematology 876–886 (2025).

Elise BANDET
Interne en Hématologie,
AP-HP

