
Centre Oscar Lambret (Lille)
Photobiomodulation : principes, techniques et applications
La photobiomodulation (PBM) est une technique thérapeutique utilisant des longueurs d'ondes spécifiques de lumière, de 600 à 100 nm, pour stimuler les processus cellulaires physiologiques. Initialement développée pour des applications esthétiques et la récupération sportive, la PBM trouve un intérêt croissant en cancérologie pour ses propriétés antalgiques, anti-inflammatoires et cicatrisantes. Historiquement, elle a été appelée thérapie par laser basse énergie en raison de la machine utilisée, mais avec la diversification technique, notamment avec les lampes à LED ou les tissus à fibre optique, il est préférable d'utiliser la terminologie biologique.
Principes de la photobiomodulation
La PBM repose sur l'absorption de la lumière par les chromophores cellulaires, ce qui entraîne une augmentation de la production d'ATP et l'activation des voies de signalisation cellulaire. Le cytochrome C (1) présent dans la mitochondrie est celui qui est le plus retrouvé dans la littérature. Sa stimulation entraîne une production d'ATP, permettant des effets anti-inflammatoires et antioxydants, favorisant la réparation et la régénération des tissus. À la différence fondamentale des photons ionisants utilisés en radiothérapie, les longueurs d'onde utilisées en PBM ont une pénétration limitée dans les tissus. Ainsi, pour une longueur d'onde de 630 nm, on estime la pénétration de l'ordre de 2 à 4 mm (Figure 1). Par ailleurs, de nombreuses données in vitro et in vivo ont été publiées sur les processus biologiques, mais les résultats sont encore hétérogènes (2).
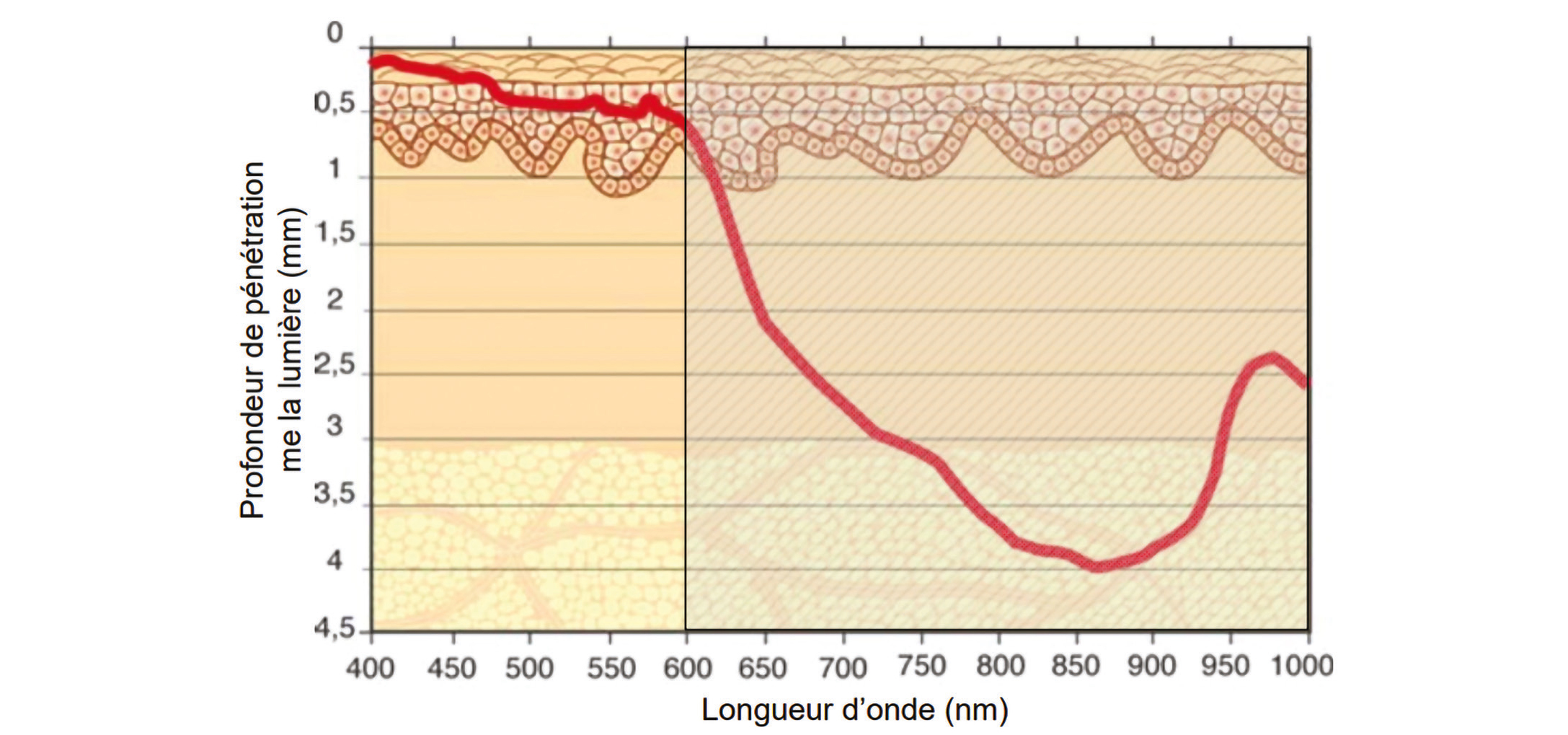
Figure 1 : Profondeur de la pénétration selon la longueur d'onde (15)
Techniques et dispositifs
Les premières machines de PBM ont utilisé la technologique laser, miniaturisée dans des applicateurs en forme de stylo. La délivrance de l'énergie nécessite alors l'application du stylo directement au contact de la muqueuse durant un temps défini (souvent 6 et 145 s selon l'énergie souhaitée) réalisant un spot d'illumination (3). Puis l'opérateur balaie la muqueuse de spots de temps identiques pour atteindre toutes les zones de la muqueuse. Cette technique peut être un peu longue, et reste opérateur dépendante.
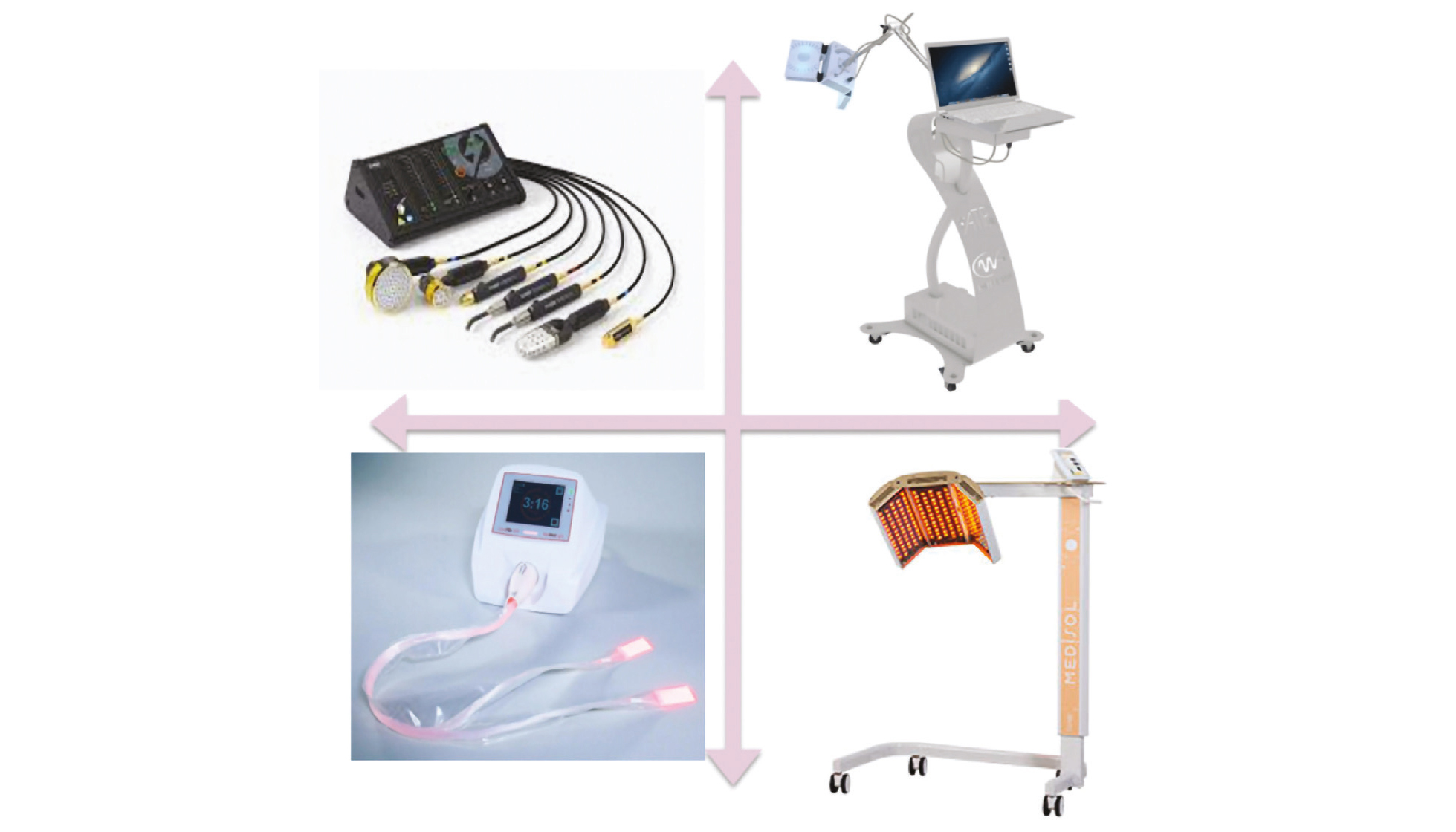
Figure 2 : Exemples de dispositifs de PBM
Dans les dernières années, plusieurs autres dispositifs ont vu le jour. Pour la PBM au contact, il existe un tissu fait de fibre optique qui peut se placer directement au contact de la peau ou de la muqueuse pour délivrer la lumière simplifiant ainsi le traitement (4). Son inconvénient vient de l'utilisation de consommables augmentant le coût global. Enfin, des lampes LED utilisées en médecine esthétique ont été ré-adaptées pour délivrer une PBM à proximité de la cible, sans forcément être au contact de la peau ou de la muqueuse. Ces lampes ont l'avantage de traiter de larges zones facilement, d'être peu onéreuses, mais rendent plus difficile le traitement de zones de muqueuses plus profondes (Figure 2).
Applications de la photobiomodulation en radiothérapie
La PBM est un soin de support qui a pour objectif de prévenir et traiter les effets secondaires des traitements anticancéreux, tels que la mucite aiguë, les radiodermites, les neuropathies périphériques induites par la chimiothérapie, ou les fibroses cutanées.
Dans le champ de la radiothérapie, la mucite des voies aéro-digestives supérieures est la plus étudiée pour des raisons anatomiques d'accessibilité de la muqueuse. Les données de la littérature sont de qualité variable, néanmoins, nous pouvons avoir confiance en une première conclusion : cette méthode thérapeutique ne présente pas de toxicité (5–7). De plus, une inquiétude a été soulevé sur l'illumination de tumeurs, en raison du risque de progression ; mais aucun signal n'a été détecté à ce jour (8) Il faut malgré tout en démontrer l'efficacité avant de développer et fi- nancer l'offre de soin. Les récentes recommandations de la WALT (9) et de la MASCC / ISOO (10) sont basées sur plusieurs essais cliniques randomisés ou cohortes prospectives. Ces essais sont de qualité variable. Certains randomisent contre placebo, et décrivent de façon claire le protocole de PBM (longueur d'onde entre 632 et 685 nm, application au contact de la muqueuse, sessions quotidiennes) (7, 11–13). On y retrouve des résultats hétérogènes : souvent diminution du taux de mucite sévère (grade 3), peu ou pas de différence sur la douleur, pas de différence sur la dysphagie sévère, moins de nutrition entérale (SNG) ou d'utilisation opioïdes. Tous ces essais utilisent des techniques de radiothérapie conformationnelle ou 2D. Or, il est démontré dans les essais de RCMI récente que les taux de mucite sévères ont diminuées (Tableau 1). La seule étude randomisée multicentrique utilisant la RCMI n'a pas retrouvée de différence sur le grade de la mucite, sur la douleur ou la nutrition (14).

Tableau 1 : Taux de mucite sévère (grade 3-4) selon la technique de radiothérapie, sans PBM
Perspectives et défis futurs
L'intégration de la PBM dans les soins de support en oncologie nécessite une évaluation rigoureuse de son efficacité. De nouveaux dispositifs sont commercialisées, et plusieurs centres de radiothérapie se sont équipés en formant médecins et paramédicaux. Cet investissement peut être la base d'un réseau de recherches futures et d'essais cliniques. Plusieurs questions se posent : impact de la modulation d'intensité sur l'effet de la PBM, relation avec le fractionnement quotidien, relation entre effet de la PBM et la dose prescrite ?
Références
1. Zecha JAEM, Raber-Durlacher JE, Nair RG, Epstein JB, Sonis ST, Elad S, et al. Low level laser therapy/photobiomodulation in the management of side effects of chemoradiation therapy in head and neck cancer: part 1: mechanisms of action, dosimetric, and safety considerations. Support Care Cancer. 1 juin 2016;24(6):2781-92.
2. Del Vecchio A, Tenore G, Luzi MC, Palaia G, Mohsen A, Pergolini D, et al. Laser Photobiomodulation (PBM)—A Possible New Frontier for the Treatment of Oral Cancer: A Review of In Vitro and In Vivo Studies. Healthcare. févr 2021;9(2):134.
3. Bensadoun RJ, Franquin JC, Ciais G, Darcourt V, Schubert MM, Viot M, et al. Low-energy He/Ne laser in the prevention of radiation-induced mucositis. A multicenter phase III randomized study in patients with head and neck cancer. Support Care Cancer. juill 1999;7(4):244-52.
4. Bensadoun RJ, Bollet MA, Liem X, Cao K, Magné N. New photobiomodulation device for prevention and cure of radiotherapy-induced oral mucositis and dermatitis: results of the prospective Safe PBM study. Support Care Cancer. 2022;30(2):1569-77.
5. Gautam AP, Fernandes DJ, Vidyasagar MS, Maiya AG, Nigudgi S. Effect of low-level laser therapy on patient reported measures of oral mucositis and quality of life in head and neck cancer patients receiving chemoradiotherapy--a randomized controlled trial. Support Care Cancer. mai 2013;21(5):1421-8.
6. Antunes HS, Herchenhorn D, Small IA, Araújo CMM, Viégas CMP, Cabral E, et al. Phase III trial of low-level laser therapy to prevent oral mucositis in head and neck cancer patients treated with concurrent chemoradiation. Radiother Oncol. nov 2013;109(2):297-302.
7. Gouvêa de Lima A, Villar RC, de Castro G, Antequera R, Gil E, Rosalmeida MC, et al. Oral mucositis prevention by low-level laser therapy in head-and-neck cancer patients undergoing concurrent chemoradiotherapy: a phase III randomized study. Int J Radiat Oncol Biol Phys. 1 janv 2012;82(1):270-5.
8. Antunes HS, Herchenhorn D, Small IA, Araújo CMM, Viégas CMP, de Assis Ramos G, et al. Long-term survival of a randomized phase III trial of head and neck cancer patients receiving concurrent chemoradiation therapy with or without low-level laser therapy (LLLT) to prevent oral mucositis. Oral Oncol. août 2017;71:11-5.
9. Robijns J, Nair RG, Lodewijckx J, Arany P, Barasch A, Bjordal JM, et al. Photobiomodulation therapy in management of cancer therapy-induced side effects: WALT position paper 2022. Front Oncol [Internet]. 30 août 2022 [cité 13 mai 2025];12. Disponible sur: https://www.frontiersin.org/journals/oncology/articles/10.3389/fonc.2022.927685/full
10. Zadik Y, Arany PR, Fregnani ER, Bossi P, Antunes HS, Bensadoun RJ, et al. Systematic review of photobiomodulation for the management of oral mucositis in cancer patients and clinical practice guidelines. Support Care Cancer. oct 2019;27(10):3969-83.
11. Gautam AP, Fernandes DJ, Vidyasagar MS, Maiya GA. Low level helium neon laser therapy for chemoradiotherapy induced oral mucositis in oral cancer patients - a randomized controlled trial. Oral Oncol. sept 2012;48(9):893-7.
12. Carvalho P a. G, Jaguar GC, Pellizzon AC, Prado JD, Lopes RN, Alves FA. Evaluation of low-level laser therapy in the prevention and treatment of radiation-induced mucositis: a double-blind randomized study in head and neck cancer patients. Oral Oncol. déc 2011;47(12):1176-81.
13. Oton-Leite AF, Silva GBL, Morais MO, Silva TA, Leles CR, Valadares MC, et al. Effect of low-level laser therapy on chemoradiotherapy-induced oral mucositis and salivary inflammatory mediators in head and neck cancer patients. Lasers in Surgery and Medicine. 2015;47(4):296-305.
14. Legouté F, Bensadoun RJ, Seegers V, Pointreau Y, Caron D, Lang P, et al. Low-level laser therapy in treatment of chemoradiotherapy-induced mucositis in head and neck cancer: results of a randomised, triple blind, multicentre phase III trial. Radiat Oncol. 22 mai 2019;14(1):83.
15. Dobre S. Analyses de sensibilité et d'identifiabilité globales. Application à l'estimation de paramètres photophysiques en thérapie photodynamique.
16. Bourhis J, Sire C, Graff P, Grégoire V, Maingon P, Calais G, et al. Concomitant chemoradiotherapy versus acceleration of radiotherapy with or without concomitant chemotherapy in locally advanced head and neck carcinoma (GORTEC 99-02): an open-label phase 3 randomised trial. The Lancet Oncology. févr 2012;13(2):145-53.
17. Machiels JP, Tao Y, Licitra L, Burtness B, Tahara M, Rischin D, et al. Pembrolizumab plus concurrent chemoradiotherapy versus placebo plus concurrent chemoradiotherapy in patients with locally advanced squamous cell carcinoma of the head and neck (KEYNOTE-412): a randomised, double-blind, phase 3 trial. The Lancet Oncology. 1 mai 2024;25(5):572-87.
18. Bonner JA, Harari PM, Giralt J, Azarnia N, Shin DM, Cohen RB, et al. http://dx.doi.org/10.1056/NEJMoa053422. 2009 [cité 31 mai 2018]. Radiotherapy plus Cetuximab for Squamous-Cell Carcinoma of the Head and Neck. Disponible sur: https://www.nejm.org/doi/10.1056/NEJMoa053422?url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref. org&rfr_dat=cr_pub%3Dwww.ncbi.nlm.nih.gov
19. Tao Y, Biau J, Sun XS, Sire C, Martin L, Alfonsi M, et al. Pembrolizumab versus cetuximab concurrent with radiotherapy in patients with locally advanced squamous cell carcinoma of head and neck unfit for cisplatin (GORTEC 2015-01 PembroRad): a multicenter, randomized, phase II trial. Annals of Oncology. 1 janv 2023;34(1):101-10.

Dr Xavier LIEM
Oncologue Radiothérapeute
Centre Oscar Lambret
Lille

Dr Isaure ROQUETTE
Oncologue Radiothérapeute
Centre Oscar Lambret
Lille

