Article présenté
Immunotherapeutic targeting of surfaceome heterogeneity in AML
Marie-Eve Bordeleau, Éric Audemard, Arnaud Métois et al.
Cell Reports 2024
Introduction
Au cours des trois dernières décennies, l'hématologie et l'oncologie ont évolué vers une médecine personnalisée, centrée sur les marqueurs antigéniques [1], les caractéristiques moléculaires [2], les anomalies des voies de signalisation [3], permettant de traiter les néoplasies de façon ciblée.
Les thérapies ciblées regroupent un grand nombre d'approches thérapeutiques parmi lesquelles l'immunothérapie s'est imposée comme une révolution médicale tant elle a apporté de bénéfices dans une grande diversité de cancers [4].
La catégorie des immunothérapies regroupe plusieurs types de traitement parmi lesquels se trouvent les inhibiteurs de checkpoints avec comme exemple phare le Pembrolizumab (anti-PD-1) [4], les anticorps monoclonaux dont fait partie le Rituximab (anti-CD20) [5], les anticorps conjugués qui associent un anticorps couplé à un agent cytotoxique avec par exemple le Trastuzumab- deruxtecan [6] dans les tumeurs exprimant HER2.
Plus récemment, d'autres approches immunologiques ont apporté un progrès thérapeutique en impliquant le système immunitaire dans la lyse tumorale avec les anticorps bispécifiques, les T-cell engagers et les CAR-T cells. Parmi les T-cell engagers se positionne le Blinatumomab (anti-CD3 et anti-CD19) [7] qui a révolutionné la prise en charge de la leucémie aiguë lymphoblastique B en améliorant le contrôle de la maladie résiduelle. Les CAR-T cells constituent un traitement autonome capable de s'expendre et d'éliminer efficacement les cellules tumorales, souvent de façon prolongée dans le temps [8].
Cependant, certaines pathologies n'ont pas tiré grand bénéfice de l'avènement des immunothérapies parmi lesquelles se trouve la leucémie aiguë myéloïde (LAM) [9, 10]. Dans la LAM, les cibles morphologiques et du microenvironnement tumoral se sont souvent avérées décevantes, une seule immunothérapie a été validée, il s'agit du Gemtuzumab- Ozogamycine (anti-CD33 couplé à un agent cytotoxique) qui est efficace principalement dans les LAMs CBF, de bon pronostic [11].
L'article présenté ici porte sur l'analyse du surfaceome de la LAM et vise à identifier de nouvelles cibles thérapeutiques qui pourraient être pertinentes pour le développement de nouvelles immunothérapies.
Méthodes
Le travail de cette équipe de chercheurs a porté sur 100 échantillons de patients atteints de LAM (non LAP) avec comme objectif d'identifier des cibles membranaires spécifiques et en particulier des cellules souches leucémiques.
Des données de transcriptomique, de protéomique et de protéomique membranaire ont été collectées pour identifier des patterns permettant de distinguer les cellules leucémiques des cellules saines. Ces analyses sont complémentaires, la transcriptomique a permis de nombreux progrès dans la compréhension du fonctionnement tumoral, mais elle présente la limite de négliger la machinerie traductionnelle, laquelle est prise en compte par l'approche protéomique.
L'analyse protéomique de surface est complexe, il est en effet à l'heure actuelle difficile de mettre en évidence les marqueurs présents à la membrane d'une cellule. Pour résoudre ce problème, cette équipe s'est basée sur l'outil SPAT (Surface Protein Annotation Tool) d'annotation des protéines de surface, un algorithme permettant d'attribuer un score de probabilité sur la localisation d'une protéine à la membrane sur son versant extracellulaire.
Différents sous-types de LAM ont été distingués et explorés dans cette étude comme les LAM avec inversion du chromosome 16, les remaniements MECOM, les LAM à caryotype complexe, etc. L'hypothèse soulevée dans cette étude est que l'hétérogénéité génétique se traduit par une hétérogénéité de marqueurs de surface.
Du séquençage ARN en single-cell a été réalisé pour identifier des antigènes exprimés en particulier par les cellules souches leucémiques, réservoir de la maladie.
Résultats
Pour chaque LAM, environ 2000 protéines sont détectées à la surface des cellules leucémiques, parmi celles-ci, 400 protéines avaient un score SPAT robuste. La plupart des échantillons analysés présentaient bien les marqueurs connus de la LAM (CD33, CD123).
Il a été observé que toutes les LAM n'expriment pas de façon homogène les différents marqueurs membranaires, il existe par exemple une sous-représentation de CD34 et CD2 dans les LAM avec inversion du chromosome 16, une surexpression du marqueur monocytaire CD300LB et une faible expression de CD34 pour les LAM avec remaniement de KMT2A.
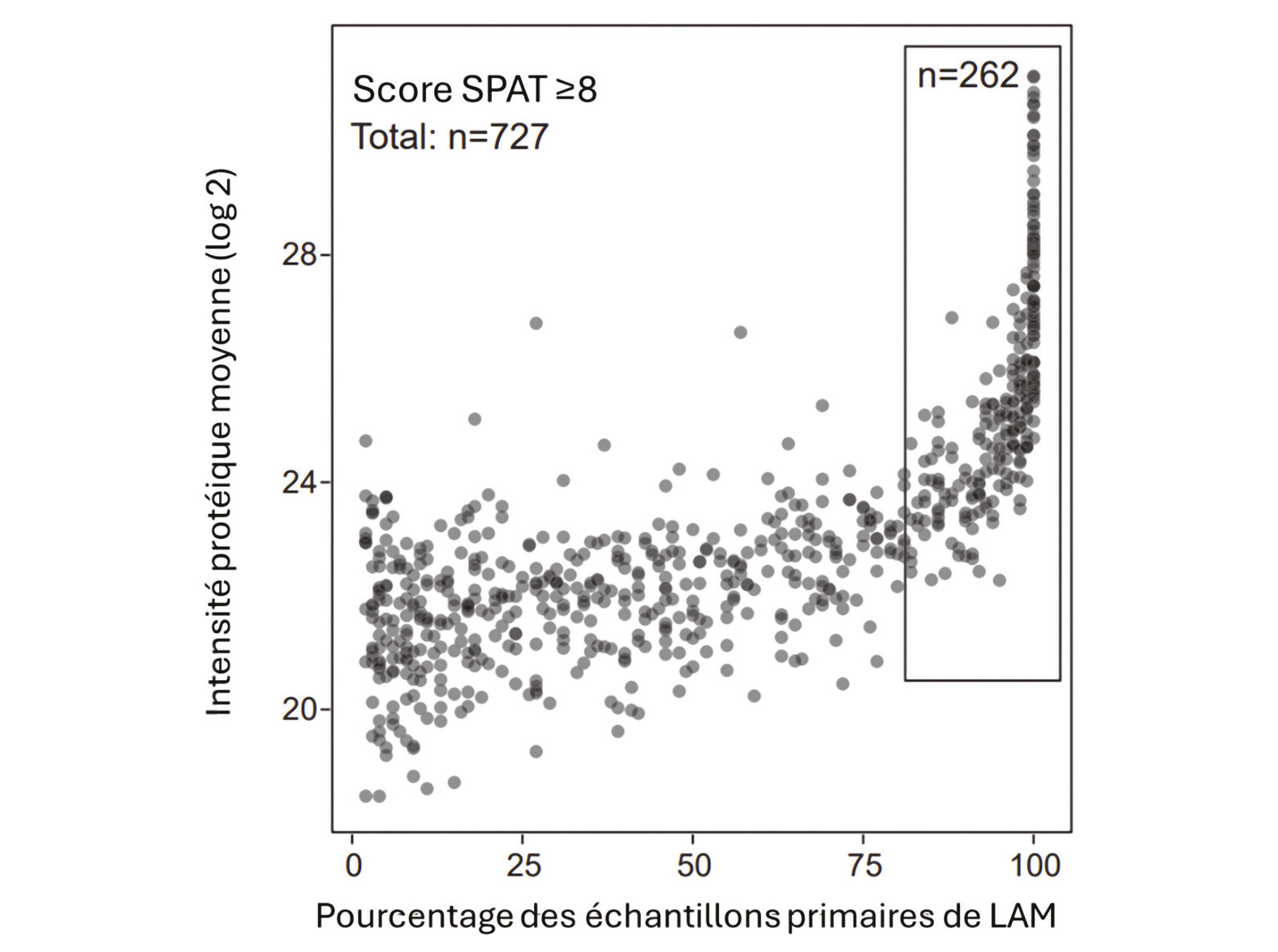
Figure 1. Intensité protéique moyenne du protéome de surface de la LAM en fonction du pourcentage d'échantillons dans lesquels chaque protéine est détectée.
Des marqueurs pan-LAM ont été recherchés, 262 protéines avec un score SPAT élevé ont été détectés dans plus de 80 % des échantillons de la cohorte.
Parmi ces antigènes pan-LAM, ceux présentant un score SPAT robuste (supérieure ou égale à 8) ont été identifiés. Dix d'entre eux sont la cible d'immunothérapies en cours de développement dans la LAM, 19 antigènes sont ciblés par d'autres immunothérapies en cours de développement dans d'autres pathologies et 3 marqueurs n'ont pas fait l'objet de ciblage thérapeutique. Parmi ces antigènes, huit d'entre eux sont exprimés à un niveau similaire ou supérieur à CD33 et ILR3A : LAIR1, CD47, PTPRC, FLT3, CD37, ITGA4, VSIR, CD74 (figure 2). Des analyses de cytométrie en flux ont confirmé l'expression d'ITGA4 et de VSIR dans les échantillons de LAM confortant leur intérêt clinique dans la LAM.

Figure 2. Représentation du processus de sélection des antigènes pan-LAM. Les antigènes exprimés par les cellules de LAM et les cellules souches leucémiques dans des proportions similaires ou supérieures à celles de CD33 ou IL3RA sont notés en bleu.
Pour évaluer l'expression de ces marqueurs à la surface des cellules souches leucémiques, une analyse complémentaire des protéines pan-LAM a été poursuivie par une approche de single-cell. Les transcriptomes d'échantillons riches en cellules souches leucémiques ont été comparés aux échantillons pauvres et trois marqueurs exprimés préférentiellement dans le compartiment souche ont été retenus SLC38A1, CD34 et NPR3. Douze marqueurs complémentaires ont également été identifiés mais dans des sous-groupes spécifiques de LAM, cette observation témoigne d'une différence phénotypique des cellules souches leucémiques entre les différents sous-groupes de LAM (figure 3 et figure 4).

Figure 3. Aperçu des données de séquençage d'ARN single-cell. Le pourcentage de cellules de LAM exprimant les antigènes, issues d'échantillons des sous-groupes de LAM indiqués, ainsi que les scores Z calculés pour chaque gène en fonction de son expression dans les différents sous-groupes de LAM, sont présentés.

Figure 4. Aperçu des données de séquençage d'ARN single-cell obtenues pour les marqueurs potentiels de cellules souches leucémiques (CSL). Le pourcentage de cellules de LAM de type cellules souches hématopoïétiques (CSH) issues d'échantillons des sous-groupes de LAM indiqués, exprimant les antigènes indiqués, ainsi que les scores Z calculés par gène pour les niveaux d'expression dans les différents sous-groupes de LAM, sont présentés.
Concernant les analyses des différents sous-groupes, une population d'intérêt concerne les LAM à caryotype complexe. Leur analyse a permis d'identifier trois antigènes candidats (ENG, PTPRC et CD47). ENG est la protéine de surface la plus fortement exprimée par les cellules LAM à caryotype complexe et avec réarrangement de MECOM par rapport aux autres sous-groupes de LAM et cette observation a été confirmée par cytométrie en flux (figure 5).

Figure 5. Analyse par cytométrie en flux de l'expression d'ENG à la surface de cellules dans des échantillons primaires de LAM (CK, n = 9 ; MECOM -r, n = 10). Les profils de deux échantillons représentatifs sont présentés. La proportion moyenne de cellules exprimant l'antigène au sein de la population blastique pour les échantillons analysés est indiquée en rouge.
Discussion
Dans la LAM, les innovations thérapeutiques actuelles se tournent vers le ciblage des anomalies métaboliques, les anomalies de voies de signalisation, les résistances des voies de mort cellulaire. Les approches d'immunothérapie n'ont pas permis jusqu'alors d'apporter de bénéfice en survie pour l'ensemble des soustypes de LAM bien que l'approche de ciblage morphologique apparaisse pertinente.
Cette étude souligne que l'approche protéomique de surface pourrait permettre d'identifier de nouvelles cibles pour le design d'immunothérapies à visée de réduction de la charge blastique voire de cibler le réservoir de cellules souches leucémiques à l'origine de la persistance de la maladie. Elle révèle également la complexité de l'hétérogénéité phénotypique et l'architecture cellulaire des leucémies aiguës myéloïdes qui pourraient également constituer des défis dans le cadre d'une approche thérapeutique par immunothérapie.
Bibliographie
1. Maloney DG, Liles TM, Czerwinski DK, Waldichuk C, Rosenberg J, Grillo-Lopez A, et al. Phase I Clinical Trial Using Escalating Single-Dose Infusion of Chimeric Anti-CD20 Monoclonal Antibody (IDEC-C2B8) in Patients With Recurrent B-Cell Lymphoma. Blood. 15 oct 1994;84(8):2457-66.
2. Gallogly MM, Lazarus HM, Cooper BW. Midostaurin: a novel therapeutic agent for patients with FLT3-mutated acute myeloid leukemia and systemic mastocytosis. Ther Adv Hematol. sept 2017;8(9):245-61.
3. McArthur GA, Chapman PB, Robert C, Larkin J, Haanen JB, Dummer R, et al. Safety and efficacy of vemurafenib in BRAFV600E and BRAFV600K mutation-positive melanoma (BRIM-3): extended follow-up of a phase 3, randomised, open-label study. Lancet Oncol. mars 2014;15(3):323-32.
4. Marabelle A, Le DT, Ascierto PA, Di Giacomo AM, De Jesus- Acosta A, Delord JP, et al. Efficacy of Pembrolizumab in Patients With Noncolorectal High Microsatellite Instability/ Mismatch Repair–Deficient Cancer: Results From the Phase II KEYNOTE-158 Study. J Clin Oncol. 1 janv 2020;38(1):1-10.
5. Maloney DG, Liles TM, Czerwinski DK, Waldichuk C, Rosenberg J, Grillo-Lopez A, et al. Phase I clinical trial using escalating single-dose infusion of chimeric anti-CD20 monoclonal antibody (IDEC-C2B8) in patients with recurrent B-cell lymphoma. Blood. 15 oct 1994;84(8):2457-66.
6. Trastuzumab deruxtecan (DS-8201a) in patients with advanced HER2-positive breast cancer previously treated with trastuzumab emtansine: a dose-expansion, phase 1 study - The Lancet Oncology [Internet]. [cité 31 janv 2026]. Disponible sur : https://www.thelancet.com/journals/lanonc/ article/PIIS1470-2045(19)30097-X/fulltext
7. Ali S, Moreau A, Melchiorri D, Camarero J, Josephson F, Olimpier O, et al. Blinatumomab for Acute Lymphoblastic Leukemia: The First Bispecific T‐Cell Engager Antibody to Be Approved by the EMA for Minimal Residual Disease. The Oncologist. avr 2020;25(4):e709-15.
8. Neelapu SS, Locke FL, Bartlett NL, Lekakis LJ, Miklos DB, Jacobson CA, et al. Axicabtagene Ciloleucel CAR T-Cell Therapy in Refractory Large B-Cell Lymphoma. N Engl J Med. 28 déc 2017;377(26):2531-44.
9. He SZ, Busfield S, Ritchie DS, Hertzberg MS, Durrant S, Lewis ID, et al. A Phase 1 study of the safety, pharmacokinetics and anti-leukemic activity of the anti-CD123 monoclonal antibody CSL360 in relapsed, refractory or high-risk acute myeloid leukemia. Leuk Lymphoma. mai 2015;56(5):1406-15.
10. Ravandi F, Stein AS, Kantarjian HM, Walter RB, Paschka P, Jongen-Lavrencic M, et al. A Phase 1 First-in-Human Study of AMG 330, an Anti-CD33 Bispecific T-Cell Engager (BiTE®) Antibody Construct, in Relapsed/Refractory Acute Myeloid Leukemia (R/R AML). Blood. 29 nov 2018;132(Supplement 1):25.
11. Efficacy and Safety of Gemtuzumab Ozogamicin in Patients With CD33-Positive Acute Myeloid Leukemia in First Relapse | Journal of Clinical Oncology

Dr Alexandre IAT
Assistant spécialiste
en hématologie
Institut Paoli-Calmettes
Marseille

