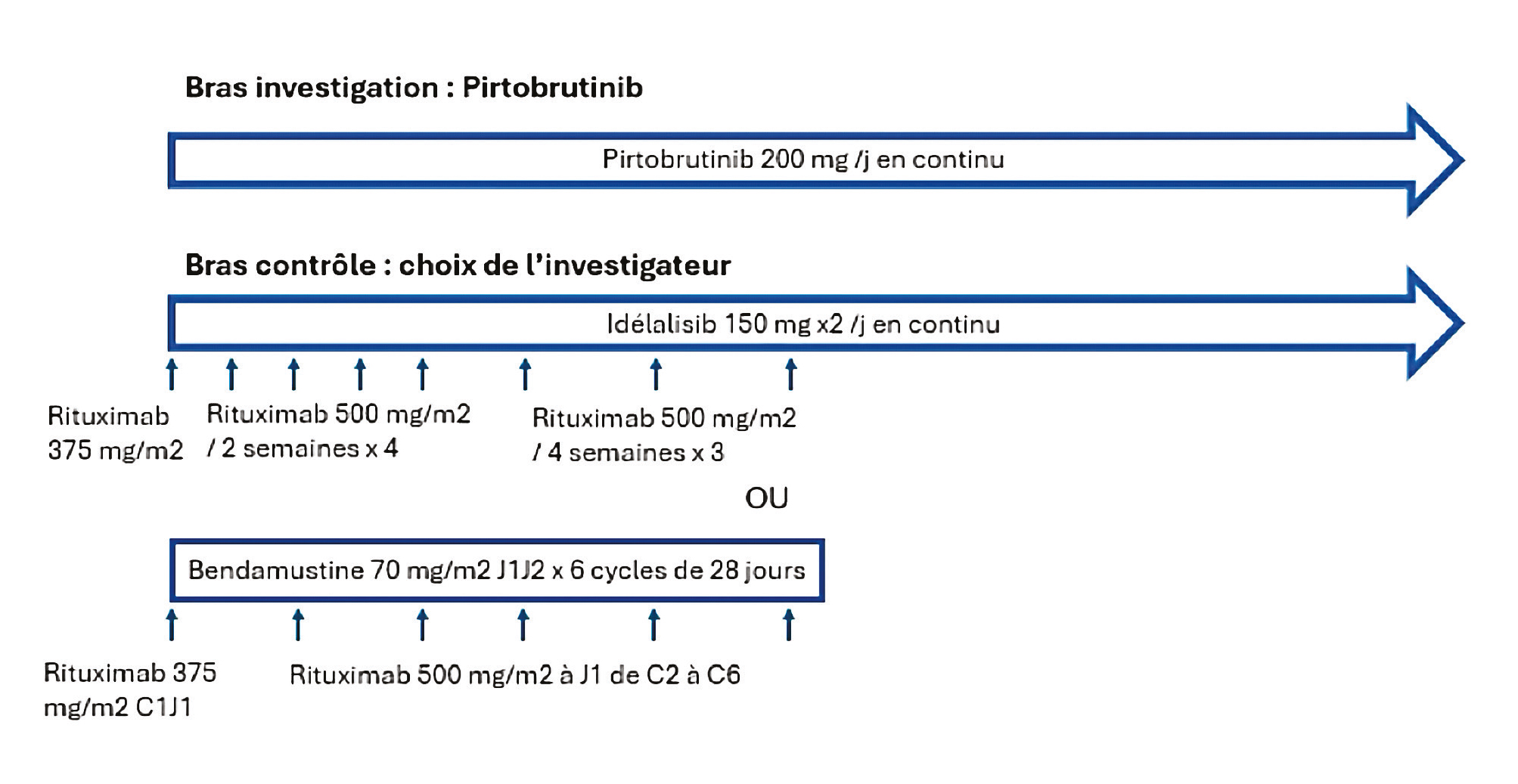
Figure 1. Schéma thérapeutique de l'essai BRUIN CLL-312 en fonction du bras de randomisation.
Au total, 238 patients ont été inclus entre mars 2021 et juillet 2023, soit 119 patients dans chaque bras avec, parmi les patients du bras contrôle, 82 assignés par l'investigateur à un traitement par Rituximab et Idélalisib et 37 à un traitement par Rituximab et Bendamustine. Trois et 10 patients des bras Pirtobrutinib et contrôle respectivement n'ont pas reçu de traitement, principalement du fait d'un retrait du consentement. Les caractéristiques étaient globalement équilibrées entre les bras avec un âge médian de 66 ans, 70 % d'hommes, et 50 % de patients exposés au Vénétoclax. Une légère surreprésentation de caryotypes complexes (72 % contre 59 %) et d'IGH non mutées (93 % contre 80 %) était observée dans le bras Pirtobrutinib. Le traitement antérieur par icBTK concernait principalement l'Ibrutinib (87 %), et 72 % des patients l'avaient arrêté pour progression. Une mutation C481S de BTK était présente chez 38 % des patients pour qui l'information était disponible.
Après un suivi médian de 17,2 mois, le Pirtobrutinib est associé à une amélioration significative de la survie sans progression (Figure 2). Les analyses en sous-groupes montrent également la persistance de cet effet, y compris chez les patients exposés au Vénétoclax. Un bénéfice est également rapporté sur les critères de jugements secondaires avec un taux de réponse globale de 65 % contre 53 % et un délai jusqu'au prochain traitement de 24 mois contre 10.9 mois (Figure 2). La survie globale à 18 mois n'était pas significativement modifiée et était de 73.4 % dans le bras Pirtobrutinib contre 70.8 % dans le bras contrôle. Le protocole autorisait un crossover vers le Pirtobrutinib en cas de progression avec critères de traitement et 76 % des patients ayant progressé dans le bras contrôle ont reçu du Pirtobrutinib, ce qui a pu impacter la survie globale. Les patients ayant une progression documentée sous traitement pouvaient le poursuivre à la discrétion de l'investigateur et 38.6 % des patients progressant sous Pirtobrutinib ont continué le traitement, ce qui pose la question de la pertinence de la SSP comme critère de jugement principal. Les effets indésirables principaux rapportés dans le bras Pirtobrutinib étaient infectieux (22.4 % de pneumonies) et hématologiques. Trois évènements hémorragiques de grade supérieure ou égale à 3, ainsi que 3 et 8 cas de fibrillation atriale et d'hypertension artérielle ont été notés chez les patients traités par Pirtobrutinib. Les réductions de doses et interruptions de traitement étaient plus fréquentes dans le bras contrôle (36.7 contre 11.2 %, et 34.9 contre 17.2 %). Le traitement était toujours en cours chez 39.7 % des patients sous Pirtobrutinib contre 6.5 % sous Idélalisib.
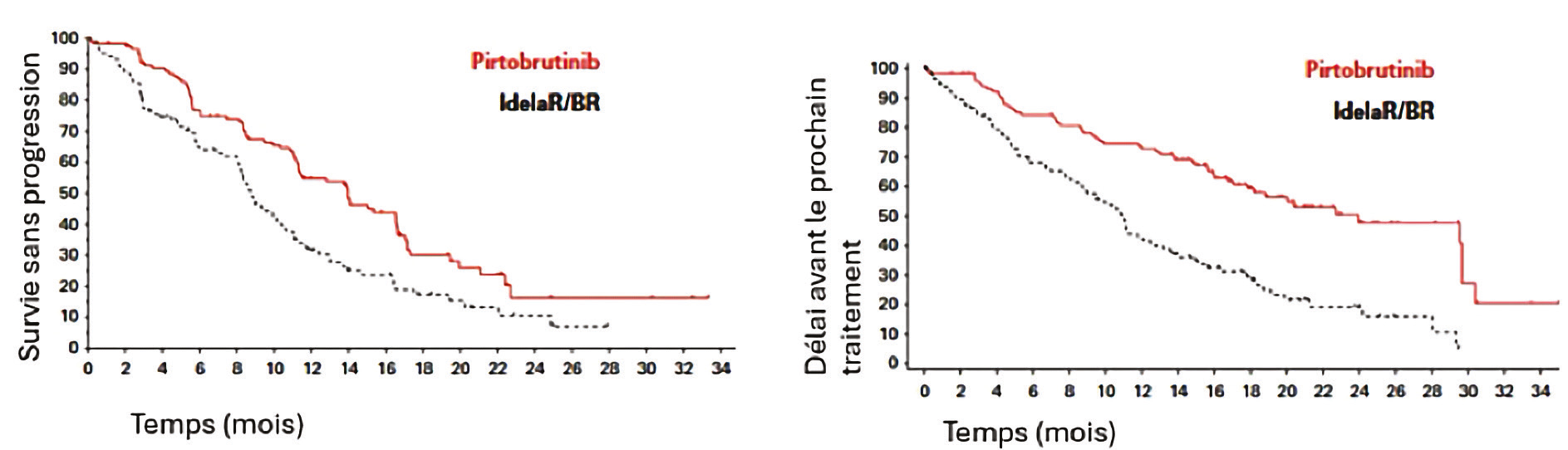
Figure 2. Survie sans progression et délai avant le prochain traitement en fonction du bras de randomisation.
En conclusion, cet essai confirme l'intérêt du Pirtobrutinib comme traitement de la LLC après échec d'icBTK. Des données préliminaires de phases 3 sur l'utilisation du Pirtobrutinib en comparaison à l'Ibrutinib chez des patients atteints de LLC et non préalablement exposés aux icBTK ont par ailleurs été présentés à l'ASH 2025, avec des données encourageantes sur le taux de réponse et un suivi encore immature sur la survie globale et sans progression [5]. La place du Pirtobrutinib dans l'arsenal thérapeutique de la LLC reste donc encore à établir.
Bibliographie
1. Al-Sawaf, O. et al. Fixed-Duration versus Continuous Treatment for Chronic Lymphocytic Leukemia. N Engl J Med NEJMoa2515458 (2025) doi:10.1056/NEJMoa2515458.
2. Mato, A. R. et al. Outcomes for Patients With Chronic Lymphocytic Leukemia (CLL) Previously Treated With Both a Covalent BTK and BCL2 Inhibitor in the United States: A Real-World Database Study. Clinical Lymphoma Myeloma and Leukemia 23, 57–67 (2023).
3. Gomez, E. B. et al. Pirtobrutinib preclinical characterization: a highly selective, non-covalent (reversible) BTK inhibitor. Blood blood.2022018674 (2023) doi:10.1182/blood.2022018674.
4. Mato, A. R. et al. Pirtobrutinib after a Covalent BTK Inhibitor in Chronic Lymphocytic Leukemia. N Engl J Med 389, 33–44 (2023).
5. Woyach, J. et al. Pirtobrutinib vs ibrutinib in treatment-naïve and relapsed/refractory CLL/SLL: Results from the first randomized phase III study comparing a non-covalent and covalent BTK inhibitor. Blood 146, 683–683 (2025).

Elise BANDET
Interne en Hématologie,
AP-HP

