Abréviations
Artériopathie Oblitérante des Membres Inférieurs (AOMI) ; Bandelette Urinaire (BU) ; Examen Cytobactériologique des Urines (ECBU) ; Érythropoïétine (EPO) ; European Society of Hypertension (ESH) ; Hypertension Artérielle (HTA) ; Facteur de Croissance Insuline-Like 1 (IGF-1) ; Pression Artérielle (PA) ; Pression Artérielle Systolique (PAS) ; Polykystose Rénale Autosomique Dominante (PKRAD) ; Hormone Parathyroïdienne (PTH) ; Syndrome d'Apnée Obstructive du Sommeil (SAOS) ; Système Rénine-Angiotensine (SRA) ; Triiodothyronine et Thyroxine (T3/T4) ; Hormone Stimulante de la Thyroïde (TSH).
Introduction
L'hypertension artérielle (HTA) est l'une des maladies les plus répandues dans le monde affectant environ un adulte sur trois soit près de 1,5 milliards d'individus. Premier facteur de mortalité cardiovasculaire dans le monde, elle est responsable de 10 millions de décès annuels. En France, la situation est tout aussi préoccupante avec 17 millions de la population nationale concernée par l'hypertension. Malgré les conséquences et la gravité de cette maladie, un constat alarmant peut être fait en France : la moitié des hypertendus n'est pas diagnostiquée et parmi ceux qui sont identifiés, la moitié d'entre eux ne bénéficie pas d'un contrôle adéquat de sa tension artérielle laissant 3/4 des patients non pris en charge de manière optimale.
Bien que l'HTA soit primitive dans l'écrasante majorité des cas, la détection des formes d'HTA secondaire représente un enjeu capital. Ces formes sont souvent résistantes aux traitements anti-hypertenseurs conventionnels sans une intervention ciblée. Elles touchent des patients globalement plus jeunes et donc pour lesquels le fardeau de l'HTA sera plus conséquent sur le long terme et avec dans certaines formes un risque de mortalité cardiovasculaire accru et une atteinte plus sévère des organes cibles. En l'absence spécifique, il est démontré que ces formes sont associées à une mortalité, un risque cardiovasculaire et une atteinte des organes cibles accrus qui peut être partiellement ou totalement réversible avec le traitement de la cause secondaire3. Ce traitement d'une cause secondaire peut même parfois permettre d'obtenir la guérison (étant définie comme le maintien d'une pression artérielle sans traitement) contrairement à l'HTA primitive dont l'origine est multifactorielle.
Les données sur la prévalence de l'HTA secondaire5, 6 sont disparates et hétérogènes selon les études, oscillant entre 15 et 30 % des patients hypertendus (plutôt 10 % en population de médecine générale « tout venant » et 30 % en centres spécialisés après une pré-sélection des patients hypertendus). Cette prévalence augmente considérablement en cas d'HTA résistante (où elle avoisine les 50 %) et aussi chez les patients de moins de 40 ans. Si l'on rapporte ce chiffre de 15 à 30 % à la prévalence de 17 millions d'hypertendus en France, il est évident qu'il existe une sous-détection importante des HTA secondaires.
La détection de ces formes d'HTA secondaire représente donc un défi diagnostique majeur avec des implications thérapeutiques et pronostiques certaines.
La découverte d'une hypertension artérielle doit systématiquement inclure :
1. La confirmation du diagnostic grâce à des automesures tensionnelles
2. Une évaluation et une prise en charge du risque cardiovasculaire global
2. Une évaluation du retentissement sur les organes cibles incluant un bilan minimal
3. La recherche de points d'appel en faveur d'une HTA secondaire.
Étiologies de l'HTA secondaire : À quoi penser ?
Les principales étiologies d'HTA secondaires, résumés dans le [Tableau 1], sont dominés par les causes endocrines, rénales, réno-vasculaires et toxiques et iatrogènes.
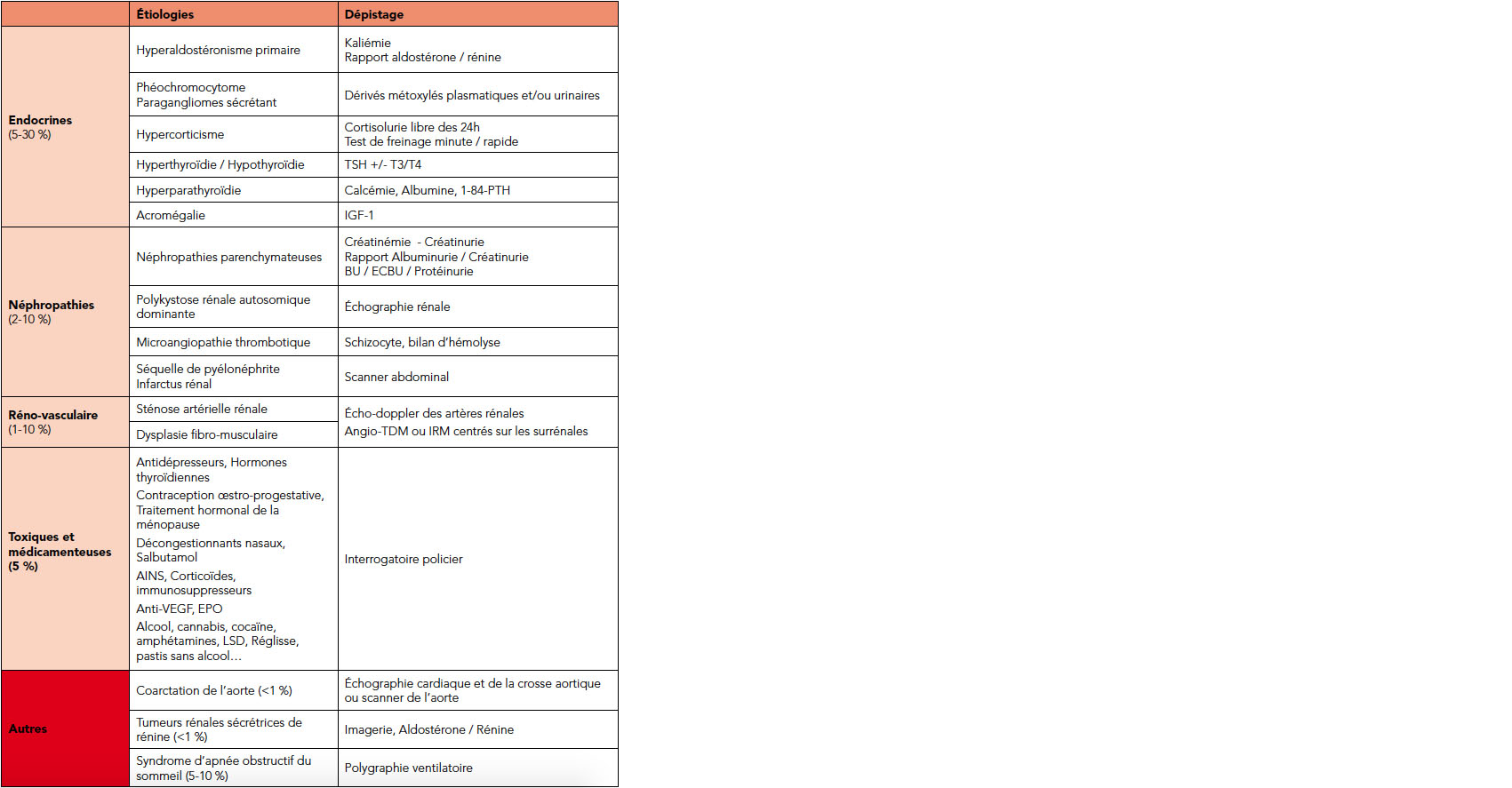
Tableau 1 : Principales causes d'HTA secondaires
L'hyperaldostéronisme primaire représente de loin la première cause d'HTA secondaire avec 6 % de patients hypertendus en population générale mais ce chiffre peut s'élever jusqu'à 35 % de prévalence en cas d'HTA résistante bénéficiant d'une évaluation dans un centre tertiaire. Cette forme d'HTA secondaire est associée à une atteinte des organes cibles accrue et à une augmentation du risque cardiovasculaire, indépendamment des chiffres de pression artérielle7-8. La manifestation la plus courante est l'hyperplasie bilatérale des surrénales mais il peut s'agir de formes unilatérales, tels que l'adénome de Conn (l'hyperplasie des surrénales étant neuf fois plus fréquente que l'adénome de Conn).
Le diagnostic est complexe et repose sur le rapport aldostérone/rénine plasmatique. Il est important de noter qu'une kaliémie normale et un scanner surrénalien normal ne permettent pas toujours d'exclure le diagnostic. De, plus, les conditions de prélèvement doivent être scrupuleusement respectées afin de permettre une mesure standardisée tenant compte des fluctuation de ces hormones en fonction de la volémie, de la kaliémie et du traitement médicamenteux. Ce bilan doit ainsi être réalisé, le matin à jeun, plus de 2h après le lever et en position assise depuis au moins 15 minutes avec 2 mesures consécutives. Le régime normo- sodée doit être contrôlé (par une natriurèse entre 100 et 200 mmol/ 24h) ainsi que la normokaliémie. De surcroît, le dosage doit être réalisé sous traitement neutre c'est-à -dire que les bétabloquants, les bloqueurs du SRA et les diurétiques thiazidiques sont à arrêter 2 semaines avant le dosage et les antagonistes des récepteurs aux minéralocorticoïdes 6 semaines avant. Les pilules oestro-progestatives, les AINS et les corticoïdes sont à arrêter 3 mois avant. Dans ce contexte, il est possible de relayer le traitement anti-hypertenseur par un traitement neutre pouvant comprendre des inhibiteurs calciques d'action longue et/ou des alpha- bloquants. Depuis les dernières recommandations l'ESC 2024, un dosage du rapport aldostérone sur rénine plasmatique est désormais recommandé en première intention chez tous les patients avec une HTA confirmée avec un niveau de recommandation IIa/B.
Le dosage plasmatique et/ou urinaire des dérivés métoxylés (normétanéphrines) permet de dépister un éventuel phéochromocytome (80-85 %) ou un paragangliome (15-20 %). Les normétanéphrines urinaires doivent obligatoirement faire l'objet des recueil des urines des 24h. Bien que la prévalence soit faible (0,2-0,6 %)9-10, leur détection reste cruciale.
Le cortisol libre urinaire sur 24h est l'examen à privilégier pour le dépistage d'un hypercorticisme avec la réalisation d'un test de freinage à la dexaméthasone à minuit avec dosage du cortisol plasmatique le matin à 8h. Même si 80 % des patients présentant un hypercorticisme sont hypertendus, elle représente moins de 1 % (0,1 %) des d'HTA secondaires11.
La sténose des artères rénales qu'elle soit athéromateuse ou secondaire à une dysplasie fibro-musculaire doit être évoquée devant un souffle des artères rénales, la notion d'OAP flashs sans explication cardiologique, une élévation de la créatinine supérieure à 30 % après introduction d'un bloqueur du SRA, ou encore une asymétrie rénale.
Sa prévalence en population générale varie de 1 à 8 % mais elle peut atteindre 30 % en cas de signes d'athérosclérose multisite12. Le dépistage peut être réalisée grâce à une échographie doppler des artères (souvent en première intention actuellement) mais l'examen le plus performant pour le diagnostic est l'angioscanner des artères rénales ou à défaut l'angio-IRM en cas de contre-indication. La stratégie diagnostique est débattue actuellement sur la place respective de l'échographie doppler et de l'angioscanner des artères rénales.
En effet, l'échographie doppler avant la réalisation de l'angioscanner des artères rénales pourrait majorer un risque de faux négatif et de « rater » des diagnostics.
Sa réalisation après l'angioscanner des artères rénales ciblerait alors plus une évaluation affinée du caractère fonctionnel et de l'hémodynamique d'une sténose objectivée par scanner.
La maladie rénale chronique est également une cause très fréquente d'HTA (incluant les néphropathies glomérulaires, la néphropathie diabétique, les maladies polykystiques rénales mais aussi de manière plus anecdotique le syndrome de Liddle ou de Gordon).
La majorité des patients atteints de néphropathies parenchymateuses sont atteints d'HTA et l'incidence de l'HTA augmente avec le déclin de la fonction rénale.
À l'inverse l'HTA, en particulier mal contrôlé aggrave le pronostic rénal et le déclin du débit de filtration glomérulaire13-14.
La polygraphie ventilatoire permet de dépister un syndrome d'apnée obstructive du sommeil (SAOS) dont la prévalence est importante même en l'absence de signes évocateurs. Bien que le SAOS affecte considérablement la prévalence de l'HTA, le traitement du SAOS ne normalise pas toujours les valeurs tensionnelles, soulignant la complexité de déterminer le caractère secondaire de l'HTA liée au SAOS.
Enfin, l'interrogatoire de tout patient doit être « policier » afin de dépister une cause toxique ou iatrogène.
Quand un arrêt du traitement incriminé est possible, le simple arrêt peut permettre de corriger « simplement » une HTA. Quand cela n'est pas possible, le traitement anti-hypertenseur doit intégrer cette donnée dans le choix de la molécule (Par exemple privilégier les bétabloquants en cas d'HTA induite par les oestroprogestatifs, les antagonistes des récepteurs aux minéralocorticoïdes en cas d'HTA induite par les corticoïdes en association avec des diurétiques en cas de rétention hydrosodée associée et les inhibiteurs calciques en cas d'HTA secondaires à des AINS ou de l'EPO).
Le spectre des HTA secondaires dépend également de l'âge15 [Figure 1]. Si le diagnostic de coarctation de l'aorte se fait généralement dans l'enfance, il peut passer inaperçu et n'être découvert qu'à l'âge adulte.
Dans le cadre de l'HTA réno-vasculaire, l'âge permet d'orienter vers une origine dysplasique fibro-musculaire ou une sténose des artères rénales secondaire à de l'athérosclérose qui touchera d'avantage les sujets plus âgé. Enfin, les maladies endocrines se révèlent essentiellement chez l'adulte actif, entre 13 et 65 ans, le syndrome de Cushing étant plutôt l'apanage des sujets âgés et le phéochromocytome impactant des sujets plus jeunes.

Figure 1 : Incidences des HTA secondaires selon l'âge (adapté des Guidelines de l'ESH 2023)15
Screening de l'HTA secondaire : Quand y penser ?
Ainsi, si la recherche d'une HTA secondaire par un bilan exhaustif chez tous les patients présentant une HTA n'est ni recommandé ni réalisable en pratique courante en regard du nombre de patients que cela implique ; la recherche de points d'appel en faveur d'une étiologie secondaire doit être systématique [Tableau 2].
Ces points d'appels intègrent le terrain du patient, les signes fonctionnels et d'examen physique, mais aussi le bilan biologique « de base » recommandé devant toute HTA.
Le bilan biologique recommandé par la Haute Autorité de santé (HAS) comprend :
• Glycémie / Hémoglobine glyquée.
• Kaliémie ou ionogramme sanguin.
• Créatinémie, BU +/- Recherche d'une protéinurie.
• Exploration des anomalies lipidiques.
À ce bilan systématique, un bilan recherchant des causes d''HTA secondaire [Tableau 1] pourra être adjoint dans les situations décrites dans le Tableau [2] :
• Rapport aldostérone / rénine +/- test dynamiques spécifiques.
• TSH +/- T3/T4, calcium, albumine, PTH.
• Cortisol libre urinaire 24h +/- test de freinage à la dexaméthasone avec cortisol à 8h.
• Dérivés métoxylés (métanéphrines) plasmatiques et/ou urinaires sur 24h.
• Échographie-doppler des artères rénales / Angioscanner des artères rénales +/- avec des coupes centrées sur les surrénales.
• Polygraphie ventilatoire.
• ETT.

Tableau 2 : Points d'appel cliniques et biologiques en faveur d'une HTA secondaire
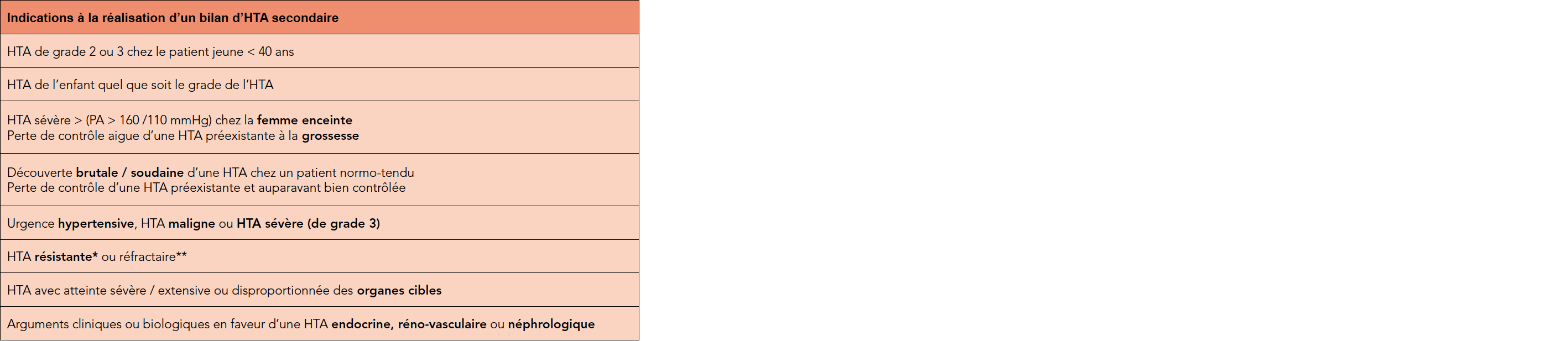
HTA résistante : Persistance d'une PAS supérieure à 140/90 mmHg en mesure de consultation malgré l'association des règles hygiénodiététiques et d'une trithérapie à dose maximale tolérée incluant un diurétique thiazidique, un bloqueur du système rénine angiotensine aldostérone et un inhibiteur calcique avec une bonne observance.
HTA réfractaire : Persistance d'une PAS supérieure à 140 /90 mmHg en mesure de consultation malgré l'adjonction d'un antagoniste des récepteurs aux minéralocorticoïdes à cette trithérapie avec une bonne observance.
Savoir passer le relai : Quand et à qui adresser ?
Le diagnostic d'une HTA secondaire peut être complexe et faire appel à des connaissances multidisciplinaire et spécialisée nécessitant l'adressage du patient au spécialiste concerné selon l'étiologie suspectée.
Une collaboration étroite est essentielle entre les différents spécialistes concernés par l'HTA (cardiologues, néphrologues, endocrinologues, médecins ou chirurgiens vasculaires, vasculaires…).
Les « European Excellence Centers » et les « Blood Pressure Clinic » sont des centres d'excellence européens en hypertension artérielle reconnus et validés par l'European Society of Hypertension (ESH). Ces centres tertiaires offrent une structure idéale et réunissent des équipes transversales et pluridisciplinaires expertes dans le diagnostic et la prise en charge des cas d'HTA les plus complexes.
En cas de situation équivoque, d'anomalies relevées lors du bilan d'HTA secondaire ou même de bilan d'HTA secondaire négatif avec la persistance d'une conviction clinique forte ; le recours à ces centre experts est fortement recommandé. Le maillage sur le territoire français [Figure 2] de ces centres doit permettre le recours à des avis spécifiques l'adressage des patients afin de permettre de meilleurs performances dans le diagnostic d'HTA.

Figure 2 : Répartition géographiques des centres-experts en HTA
Conclusion / Les messages-clés
• L'HTA secondaire, c'est très fréquent (Au minimum 10 % d'une maladie qui touche 17 millions de personnes en France) et largement sous-diagnostiquée en raison d'un défaut de bilans d'HTA secondaire !
• Rater un diagnostic d'HTA secondaire, c'est manquer une opportunité de diminuer le risque d'événement cardiovasculaire, de diminuer l'atteinte des organes cibles, de mieux contrôler la pression artérielle et même parfois de guérir une HTA.
• Les étiologies de l'HTA secondaire sont dominées par les causes endocrines, rénales, réno-vasculaires et toxiques & médicamenteuses.
• L'hyperaldostéronisme primaire est la première cause d'HTA secondaire mais le diagnostic est particulièrement exigeant. Il faut savoir répéter les examens et prendre le temps de réunir les conditions optimales pour l'interprétation du bilan d'hyperaldostéronisme.
• Il faut savoir éliminer les causes « facilement » identifiables d'HTA secondaire grâce à un interrogatoire policier, des questionnaires standardisés et un examen clinique ciblé.
• Il faut savoir traquer les points d'appel en faveur d'une étiologie secondaire en « ayant en tête le listing » des étiologies. On trouve ce qu'on cherche et on cherche ce que l'on connait.
• Toute HTA avant 40 ans, résistante, de grade III, avec atteinte sévère des organes cibles ou d'évolution soudaine doit faire rechercher une HTA secondaire.
• Il faut savoir être persévérant et répéter les examens : la plupart des examens dans le bilan d'HTA peuvent être pris en défaut et leur normalité ne suffit pas toujours à exclure le diagnostic.
• L'HTA secondaire nécessite une approche transversale et multidisciplinaire avec une collaboration étroite entre les différents spécialistes.
• Il faut savoir adresser les patients en centres-experts qui sont répartis sur tout le territoire et réunissent des équipes expertes dans le diagnostic et la prise en charge de l'HTA secondaire.
Bibliographie
1. Foreman KJ, Marquez N, Dolgert A, et al. Forecasting life expectancy, years of life lost, and all-cause and cause-specific mortality for 250 causes of death: reference and alternative scenarios for 2016–40 for 195 countries and territories. Lancet 2018 ; 392:2052–90.
2. Rubin S, Boulestreau R, Couffinhal T, Combe C, Girerd X. Impaired hypertension control in France: What the nephrologist needs to know. 2020; 16:347–52.
3. Rossi GP, Bisogni V, Rossitto G, Maiolino G, Cesari M, Zhu R, Seccia TM. Practice Recommendations for Diagnosis and Treatment of the Most Common Forms of Secondary Hypertension. High Blood Press Cardiovasc Prev. 2020 Dec;27(6):547-560.
4. Chiong JR, Aronow WS, Khan IA, Nair CK, Vijayaraghavan K, Dart RA, et al. Secondary hypertension: current diagnosis and treatment. Int J Cardiol. 2008;124:6–21.
5. Azizi M, Sapoval M, Gosse P, Monge M, Bobrie G, Delsart P, et al. Optimum and stepped care standardised antihypertensive treatment with or without renal denervation for resistant hypertension (DENERHTN): a multicentre, open label, randomised controlled trial. Lancet. 2015; 385:1957–1965.
6. Rossi GP, Rossitto G, Amar L, Azizi M, Riester A, Reincke M, et al. Prevalence and outcome of drug-resistant hypertension in primary aldosteronism patients undergoing adrenal vein sampling. Eur J Prev Cardiol. 2020.
7. Mulatero P, Monticone S, Deinum J, Amar L, Prejbisz A, Zennaro M-C, et al. Genetics, prevalence, screening and confirmation of primary aldosteronism. J Hypertens. 2020.
8. Rossi GP. Primary aldosteronism: JACC state-of-the-art review. J Am Coll Cardiol. 2019;74:2799–2811.
9. Lenders JWM, Duh QY, Eisenhofer G, Gimenez-Roqueplo AP, Grebe SKG, Murad MH, et al. Pheochromocytoma and paraganglioma: an endocrine society clinical practice guideline. J Clin Endocrinol Metab. 2014;99:1915–1942.
10. Lenders JWM, Kerstens MN, Amar L, Prejbisz A, Robledo M, Taieb D, et al. Genetics, diagnosis, management and future directions of research of pheochromocytoma and paraganglioma: a position statement and consensus of the Working Group on Endocrine Hypertension of the European Society of Hypertension. J Hypertens. 2020;38:1443–1456.
11. Rimoldi SF, Scherrer U, Messerli FH. Secondary arterial hypertension: when, who, and how to screen? Eur Heart J. 2014;35:1245–1254.
12. Hansen KJ, Edwards MS, Craven TE, et al. Prevalence of renovascular disease in the elderly: a population-based study. J Vasc Surg.
13. Rao MV, Qiu Y, Wang C, Bakris G. Hypertension and CKD: Kidney Early Evaluation Program (KEEP) and National Health and Nutrition Examination Survey (NHANES), 1999-2004. Am J Kidney Dis. 2008 Apr;51(4 Suppl 2):S30-7.
14. Hamrahian SM, Falkner B. Hypertension in Chronic Kidney Disease. Adv Exp Med Biol. 2017;956:307-325.
15. Mancia G et al. 2023 ESH Guidelines for the management of arterial hypertension The Task Force for the management of arterial hypertension of the European Society of Hypertension: Endorsed by the International Society of Hypertension (ISH) and the European Renal Association (ERA). J Hypertens. 2023 Dec 1;41(12):1874-207.

Nabil BOUALI
CCF, CJH, Poitiers

Dr Guillaume LAMIRAULT
SFHTA, SFC, CJH
Nantes

