Définitions
Les RILI se caractérisent par des dommages du parenchyme pulmonaire, de la plèvre ou de l'arbre trachéobronchique, à la suite d'une exposition aux rayonnements ionisants. Il existe deux principales phases interdépendantes qui peuvent être clairement séparées dans le temps :
- Les toxicités respiratoires aiguës, incluant la pneumopathieradique (RP), la pleurite, la trachéite et la bronchite, surviennent généralement dans les 6 mois suivant la radiothérapie (3).
- Les formes chroniques et tardives, qui se manifestent au moins 6 mois après la fin de la radiothérapie, avec une fibrose radique, qui est une maladie cicatricielle pouvant considérablement réduire la fonction pulmonaire. Ces formes chroniques peuvent se développer chez des patients n'ayant pas connu de phase aiguë, bien que la fibrose puisse être considérée comme l'entité finale d'un continuum physiopathologique (4).
Certaines formes particulières de RILI existent, notamment la pneumopathie organisée (anciennement appelée bronchiolite oblitérante avec pneumonie organisée, BOOP) (5) et la pneumopathie radique de rappel (6). Les autres sujets d'intérêt comprennent l'association radiothérapie thoracique et traitements systémiques (chimiothérapie, hormonothérapie, thérapie ciblée, immunothérapie), les spécificités de la radiothérapie stéréotaxique pulmonaire, l'association avec les comorbidités cardiaques et les maladies pulmonaires interstitielles préexistantes (ILD).
Épidémiologie
Environ 10 % à 20 % des patients présentent des signes de RILI d'une gravité variable (7). L'incidence estimée des RILI varie considérablement selon les études, en fonction de la localisation traitée, du grade, du type de RILI, ainsi que de la technique de radiothérapie utilisée.
Facteurs de risque
Les principaux facteurs de risque validés comprennent les facteurs de risque dosimétriques, les pneumopathies chroniques préexistantes (ex : fibrose pulmonaire idiopathique), un volume tumoral important, une tumeur située dans les lobes moyen ou inférieurs, les situations de ré-irradiation.
Diagnostic différentiel
Les signes et symptômes de RILI ne sont pas spécifiques. Les principaux diagnostics différentiels incluent les infections pulmonaires, les toxicités respiratoires induites par la chimiothérapie ou l'immunothérapie, les symptômes liés à la tumeur (obstruction, atélectasie, lymphangite, récidive, progression), les symptômes ou exacerbations liés à une pneumopathie préexistante (par exemple, BPCO), l'embolie pulmonaire, l'insuffisance cardiaque, les arythmies cardiaques et l'anémie. Le diagnostic de RILI ne peut être posé qu'après avoir exclu ces diagnostics (8).
Pneumopathie radique aiguë (RP)
La RP survient généralement entre 1 et 6 mois après la radiothérapie (3). Les symptômes les plus fréquents incluent une dyspnée légère à sévère (parfois sifflante) et une toux sèche non productive (9). Les patients peuvent également présenter une exacerbation de symptômes respiratoires préexistants, de la fièvre ou d'autres symptômes aspécifiques. L'auscultation pulmonaire peut être normale, bien que des râles crépitants, un frottement pleural, ainsi qu'un épanchement pleural, puissent être présents.
Une tomodensitométrie (CT) injectée offre une sensibilité accrue par rapport à la radiographie pour la détection des RILI, ce qui permet d'éliminer les diagnostics différentiels fréquents et d'exclure, par exemple, une embolie pulmonaire. Par conséquent, la radiographie thoracique est obsolète.
Deux caractéristiques majeures se dégagent sur l'imagerie :
- La RP est généralement limitée au champ d'irradiation et ne respecte pas les limites anatomiques (scissures ou lobes) (10).
- Il n'existe pas d'association claire entre les manifestations cliniques et radiologiques.
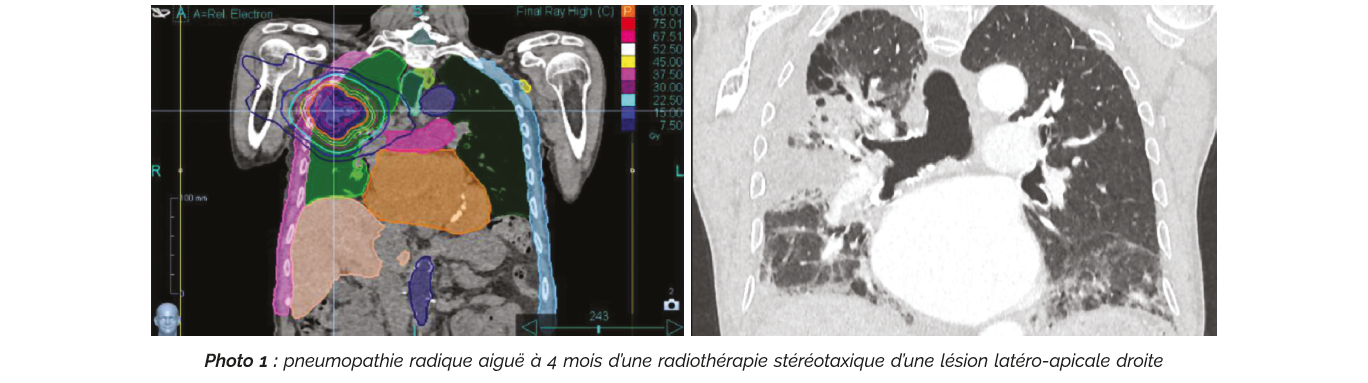
La RP se manifeste par des opacités en verre dépoli, des condensations pseudonodulaires ou arciformes, ou encore des bronchectasies de traction, avec d'éventuels épanchements pleuraux, interlobulaires ou péricardiques.
Les tests de fonction pulmonaire (plethysmographie et capacité de diffusion du monoxyde de carbone [DLCO]) sont recommandés, lorsqu'ils peuvent être réalisés en phase aiguë, et sont essentiels pour le suivi. Ils révèlent des troubles restrictifs avec réduction des volumes et de la compliance, une diminution du volume expiratoire maximal par seconde (VEMS) et de la capacité vitale forcée (CVF), une augmentation du rapport VEMS/CVF, ainsi qu'une diminution de la DLCO (11).
La DLCO réalisée après radiothérapie est essentielle pour évaluer et surveiller les anomalies respiratoires au cours du suivi (12). Ces troubles sont généralement combinés avec des troubles obstructifs préexistants. La biologie sanguine peut révéler des anomalies aspécifiques avec un syndrome inflammatoire biologique.
Bien que non systématique, une bronchoscopie avec lavage broncho-alvéolaire réalisée chez les patients ayant une fonction respiratoire suffisante peut être utile pour le diagnostic différentiel avec une lymphangite carcinomateuse, une infection, un saignement ou une hypersensibilité médicamenteuse.
Le système de classification à utiliser est celui de la « Common Terminology Criteria for Adverse Events (CTCAE) » version 5.0 (13).
La RP est traitée en fonction du grade. Le traitement n'est initié qu'une fois que les patients deviennent symptomatiques (Grade supérieure ou égale à 2) et il implique généralement des glucocorticoïdes oraux à haute dose administrés sur le long terme en association avec une antibiothérapie si une infection n'a pas pu être éliminée. L'inhalation de corticoïdes et de bronchodilatateurs (budesonide et formotérol) peut compléter la prise en charge.
Les patients correctement diagnostiqués et traités de manière appropriée avec des glucocorticoïdes à haute dose ont généralement un bon pronostic, avec une possible résolution des symptômes et des anomalies radiologiques (11).
Une consultation en pneumologie doit faire partie du suivi systématique.
Fibrose pulmonaire radio-induite (RF)
La (RF) survient généralement à partir de 6 mois après la fin de l'irradiation, les lésions se consolidant 24 mois après la fin de la radiothérapie (4). Elle peut survenir chez des patients sans antécédents de pneumopathie radique (RP).
Les patients peuvent être asymptomatiques, ou bien présenter une dyspnée progressive. Cette maladie chronique peut également se présenter par une aggravation des symptômes antérieurs. Des infections bronchiques récurrentes en raison des bronchectasies de traction dans la zone de fibrose sont également possibles.
Les symptômes et l'auscultation sont non spécifiques ou peuvent retrouver les mêmes signes que la RP.
Il n'existe aucune association évidente entre clinique et imagerie. Comme dans la RP, le scanner thoracique (CT) injecté est la technique d'imagerie de choix. Les principales anomalies radiologiques radio-induites sont des anomalies localisées dans les champs d'irradiation qui ne suivent pas la systématisation lobaire, avec des lésions se conformant aux isodoses (10).
La RF au CT se manifeste par des opacités rétractiles avec des signes de fibrose, des bronchectasies destructives, un épaississement pleural, une attraction de la trachée et du médiastin vers la région irradiée, et une perte de volume (14).
Lorsque cela est possible, des explorations fonctionnelles respiratoires doivent être réalisés au moment du diagnostic et sont essentielles pour le suivi. Elles montrent les mêmes altérations que celles décrites dans la RP.
La prise en charge de la RF est identique à celle des fibroses pulmonaires non induites par la radiothérapie, pour lesquelles aucun traitement efficace n'existe à ce jour. Elle inclut des mesures palliatives et symptomatiques, notamment une prise en charge respiratoire spécialisée par un pneumologue, un traitement de l'encombrement bronchique par kinésithérapie respiratoire et une réadaptation cardio-respiratoire. Les corticostéroïdes et autres agents anti-inflammatoires sont inappropriés.
L'évolution dépend du grade, devenant plus défavorable aux stades avancés.
Le suivi doit être alterné avec un pneumologue, un kinésithérapeute et, dans certains cas, un cardiologue pour la prise en charge de l'hypertension artérielle pulmonaire ou du cœur pulmonaire chronique.
Pneumonie organisée
La pneumonie organisée (anciennement connue sous le nom de bronchiolite oblitérante avec pneumonie organisée ou BOOP), également appelée pneumonie organisée cryptogénique, survient généralement entre 1 et 6 mois après la radiothérapie.
C'est une maladie interstitielle pulmonaire rare, presque exclusivement rapportée après une radiothérapie chez les femmes ayant subi une chirurgie conservatrice du sein. Elle peut être asymptomatique et découverte uniquement par imagerie. Les symptômes et l'auscultation sont similaires à ceux de la pneumopathie radique (RP). Cette maladie est probablement sous-diagnostiquée en raison de sa similarité avec la RP.
Les résultats au scanner thoracique (CT) injecté montrent des opacités alvéolaires, périphériques, sous-pleurales et migratrices. En effet, ces opacités sont initialement confinées à la zone irradiée avant de se propager au parenchyme non traité, ce qui différencie la pneumonie organisée de la RP.
La prise en charge dépend du grade de la pneumonie organisée et correspond à celle de la RP. La spécifi cité concerne la corticothérapie orale : 0,75 mg/kg/jour de prednisone pendant 4 semaines, puis 0,5 mg/kg/jour pendant 4 semaines, avant de réduire très progressivement la dose sur une période de 6 à 24 mois en raison du risque élevé de rebond après l'arrêt. L'inhalation de corticoïdes et de bronchodilatateurs (budesonide et formotérol) peut compléter la prise en charge. La reprise d'une dose plus élevée de corticoïdes sur une période prolongée permet de contrôler rapidement toute rechute (5).
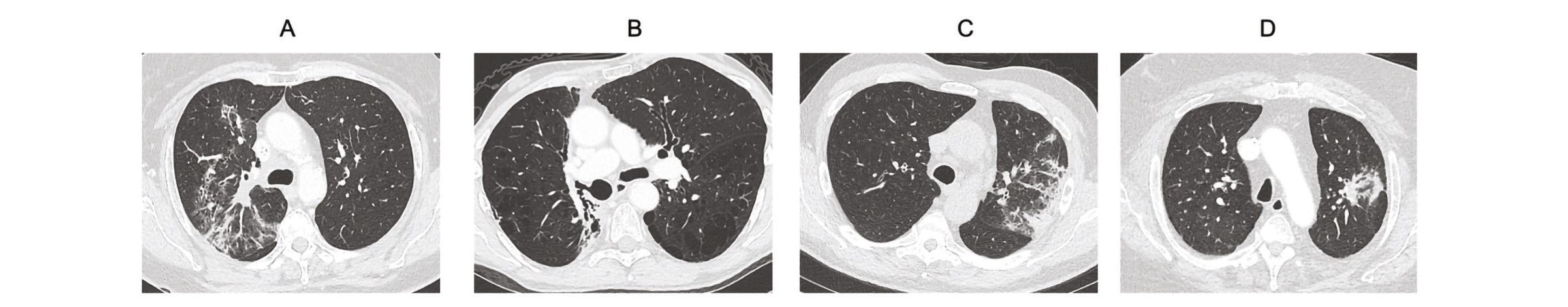
A, Pneumopathie radique aigue lobaire supérieure droite. B, Fibrose radique hilaire droite 8 ans après la fin de la radiothérapie.
C, Pneumopathie organisée après SBRT du lobe supérieur gauche. D, Remaniements radiologiques plusieurs années après SBRT
Pneumopathie de rappel radio-induite
La pneumopathie de rappel radio-induite (RRP) est une réaction inflammatoire aiguë rare et imprévisible survenant dans une zone préalablement irradiée après l'introduction d'agents systémiques. Les patients développent ou redéveloppent une pneumopathie radique (RP), avec des délais d'apparition allant de quelques jours à plusieurs mois après l'irradiation.
Les symptômes et l'auscultation sont similaires à ceux de la RP. Les agents systémiques incluent des traitements oncologiques spécifiques ainsi que des traitements non oncologiques.
Le scanner thoracique (CT) révèle des opacités en verre dépoli, une opacité diffuse, des infiltrats ou une consolidation péribronchique dans le poumon irradié, similaires à la RP (15) bien que l'évolution soit plus lente (16).
La RRP répond généralement bien au traitement par corticoïdes, avec souvent une résolution complète. La prise en charge correspond à celle de la RP. Le traitement systémique déclencheur doit être arrêté pendant la phase aiguë.
Traitements augmentant le risque d'effets secondaires respiratoires radio-induits
Lorsqu'ils sont combinés avec une radiothérapie thoracique, la plupart des traitements oncologiques spécifiques peuvent augmenter le risque de toxicités pulmonaires (17), y compris celui de RRP et de pneumonie organisée. Une liste exhaustive de médicaments, incluant ceux utilisés en oncologie et en traitements non-oncologiques, impliqués dans la iatrogénèse pulmonaire et favorisant les RILI est disponible sur le site suivant : https://www.pneumotox.com/drug/index/. Par ailleurs, un site développé récemment par la SFRO intitulé « radio-sync », disponible gratuitement en ligne, recense la plupart des traitements oncologiques et donne la conduite à tenir pour l'arrêt ou la poursuite du traitement en cours de radiothérapie, avec le nombre de jours d'arrêt nécessaire le cas échéant.
RILI et SBRT
La SBRT pulmonaire est généralement sûre et efficace (18), avec peu de toxicités de grade 4 et 5 pour les tumeurs périphériques. Le risque de toxicité est accru pour les tumeurs centrales et encore plus pour les tumeurs ultracentrales. Les tumeurs centrales sont celles situées 2 cm autour de l'arbre trachéobronchique/médiastinal, et les tumeurs ultracentrales sont celles avec un chevauchement entre le volume cible planifié (PTV) et l'arbre trachéobronchique/médiastinal (19).
Les facteurs de risque de toxicité de grade 5 pour les tumeurs centrales/ultra-centrales incluent :
- Le non-respect des contraintes dosimétriques sur l'arbre trachéobronchique.
- Les traitements anti-plaquettaires/anticoagulants (hémoptysie).
- Les tumeurs endobronchiques (hémoptysie et fi stule).
- L'association avec des thérapies ciblées, notamment les anti-VEGF (hémoptysie), et, moins bien caractérisées, les TKI, les anti-BRAF et les inhibiteurs de MEK, ainsi que l'immunothérapie comme les anti-CTLA4 (20).
- Les maladies pulmonaires interstitielles préexistantes (pneumopathies).
Les recommandations de bonnes pratiques en SBRT et les mesures clés pour prévenir les complications associées aux tumeurs ultra-centrales ont été fournies par l'International Stereotactic Radiosurgery Society (21).
Radiothérapie et maladies pulmonaires interstitielles préexistantes (ILD)
Les maladies pulmonaires interstitielles (ILD) constituent un groupe très hétérogène de pathologies, parfois associées à une fibrose pouvant s'étendre. La fibrose pulmonaire idiopathique est la forme la plus fréquente d'ILD après la sarcoïdose. Radiologiquement, ces pathologies se manifestent souvent par une pneumopathie interstitielle commune, caractérisée par des aspects en "rayons de miel" et des bronchectasies de tractions. Les ILD fibrosantes, notamment avec des images en "rayons de miel", représentent un facteur de risque majeur de RILI et d'exacerbations aiguës des ILD (22). Toute suspicion d'ILD doit être explorée par un pneumologue (explorations fonctionnelles respiratoires, DLCO, scanner, ajustement des traitements pulmonaires) avant de commencer une radiothérapie. Le risque de toxicité varie selon l'étiologie des maladies pulmonaires fibrosantes. Deux entités présentent un risque majeur :
- La fibrose pulmonaire idiopathique (23).
- Les ILD fibrosantes avec "rayons de miel" (notamment celles induites par la polyarthrite rhumatoïde et la pneumopathie d'hypersensibilité chronique).
Conclusions
Le profil des RILI évolue avec des complications spécifiques liées à la SBRT, à l'association avec des traitements oncologiques récents, notamment les TKI et l'immunothérapie, et à certaines pathologies comme les ILD ou les comorbidités cardiaques. La détection et la prise en charge rapide de ces effets secondaires sont essentielles pour assurer une bonne prise en charge des patients. Les principales mesures préventives incluent : le respect des contraintes dosimétriques, la réduction des facteurs de risque modifiables de RILI, l'utilisation de techniques innovantes telles que l'IMRT. Les RILI restent un diagnostic d'élimination, et les diagnostics différentiels les plus fréquents doivent être écartés. La réduction des risques de RILI passera essentiellement par l'intégration continue de nouvelles techniques innovantes, comme la radiothérapie guidée par imagerie fonctionnelle.
Références
1. Vallard A, Rancoule C, Le Floch H, Guy JB, Espenel S, Le Péchoux C, et al. [Medical prevention and treatment of radiation-induced pulmonary complications]. Cancer Radiother J Soc Francaise Radiother Oncol. Août 2017;21(5):411-23.
2. Hanania AN, Mainwaring W, Ghebre YT, Hanania NA, Ludwig M. Radiation-Induced Lung Injury: Assessment and Management. Chest. juill 2019;156(1):150-62.
3. Marks LB, Yu X, Vujaskovic Z, Small W, Folz R, Anscher MS. Radiation-induced lung injury. Semin Radiat Oncol. juill 2003;13(3):333-45.
4. Graves PR, Siddiqui F, Anscher MS, Movsas B. Radiation pulmonary toxicity: from mechanisms to management. Semin Radiat Oncol. juill 2010;20(3):201-7.
5. Epler GR, Kelly EM. Post-Breast Cancer Radiotherapy Bronchiolitis Obliterans Organizing Pneumonia. Respir Care. mai 2020;65(5):686-92.
6. Jan PR, Chang JWC, Wu CE. Radiation Recall Pneumonitis: A Rare Syndrome That Should Be Recognized. Cancers. 24 sept 2022;14(19):4642.
7. Kuipers ME, van Doorn-Wink KCJ, Hiemstra PS, Slats AM. Predicting radiation-induced lung injury in lung cancer patients - challenges and opportunities: Predicting radiation-induced lung injury. Int J Radiat Oncol Biol Phys. 2 nov 2023;S0360-3016(23)08049-5.
8. De Ruysscher D, Niedermann G, Burnet NG, Siva S, Lee AWM, Hegi-Johnson F. Radiotherapy toxicity. Nat Rev Dis Primer. 21 févr 2019;5(1):13.
9. Yue J, Shi Q, Xu T, Jeter M, Chen TY, Komaki R, et al. Patient-reported lung symptoms as an early signal of impending radiation pneumonitis in patients with nonsmall cell lung cancer treated with chemoradiation: an observational study. Qual Life Res Int J Qual Life Asp Treat Care Rehabil. juin 2018;27(6):1563-70.
10. Ghaye B, Wanet M, El Hajjam M. Imaging after radiation therapy of thoracic tumors. Diagn Interv Imaging. Oct 2016;97(10):1037-52.
11. Bledsoe TJ, Nath SK, Decker RH. Radiation Pneumonitis. Clin Chest Med. juin 2017;38(2):201-8.
12. Gopal R, Starkschall G, Tucker SL, Cox JD, Liao Z, Hanus M, et al. Effects of radiotherapy and chemotherapy on lung function in patients with non smallcell lung cancer. Int J Radiat Oncol Biol Phys. 1 mai 2003;56(1):114-20.
13. Common Terminology Criteria for Adverse Events (CTCAE). 2017.
14. Choi YW, Munden RF, Erasmus JJ, Park KJ, Chung WK, Jeon SC, et al. Eff ects of radiation therapy on the lung: radiologic appearances and diff erential diagnosis. Radiogr Rev Publ Radiol Soc N Am Inc. 2004;24(4):985-97; discussion 998.
15. Cousin F, Desir C, Ben Mustapha S, Mievis C, Coucke P, Hustinx R. Incidence, risk factors, and CT characteristics of radiation recall pneumonitis induced by immune checkpoint inhibitor in lung cancer. Radiother Oncol. avr 2021;157:47-55.
16. Ding X, Ji W, Li J, Zhang X, Wang L. Radiation recall pneumonitis induced by chemotherapy after thoracic radiotherapy for lung cancer. Radiat Oncol Lond Engl. 6 mars 2011;6:24.
17. Vogelius IR, Bentzen SM. A literature-based meta-analysis of clinical risk factors for development of radiation induced pneumonitis. Acta Oncol Stockh Swed. Nov 2012;51(8):975-83.
18. Yamashita H, Takahashi W, Haga A, Nakagawa K. Radiation pneumonitis after stereotactic radiation therapy for lung cancer. World J Radiol. 28 sept 2014;6(9):708-15.
19. Manyam BV, Verdecchia K, Videtic GMM, Zhuang T, Woody NM, Wei W, et al. Validation of RTOG 0813 Proximal Bronchial Tree Constraints for Pulmonary Toxicity With Stereotactic Body Radiation Therapy for Central Non-small Cell Lung Cancer. Int J Radiat Oncol Biol Phys. 1 mai 2020;107(1):72-8.
20. Kroeze SGC, Pavic M, Stellamans K, Lievens Y, Becherini C, Scorsetti M, et al. Metastases-directed stereotactic body radiotherapy in combination with targeted therapy or immunotherapy: systematic review and consensus recommendations by the EORTC–ESTRO OligoCare consortium. Lancet Oncol. mars 2023;24(3):e121-32.
21. Yan M, Louie AV, Kotecha R, Ashfaq Ahmed M, Zhang Z, Guckenberger M, et al. Stereotactic body radiotherapy for Ultra-Central lung Tumors: A systematic review and Meta-Analysis and International Stereotactic Radiosurgery Society practice guidelines. Lung Cancer. août 2023;182:107281.
22. Torre-Bouscoulet L, Muñoz-Montaño WR, Martínez-Briseño D, Lozano-Ruiz FJ, Fernández-Plata R, Beck-Magaña JA, et al. Abnormal pulmonary function tests predict the development of radiation-induced pneumonitis in advanced non-small cell lung Cancer. Respir Res. 24 avr 2018;19(1):72.
23. Kim H, Hwang J, Kim SM, Choi J, Yang DS. Risk factor analysis of the development of severe radiation pneumonitis in patients with non-small cell lung cancer treated with curative radiotherapy, with focus on underlying pulmonary disease. BMC Cancer. 17 oct 2023;23(1):992.

Olivier CRAVÉREAU
Docteur Junior
Département d'oncologie radiothérapie
Institut de Cancérologie de Lorraine
Nancy

Dr Jean-Christophe FAIVRE
Responsable du département d'oncologie radiothérapie
Institut de Cancérologie de Lorraine
Nancy

