
Article 1
Une cause atypique d'occlusion digestive
Rana R, Bhattacharya S, Bhattacharya B, Ghimire RK, Joshi N. Isolated visceral manifestation of Buerger's disease presenting as intestinal obstruction: a case report. Ann Med Surg (Lond). 2024 Apr 29;86(6):3770-3775.
Il s'agit du cas d'un patient de 42 ans, fumeur et consommateur d'alcool, admis aux urgences au Népal pour des douleurs abdominales évoluant depuis deux mois, associées à un syndrome subocclusif et à des épisodes de diarrhée parfois glairo-sanglantes. Il avait comme seul antécédent une suspicion d'ischémie transitoire d'un membre inférieur non explorée. L'examen clinique retrouvait une sensibilité épigastrique et plusieurs petits lipomes abdominaux.
Le bilan biologique montrait un taux de CRP à 22 mg/L avec une hémoglobine normale. L'échographie révélait un épaississement pariétal du jéjunum avec une rétrodilatation, confirmés à l'entéro-IRM qui objectivait une sténose segmentaire et circonférentielle du jéjunum associée à des adénomégalies mésentériques.
Devant ce tableau occlusif avec suspicion de maladie de Crohn, une résection-anastomose jéjunale coelioscopique a été réalisée.
L'examen anatomopathologique a révélé une inflammation aiguë et chronique de la muqueuse, une sclérose sous-muqueuse, ainsi qu'une atteinte vasculaire marquée : épaississement pariétal des artérioles avec œdème, fibrose, occlusions multiples et inflammation des vaisseaux. Ces lésions étaient compatibles avec une thromboangéite oblitérante (maladie de Buerger).
Pathologie vasculaire que nous connaissons peu en gastro-entérologie, la thromboangéite oblitérante est plus fréquente en Asie et au Moyen-Orient, touchant principalement des hommes jeunes et fumeurs. Elle a pour conséquence la survenue des ischémies aiguës des extrémités des membres pouvant mener à des amputations. Son mécanisme repose sur une toxicité du tabac entraînant une réaction immunitaire altérant la paroi vasculaire. Aucun traitement curatif n'est défini, mais le sevrage tabagique reste essentiel, permettant une régression des lésions dans 95 % des cas.
Article 2
Une hémostase de cowboy
Wang P, Zhang H, Xu S, Zhang Y, Ma H, Feng J, Wang X, Zhang D. Hemorrhagic Shock Caused by Spontaneous Bleeding from Early Gastric Cancer Was Successfully Cured by Emergency Endoscopic Submucosal Dissection: A Case Report. Clin Med Insights Case Rep. 2024 Aug 27;17:11795476241271552. doi: 10.1177/11795476241271552. PMID: 39206022; PMCID: PMC11350541.
Une patiente de 70 ans consulte aux urgences en Chine pour malaise et méléna évoluant depuis deux mois. Elle est instable sur le plan hémodynamique avec une hémoglobine à 4,1 g/dL.
La gastroscopie met en évidence deux lésions gastriques, une lésion de type 0-Isp (classification de Paris) sur la face postérieure de l'antre et une lésion de type 0-IIa au niveau de l'angulus, avec l'analyse en NBI différente de la muqueuse normale adjacente.
L'écho-endoscopie ne retrouve pas d'atteinte sous-muqueuse, et les biopsies concluent à de la dysplasie de haut grade. Une dissection sous-muqueuse (DSM) est programmée, et la patiente sort sous IPP.
Elle est réhospitalisée peu après pour récidive hémorragique avec méléna. La gastroscopie objective un saignement actif sur la lésion de l'antre. Une DSM en urgence est réalisée en une dizaine de minutes, permettant l'hémostase et, dans la foulée, l'endoscopiste résèque de la lésion de l'angulus par la même technique. L'analyse anatomopathologique conclut à un adénocarcinome bien différencié avec résection R0.
Ce cas l'intérêt de la DSM dans la prise en charge des hémorragies sur lésions néoplasiques précoces, sous réserve d'un bilan d'extension complet et d'un opérateur expérimenté (ici, l'endoscopiste avait plus de 300 DSM gastriques et œsophagiennes à son actif). En effet, les vaisseaux tumoraux, de gros calibre, rendent l'hémostase conventionnelle difficile (clips, coagulation thermique) et peuvent compromettre l'analyse histologique.
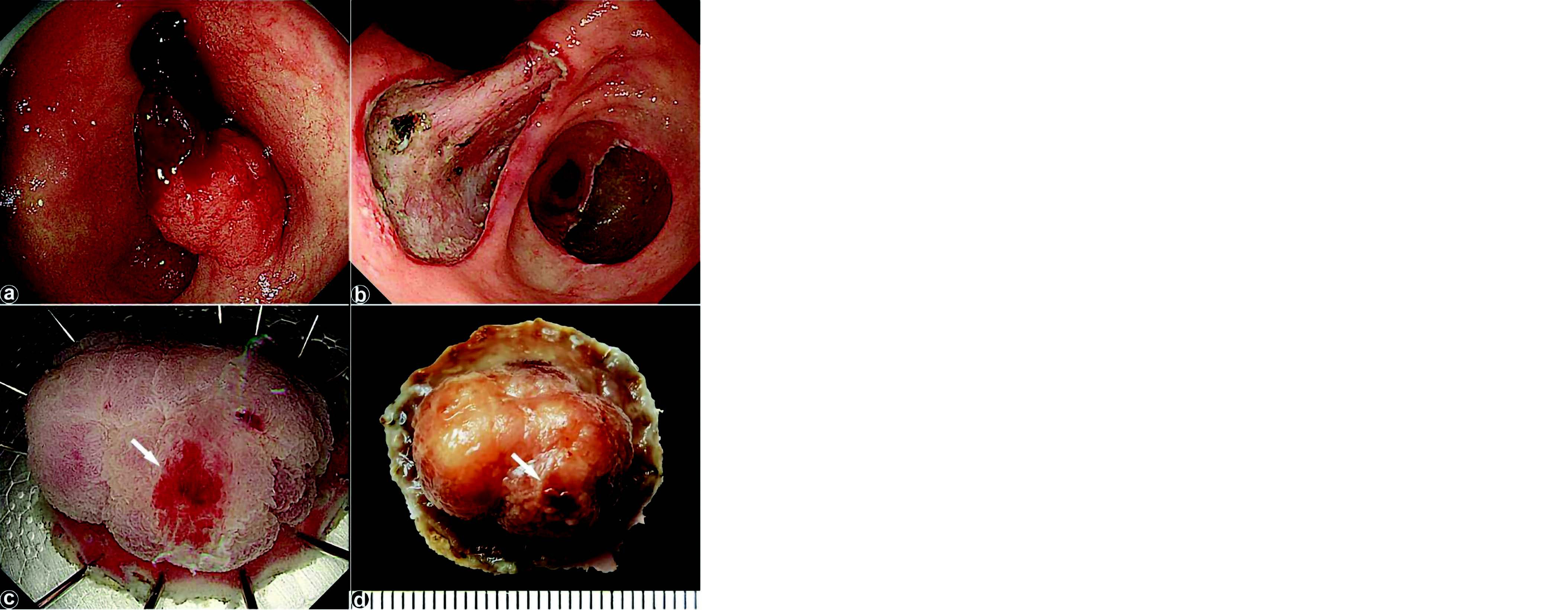
Figure 1 : a) Vision endoscopique de la lésion de l'antre 0-Isp avec caillot adhérent. b) Vision endoscopique directe après résection des deux lésions. c) Pièce opératoire avec vaisseau à l'origine du saignement. d) Pièce après fixation au formol.
Article 3
Quand le foie s'égare
Saglietti C, Fasquelle F, Barcena C, Schmidt S, Shirata C, Uldry E, Halkic N, Sempoux C. Primary hepatocellular carcinoma of the spleen. Pathology. 2024 Jun;56(4):600-601. doi: 10.1016/j.pathol.2023.09.005. Epub 2023 Oct 29. PMID: 37973456.
En Suisse, une patiente de 68 ans, diabétique de type 2 avec syndrome métabolique et antécédents vasculaires (accident ischémique cérébral, ischémie subaiguë du membre inférieur), est prise en charge pour une masse splénique fortuite découverte sur un scanner réalisé dans le bilan de son ischémie. Une IRM de contrôle à 8 mois montre une augmentation volumétrique de 40 %, motivant une splénectomie diagnostique.
L'examen anatomopathologique met en évidence une lésion multinodulaire non encapsulée, avec une prolifération carcinomateuse évoquant un carcinome hépatocellulaire (CHC). L'aspect histologique est frappant : ballonisation cellulaire, corps de Mallory et zones de stéatohépatite tumorale. Pourtant, aucun foyer tumoral n'est retrouvé dans le foie natif à l'IRM et au TEP-Coline. En préopératoire, l'alpha-fœtoprotéine était élevée (5 027 kU/L), chutant à 3 kU/L après splénectomie.
Une entité exceptionnelle : le carcinome hépatocellulaire sur foie ectopique splénique. Le foie ectopique, bien que rare (0,47 % des laparoscopies sur 1 046 cas), est décrit préférentiellement au niveau de la vésicule biliaire, mais d'autres localisations, dont la rate, ont été rapportées. Comme le foie natif, il est soumis aux mêmes agressions métaboliques et peut évoluer vers un CHC.
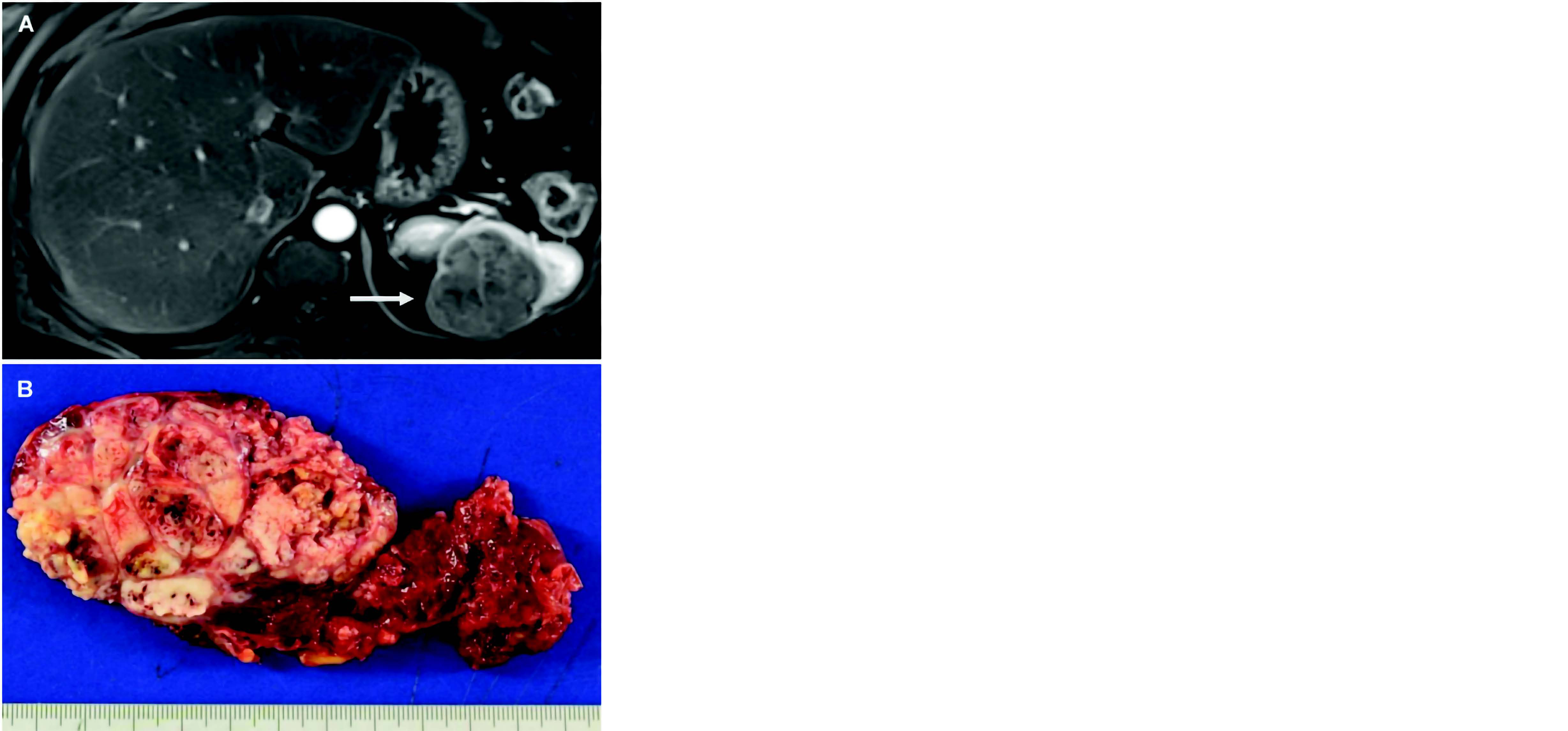
Figure 2 : A – IRM abdominale en coupe transversale en séquence T1 après injection de gadolinium montrant la lésion splénique hypointense. B – Pièce opératoire de splénectomie vaec une lésion polylobée, focalement hémorragique avec parenchyme splénique congestif
Article 4
Quand le microbiote vous saoule
Zewude RT, Croitoru K, Das R, Goldman B, Bogoch II. Auto-brewery syndrome in a 50-year-old woman. CMAJ. 2024 Jun 2;196(21):E724-E727. doi: 10.1503/cmaj.231319. Erratum in: CMAJ. 2024 Jul 1;196(24):E831. doi: 10.1503/cmaj.240839. PMID: 38830676; PMCID: PMC11142034.
Une patiente américaine de 50 ans consulte à plusieurs reprises les urgences sur deux ans pour somnolence inexpliquée, des troubles de l'élocution et une odeur d'alcool. L'éthanolémie est systématiquement élevée (1,8 g/L), mais la patiente nie toute consommation d'alcool, et son entourage le confirme. Bilan hépatique normal, imagerie cérébrale et abdominale sans anomalie, trois avis psychiatriques concluant à une intoxication éthylique avec déni des consommations.
Un médecin urgentiste finit par suspecter un syndrome d'auto-brasserie, pathologie rare où le microbiote entraîne une fermentation des glucides en éthanol. Une cure de FLUCONAZOLE améliore franchement les symptômes de la patiente. Pourtant, les cultures fongiques digestives restent négatives. Un régime pauvre en glucides et des probiotiques (Lactobacillus acidophilus) permettent une rémission de six mois. Le test au glucose est négatif, validant la guérison, et la patiente réintroduit progressivement les glucides.
Ce syndrome, décrit pour la première fois au Japon en 1952, implique principalement Saccharomyces cerevisiae et certaines espèces de Candida. Les facteurs favorisants incluent le diabète, les maladies hépatiques, les maladies inflammatoires chroniques de l'intestin et certaines prédispositions génétiques. Aucun algorithme diagnostique standardisé n'existe, mais une ingestion de glucose suivie d'un dosage de l'éthanolémie peut être informative.
Comme quoi, les patients ne mentent pas toujours…
Article 5
L'hémobilie, ou l'épistaxis des voies biliaires ?
Chiang CM, Chiang HC, Chiu HC. An Uncommon Cause of Hemobilia. Gastroenterology. 2024 Aug;167(3):e5-e8. doi: 10.1053/j.gastro.2024.01.024. Epub 2024 Jan 20. PMID: 38253186.
Une patiente de 58 ans consulte pour des douleurs abdominales associées à un ictère. L'examen retrouve une sensibilité de l'hypochondre droit et l'interrogatoire révèle des épistaxis récidivantes depuis l'âge de 40 ans, avec des antécédents similaires chez son père.
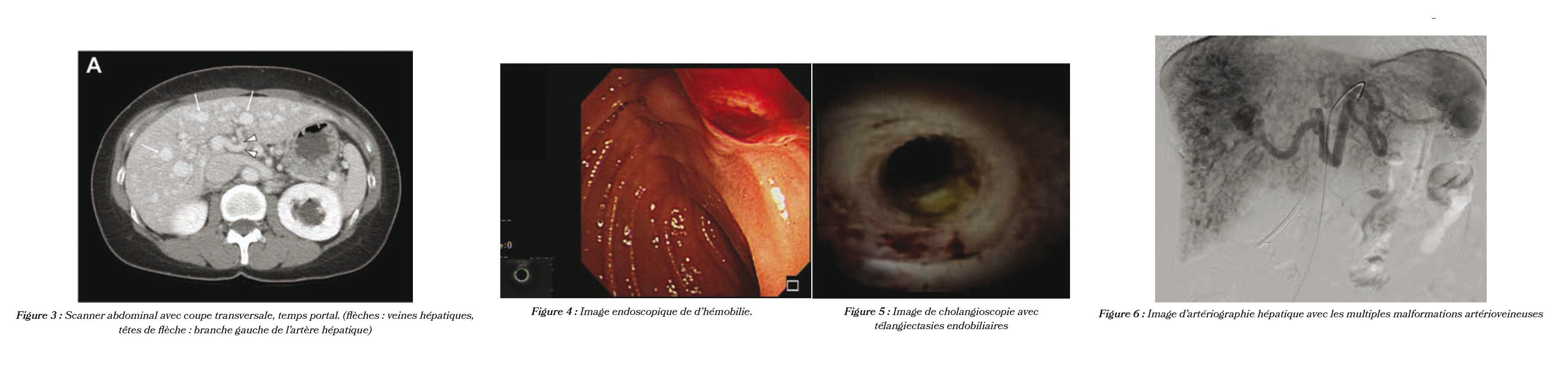
Le bilan montre une cytolyse hépatique (ASAT 193 UI/L), une bilirubine augmentée à 46 µmol/L, mais pas de syndrome inflammatoire ni d'anémie. Le scanner ne retrouve pas de lithiase ni de dilatation des voies biliaires, mais met en évidence une tortuosité des artères hépatiques, des shunts artérioportes, une veine porte dilatée et une opacification précoce des veines hépatiques, traduisant une redistribution vasculaire hépatique et peut-être une hypertension portale non cirrhotique (figure 3).
À la CPRE, on constate une hémobilie spontanée (figure 4). La cholangioscopie révèle des télangiectasies biliaires (figure 5). L'évolution est spontanément favorable et le diagnostic de télangiectasies hémorragiques héréditaires (THH), ou maladie de Rendu-Osler, est retenu.
La maladie de Rendu-Osler est une maladie autosomique dominante caractérisée par des malformations vasculaires cutanéo-muqueuses et viscérales. Son diagnostic repose sur les critères de Curaçao : épistaxis spontanées et répétées, télangiectasies cutanéo-muqueuses, atteinte viscérale (digestive, hépatique, pulmonaire, cérébrale), antécédents familiaux au premier degré.
L'atteinte hépatique est surtout celle d'une hypertension portale non cirrhotique sur les malformations artério-veineuses et une cholangite ischémique liée au vol vasculaire intra-hépatique menant à une cirrhose biliaire secondaire. Les télangiectasies biliaires sont une manifestation rare et méconnue de la maladie.
Le traitement repose sur l'acide tranexamique (épistaxis, saignements digestifs) et le bévacizumab en seconde ligne. En cas d'hémobilie sévère, la coagulation par plasma argon ou une embolisation artérielle peuvent être envisagées (en cas de choc hémorragique). La transplantation hépatique peut parfois être nécessaire lorsqu'il existe de fistules artério-veineuses avec retentissement cardiaque.
Article 6
De toutes façons, ça finit toujours par des corticoïdes…
Saad E, Agab M, Ozcekirdek EC, Awadelkarim A, Idris I. The Diagnostic Dilemma of Acute Granulomatous Hepatitis in a Patient With Crohn's Disease: A Case Report and Review of Literature. J Investig Med High Impact Case Rep. 2022 Jan-Dec;10:23247096211069764. doi: 10.1177/23247096211069764. PMID: 35343257; PMCID: PMC8966121.
Une patiente de 35 ans, atteinte de maladie de Crohn mais sans traitement depuis cinq ans, arrive en soins intensifs en état de choc : fièvre, hypotension, tachycardie, douleurs abdominales diffuses. Le bilan retrouve une pancytopénie, une insuffisance rénale aiguë, une hypercalcémie, des ALAT et des PAL légèrement augmentées, avec une bilirubine normale. Le scanner montre une cholécystite alithiasique modérée. Une cholécystectomie réalisée, et ne retrouve pas de calcul enclavé à la cholangiographie peropératoire. Mais après l'intervention, les perturbations du bilan hépatique s'aggravent, la bilirubine monte à 100 µmol/L.
La CPRE ne retrouve pas d'obstacle biliaire. Les sérologies virales sont négatives. Les anticorps anti-tissu hépatiques sont négatifs, pas d'argument pour une vascularite à ANCA, le dosage pondéral des immunoglobulines est normal, il n'y a pas de surcharge en cuivre ou en fer. L'hépatologue réalise une biopsie hépatique. L'analyse anatomopathologique conclut à une hépatite granulomateuse sans nécrose caséuse.
Les principales causes d'hépatite granulomateuse sont infectieuses : bactériennes (tuberculose, brucellose, bartonellose, fièvre Q, coccidiose), certains virus et levures. Les causes peuvent être médicamenteuses ou toxiques. La sarcoïdose fait partie des diagnostics différentiels, mais le scanner thoracique et le taux enzyme de conversion de l'angiotensine sont normaux, l'hypercalcémie est résolutive après normalisation de la fonction rénale et il n'y a pas de franc déséquilibre phosphocalcique. De plus il existe des hépatites granulomateuse liée à la maladie inflammatoire chronique de l'intestin, et en particulier la maladie de Crohn (moins de 1 % des patients), qui peut survenir sans corrélation avec l'activité de l'atteinte digestive.
En revanche, la sarcoïdose et la maladie de Crohn, partageant des mécanismes inflammatoires communs, peuvent très rarement être associés.
Au final, après avoir éliminé les causes infectieuses et médicamenteuses, la prise en charge reste la même : corticothérapie. L'amélioration est rapide. En deux mois, le bilan hépatique se normalise. En cas de corticodépendance, un traitement immunomodulateur par AZATHIOPRINE aurait été proposé, et en l'absence de réponse, un traitement par anti-TNFalpha aurait été discuté. Et ce, quelle que soit l'étiologie retenue…
Et un petit dernier pour la route...
Article 7
Une cause de pancréatite aiguë à faire réciter aux externes
Sajjad, Erum & Sami, Sumayya & Khanum, Iff at. (2025). Coral snake envenomation induced acute pancreatitis. The Egyptian Journal of Internal Medicine. 37. 10.1186/s43162-025-00413-0.
Une patiente pakistanaise de 20 ans est mordue au poignet par un serpent corail et reçoit un sérum antivenimeux dans son village. Quatre jours plus tard, elle consulte aux urgences pour un ptosis bilatéral, une faiblesse musculaire et une dyspnée.
Le tableau neurologique, évocateur d'une neurotoxicité liée au venin, est traité par néostigmine et sérum anti-venin avec une bonne amélioration.
Mais au quatrième jour d'hospitalisation, elle développe des douleurs abdominales avec une lipase significativement augmentée. Le scanner ne montre ni infiltration pancréatique ni coulée de nécrose, suggérant une pancréatite aiguë modérée. Il n'y avait d'argument pour une cause lithiasique, ni alcoolique.
Bien que rare, une pancréatite induite par le venin de serpent est décrite dans la littérature, possiblement liée à la présence de phospholipase A2, induisant une lyse cellulaire et pourrait affecter les glandes pancréatiques.
La prise en charge repose sur une réhydratation IV, un traitement antalgique mais aussi surtout sur l'administration de sérum anti-venin. L'évolution est rapidement favorable.
Relecture par Dr Théo IZOPET

FILALI-ANSARY Zakia
CHU Toulouse

