Se référer aux procedures du service - Ce domaine est en pleine expansion. Nous avons utilisé les derniers consensus datant de 2022 (CAR-T) et 2024 (bispécifiques), veuillez vérifier l'absence de recommandation plus récente.
Syndrome de relargage cytokinique
Définition
Le syndrome de relargage cytokinique (CRS) résulte de l'activation des CAR-T qui entraîne la libération de cytokines effectrices (intérferon-ɣ, TNF-ɑ, Interleukine (IL)-2) qui peuvent déclencher la libération de cytokines pro-inflammatoires (IL-1, IL-6, IFN-ɣ, IL-10 et la protéine chimioattractante monocytaire 1 (MCP1)), avec une augmentation de la protéine C-réactive (CRP) et de l'hyperferritinémie.
Les facteurs de risque de CRS de haut grade comprennent la charge tumorale, une infection concomitante, la dose de CAR-T et le type de CAR T (Axicabtagène ciloleucel inférieur à Tisagenlecleucel dans le lymphome) et le type de conditionnement de lymphodéplétion.
Prévention
Aucune prophylaxie n'est validée. L'administration précoce et prophylactique du Tocilizumab a été étudiée dans le SRC mais les données sont insuffisantes à ce jour pour le recommander en systématique.
Clinique
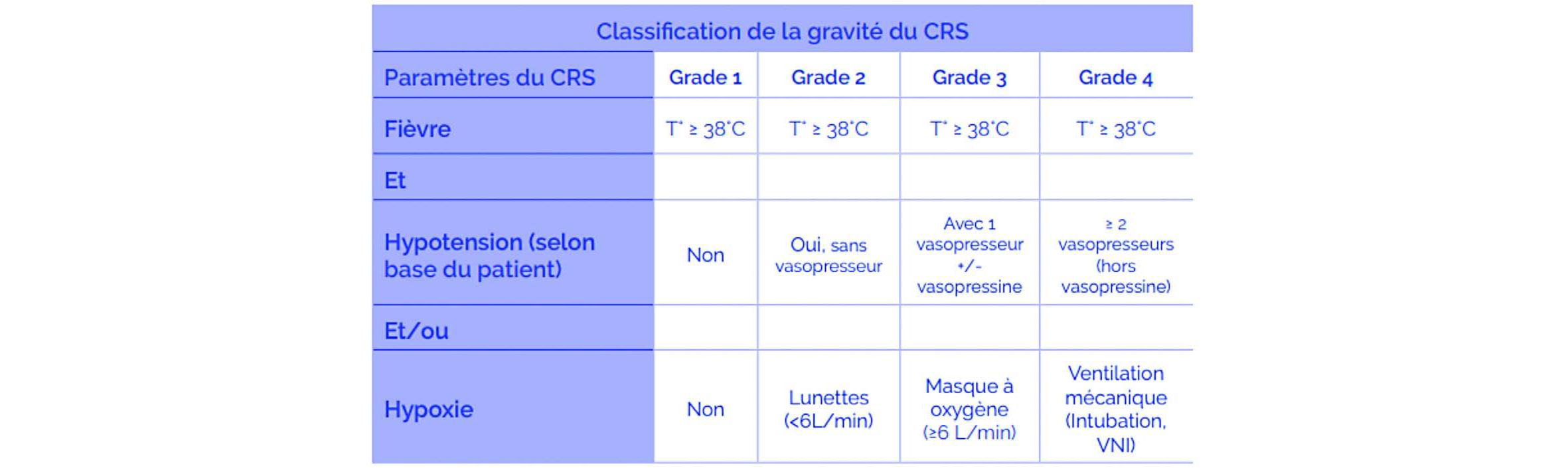
Le CRS survient entre J1 et J28, particulièrement entre J1 et J7. Les formes précoces sont associées à des formes plus sévères. L'apparition des symptômes est progressive et débute habituellement par de la fièvre, secondée fréquemment par une hypotension, un syndrome de fuite capillaire (hypoxémie) et/ou des défaillances d'organes (arythmie, insuffi- sance cardiaque, coagulopathie, insuffisance rénale, cytolyse hépatique et/ou épanchements pleuraux). Une classification de sévérité est proposée par le consensus de l'ASCT (Tableau ci-dessous). Les défaillances d'organes ne rentrent pas en compte dans cette classification.
Le grade de CRS est défini par l'évènement le plus sévère.
Traitement
Pour les CAR T-cells
Une prise en charge précoce est essentielle face au risque de dégradation rapide en cas d'errance diagnostique. Discussion obligatoire avec un chef et/ou le réanimateur pour définir la prise en charge optimale. Un résumé des thérapeutiques licites est présent dans la Figure page suivante (Recommandations EBMT 2022).
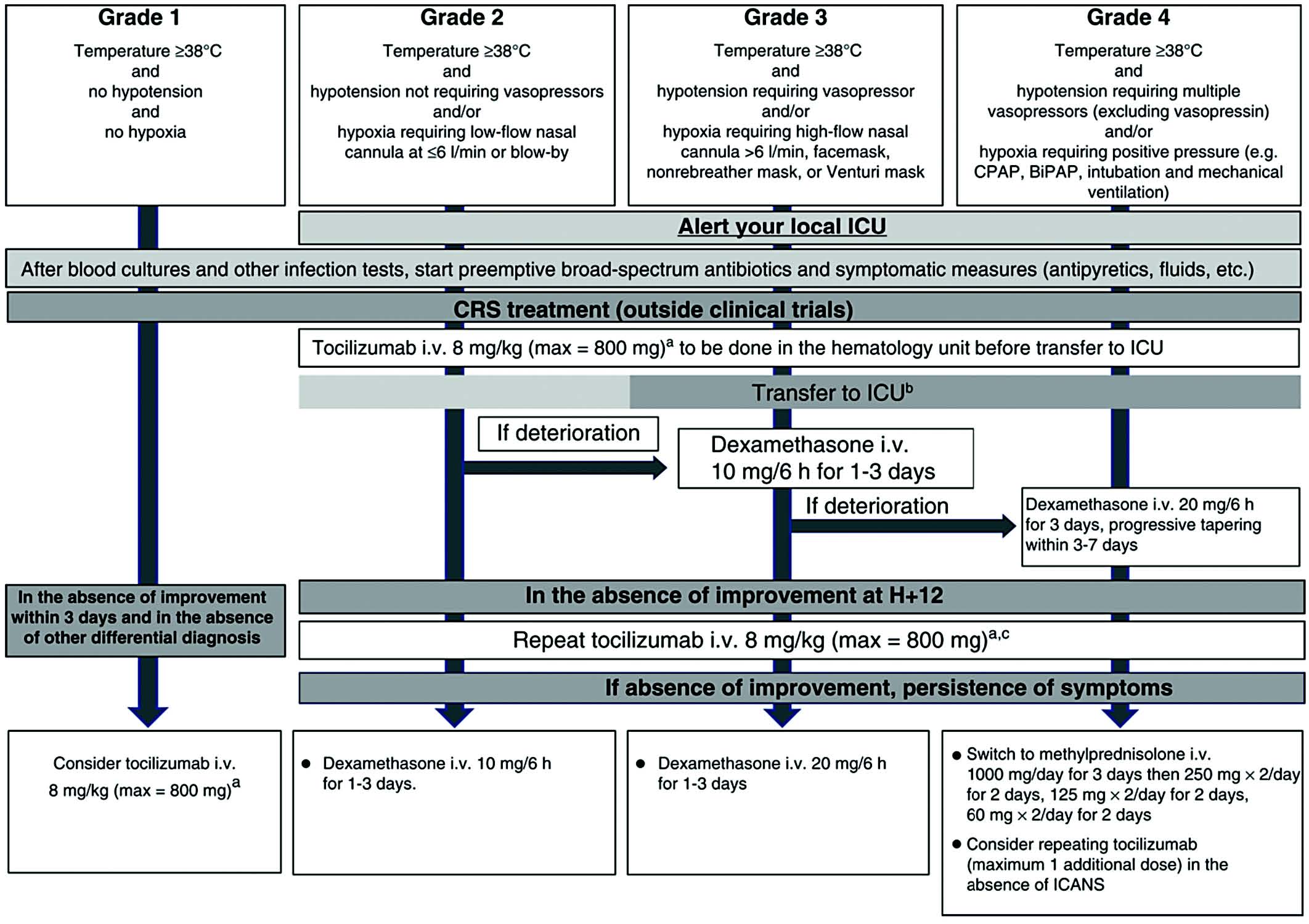
*Patient neutropénique au moment sur CRS : antibiothérapie large spectre selon les critères usuels (antibiothérapie actuelle, écologie du patient et du service, manifestations cliniques, ...).
La réponse est définie par la régression des signes cliniques du CRS. L'obtention de l'apyrexie est rapide sous tocilizumab ou corticoïdes. Les autres signes cliniques s'amendent plus lentement.
Pour les anticorps bi-spécifiques
Selon les recommandations internationales :
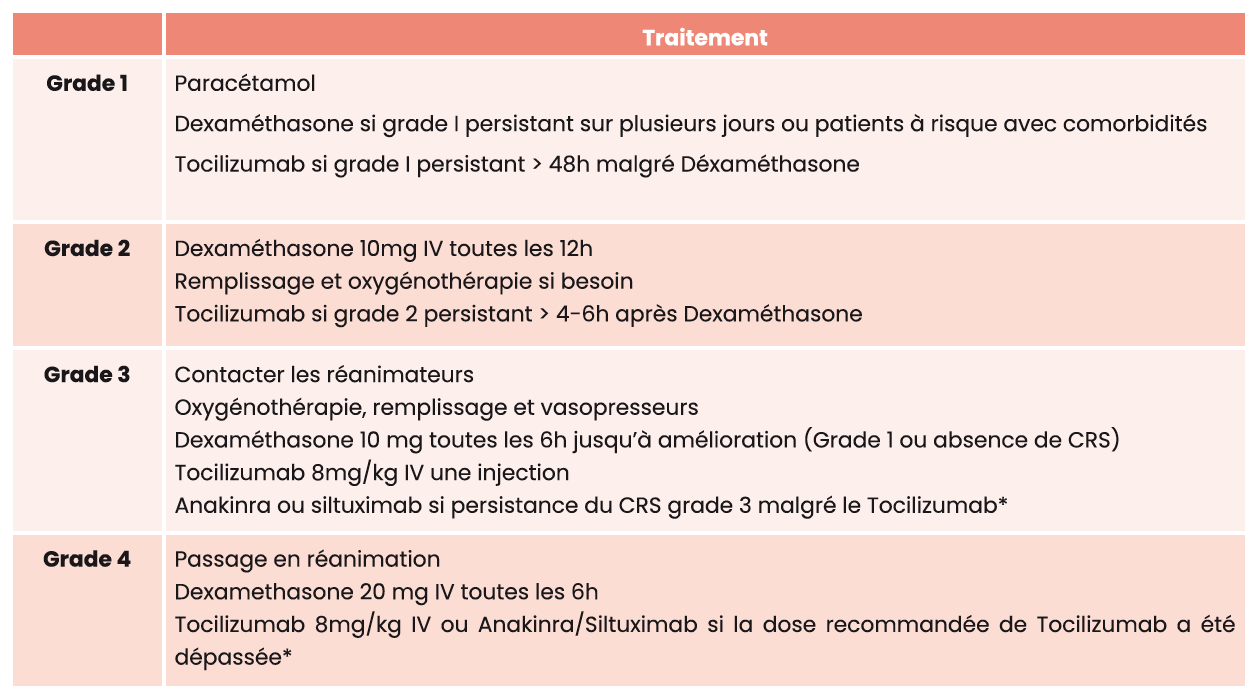
*Le Tocilizumab ne doit pas être administré > 2 fois par CRS (à au moins 8h d'intervalles) et ne devrait pas dépasser 3 administrations sur une période de 6 semaines.
Neurotoxicité
Définition
La neurotoxicité, ou ICANS (Immune effector cell-associated neurotoxicity syndrome) s'associe régulièrement de CRS mais peut également survenir de façon distincte (souvent en 2nd temps, plus rarement avant le CRS). La physiopathologie de l'ICANS est probablement due à une combinaison de cytokines inflammatoires augmentant la perméabilité vasculaire, à l'activation endothéliale conduisant à la rupture de la barrière hémato-encéphalique, à l'augmentation des cytokines du liquide céphalo-rachidien et dans certains cas conduit à un œdème cérébral.
Prévention
Une expansion plus importante des CAR-T et plus précoce in vivo est en corrélation avec un risque plus élevé d'ICANS dans des études de pharmacocinétique. Les facteurs de risque d'ICANS de grade inférieur à 3 comprennent la dose de CAR-T et le type des CAR-T (domaine de costimulation CD28 : Axicab
tagene ciloleucel, Brexucabtagene autoleucel), des comorbidités multiples et notamment des antécédents neurologiques, un taux de plaquettes faible et un CRS de haut grade précoce. Une fièvre élevée inférieure à 38.9 avec une instabilité hémodynamique dans les 36h après réinjection des CAR T-cells permet de prédire un ICANS sévère avec une sensibilité élevée.
Clinique
• Les signes précoces de neurotoxicité sont des tremblements, la dysgraphie, les difficultés de communication orale (dénomination d'objets, tentative de dialogues monosyllabiques, discours inintelligible et/ou persévérations) pouvant rapidement évoluer en aphasie complète, en troubles de l'attention, en apraxie ou en léthargie.
• Les céphalées sont non spécifiques et sont fréquemment associées à la fièvre. - Des déficits moteurs ou des autres fonctions supérieures sont également décrits.
• L'obnubilation initiale peut évoluer en coma, parfois en association à des crises convulsives subcliniques ou cliniques (importance du suivi par EEG).
• Selon les signes cliniques, des diagnostics différentiels doivent être évoqués : hémorragie, HTA maligne, insuffisance hépatique, infection, AVC, localisation spécifique de l'hémopathie.
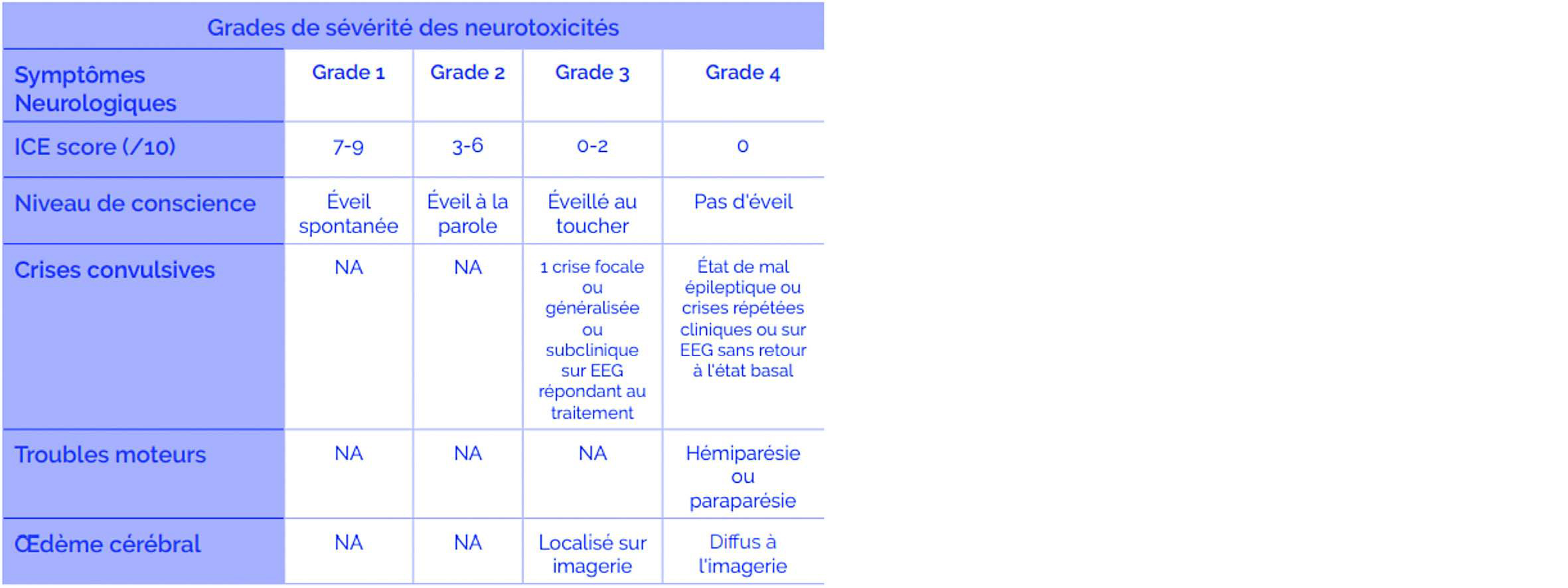
• Un bilan complet doit être réalisé : imagerie cérébrale, EEG et ponction lombaire. La classification de sévérité se fait selon le score ICE (sur 10 points).
• Il faut rechercher des symptômes en faveur d'un œdème cérébral (grade 4) : flou visuel, céphalées, paralysie du VI, vomissements en jet, œdème papillaire, triade de Cushing (hypertension, bradycardie et dépression respiratoire), signe de décérébration ou de décortication.
Score ICE sur 10 points
Orientation : Orienté sur l'année, le mois, la ville et l'hôpital (4 points).
Description : Habilité à nommer 3 objets (exemple : horloge, stylo, bouton) (3 points).
Suivre les ordres : Capacité à suivre des ordres simples (exemple « Montrez-moi 2 doigts » ou « fermez les yeux et tirez la langue ») (1 point).
Écriture : Capacité à écrire une phrase contenant un sujet, un verbe et un complément (exemple : Le chat est gris).
Attention : Capacité de réaliser des soustractions de 10 unités à partir de 100 jusqu'à atteindre 0 (1 point).
Traitement
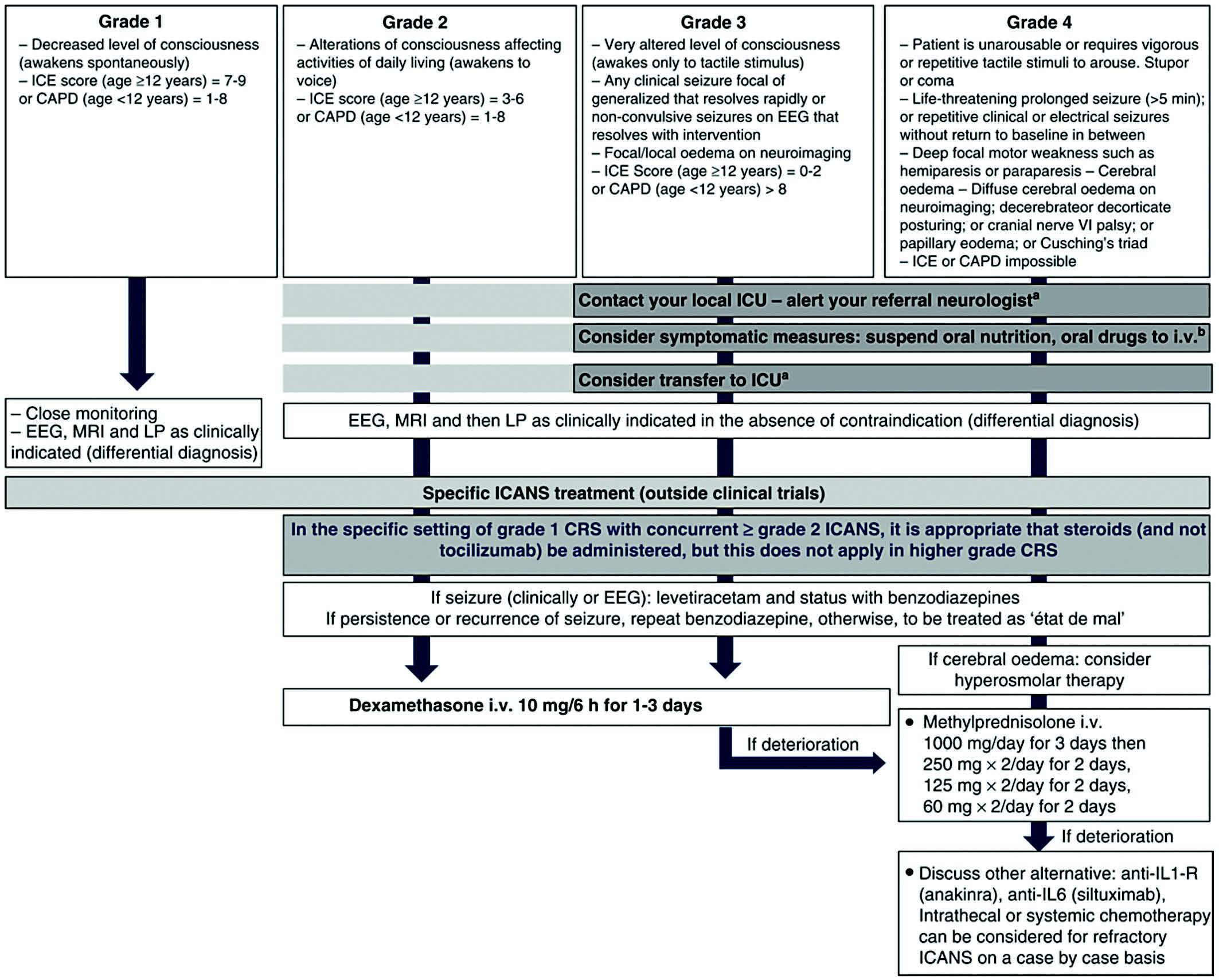
Pour les CAR T-cells
Une prise en charge précoce est essentielle face au risque de dégradation rapide en cas d'errance diagnostique. Discussion obligatoire avec un chef et/ou le réanimateur pour définir la prise en charge optimale. Un résumé des thérapeutiques licites est présent dans la Figure page suivante (Recommandations EBMT 2022).
Pour les anticorps bi-spécifiques
Selon les recommandations internationales :


Dr Raphaël LIÉVIN
Hématologue et étudiant en thèse de science à l'Institut Imagine, Paris
Relecture
Dr Roberta DI BLASI
Hématologue à l'hôpital Saint-Louis
Bibliographie
Lee DW, Santomasso BD, Locke FL, et al. ASTCT Consensus Grading for Cytokine Release Syndrome and Neurologic Toxicity Associated with Immune Effector Cells. Biol. Blood Marrow Transplant. 2019;25(4):625–638. Yakoub-Agha I, Moreau A-S, Ahmad I, et al.
Hayden PJ, Roddie C, Bader P, Basak GW, Bonig H, Bonini C, Chabannon C, Ciceri F, Corbacioglu S, Ellard R, Sanchez-Guijo F, Jäger U, Hildebrandt M, Hudecek M, Kersten MJ, Köhl U, Kuball J, Mielke S, Mohty M, Murray J, Nagler A, Rees J, Rioufol C, Saccardi R, Snowden JA, Styczynski J, Subklewe M, Thieblemont C, Topp M, Ispizua ÁU, Chen D, Vrhovac R, Gribben JG, Kröger N, Einsele H, Yakoub-Agha
I. Management of adults and children receiving CAR T-cell therapy: 2021 best practice recommendations of the European Society for Blood and Marrow Transplantation (EBMT) and the Joint Accreditation Committee of ISCT and EBMT (JACIE) and the European Haematology Association (EHA). Ann Oncol. 2022
Mar;33(3):259-275. doi: 10.1016/j.annonc.2021.12.003. Epub 2021 Dec 16. PMID: 34923107.
Cornillon J, Hadhoum N, Roth-Guepin G, et al. Prise en charge pratique d'une encéphalopathie liée au traitement par cellules CAR-T chez l'adulte et l'enfant : recommandations de la Société francophone de greffe de moelle et de thérapie cellulaire (SFGM-TC). Bull. Cancer (Paris). 2019;S0007455119302243.
Crombie JL, GraffT, Falchi L, Karimi YH, Bannerji R, Nastoupil L, Thieblemont C, Ursu R, Bartlett N, Nachar V, Weiss J, Osterson J, Patel K, Brody J, Abramson JS, Lunning M, Shah NN, Ayed A, Kamdar M, Parsons B, Caimi P, Flinn I, Herrera A, Sharman J, McKenna M, Armand P, Kahl B, Smith S, Zelenetz A, Budde LE, Hutchings M, Phillips T, Dickinson M. Consensus recommendations on the management of toxicity associated with CD3×CD20 bispecific antibody therapy. Blood. 2024 Apr 18;143(16):1565-1575. doi: 10.1182/blood.2023022432. PMID: 38252906.

