Interview du Pr Pierre CATTAN

Chef de service de chirurgie digestive à l'Hôpital Saint-Louis
Propos recueillis par Eloïse Papet & Quentin Rodriguez
Eloïse Papet & Quentin Rodriguez.– Bonjour monsieur le Professeur Cattan, nous vous remercions d'avoir accepté de répondre à notre interview pour le journal le Digest'Times avec pour sujet dans cet article : la prise en charge des ingestions de caustiques.
Alors tout d'abord, d'après vous qu'est-il important de noter à l'arrivée d'un patient ayant ingéré un produit caustique ?
Pr Pierre Cattan.– Bonjour Quentin, bonjour Eloïse. Alors la première chose à faire à l'arrivée d'un patient ayant ingéré un produit caustique est d'évaluer la gravité de la situation.
Dans de nombreux cas, l'ingestion n'aura pas de conséquences pour le patient, alors que parfois il y aura une nécrose tissulaire menaçant le pronostic vital et nécessitant une chirurgie d'exérèse en urgence. Dans les cas intermédiaires il n'y aura pas d'indication chirurgicale initiale, mais surviendront des séquelles, principalement à type de sténose de l'oesophage.
Il faut savoir qu'environ 10 % des patients auront une prise en charge chirurgicale d'emblée, 30 % auront un traitement conservateur, mais auront des séquelles et 60 % n'auront aucune conséquence de l'ingestion.
Dans une étude récente du PMSI, 89 % des patients ont bénéficié d'un traitement non opératoire et 11 % d'une chirurgie (1).
Lors de l'arrivée du patient, il existe deux risques de décès précoce :
• La défaillance respiratoire : soit par obstruction laryngée (rare mais gravissime, nécessitant une trachéotomie en urgence), soit par inhalation du produit caustique (qui entraîne un oedème lésionnel alvéolaire) ;
• La perforation digestive responsable d'une péritonite caustique (complication rare (inférieur 0,5 %), mais responsable d'une mortalité proche de 100 %) (2).
Il convient d'interroger le patient sur le produit et la quantité ingérée. Le centre antipoison est appelé systématiquement pour avoir des renseignements quant à une possible toxicité systémique du produit ingéré, responsable de troubles hydro-électrolytiques majeurs (hypocalcémie par chélation).
Deux catégories de produits peuvent être ingérés : lesagents corrosifs, comme les acides forts (pH inférieur 1) ou les bases fortes (Destop, Javel non diluée), qui entraînent une nécrose tissulaire, pourvoyeurs des indications de chirurgie en urgence. Pour avoir un ordre d'idée, un verre à moutarde de Destop aura des conséquences graves.
Les agent irritant (eau de Javel diluée) dont l'ingestion n'entraîne pas de nécrose tissulaire et le risque pour le patient est faible.
Pour la prise en charge initiale, il faut éviter toute manipulation qui peut favoriser des vomissements ou des régurgitations du produit caustique, compte tenu du risque d'inhalation caustique gravissime : décubitus dorsal, sonde naso-gastrique, lavage gastrique.
Il est important de savoir qu'il n'existe pas de corrélation entre l'état clinique du patient à l'arrivée et la gravité de l'atteinte tissulaire. Il convient donc de réaliser systématiquement et rapidement le bilan lésionnel.
Bilan initial :
• Gravité situation – maintenir homéostasie patient.
• Enquête : produit ingéré et quantité (centre antipoison).
• Bilan lésionnel rapide
E. P. & Q. R.– Merci pour votre réponse. Quel est donc le bilan lésionnel à réaliser ?
Pr P. C.– L'examen clé dans l'évaluation des conséquences des ingestions de caustiques est la TDM cervico-thoraco- abdomino-pelvienne sans injection et avec injection de produit de contraste (temps d'acquisition 90s), à réaliser dans un délai de 3 à 6h (en pratique souvent après 6h selon l'arrivée du patient) après l'ingestion.
Le but de cet examen est d'évaluer l'existence d'une nécrose transmurale de l'oesophage et de l'estomac.
Il n'y a plus de place pour l'endoscopie en urgence, car elle est beaucoup moins performante que la TDM pour remplir cet objectif (3).
Une fois le scanner réalisé, nous sommes capables d'évaluer le grade de l'atteinte et l'attitude thérapeutique qui en découle.
Sur le plan oesophagien, les lésions ont été classées en 4 grades de sévérité croissante.
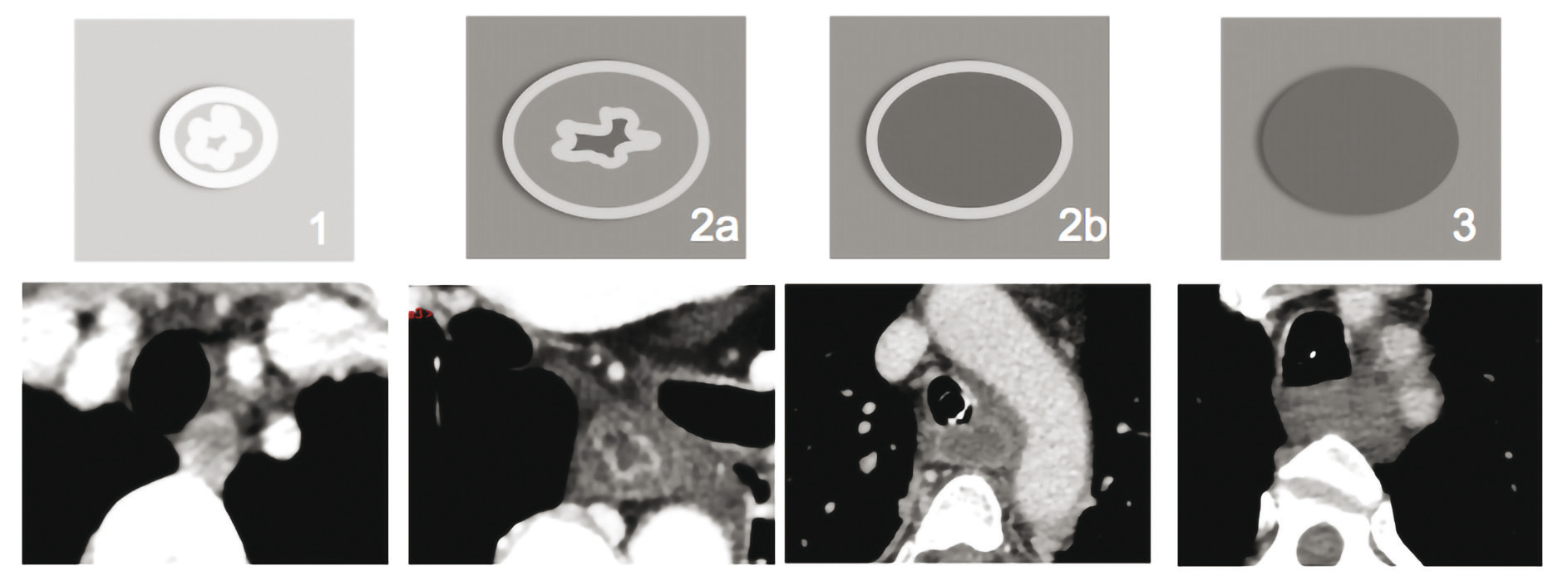
• Le stade I correspond à un œsophage normal, +/- oedème discret.
• Le stade IIa correspond à une prise de contraste en cocarde, qui correspond à un important oedème de la paroi, mais avec préservation de la vascularisation de la sous-muqueuse inflammatoire, mais pas complètement nécrosée et en externe une musculeuse rehaussée.
Le stade IIa évolue vers la sténose dans 20 % des cas (4).
• Le stade IIb correspond à une prise de contraste de la musculeuse uniquement, avec un oesophage dilaté.
Il existe une infiltration de la graisse péri-oesophagienne. Le risque de sténose oesophagienne est évaluée à plus de 80 % (4).
• Le stade III correspond à la nécrose transmurale avec absence de prise de contraste de la paroi de l'oesophage, localisée ou étendue et doit conduire à une prise en charge chirurgicale d'emblée.
Il faut savoir que l'oesophage est souvent difficile à analyser en arrière des veines pulmonaires.
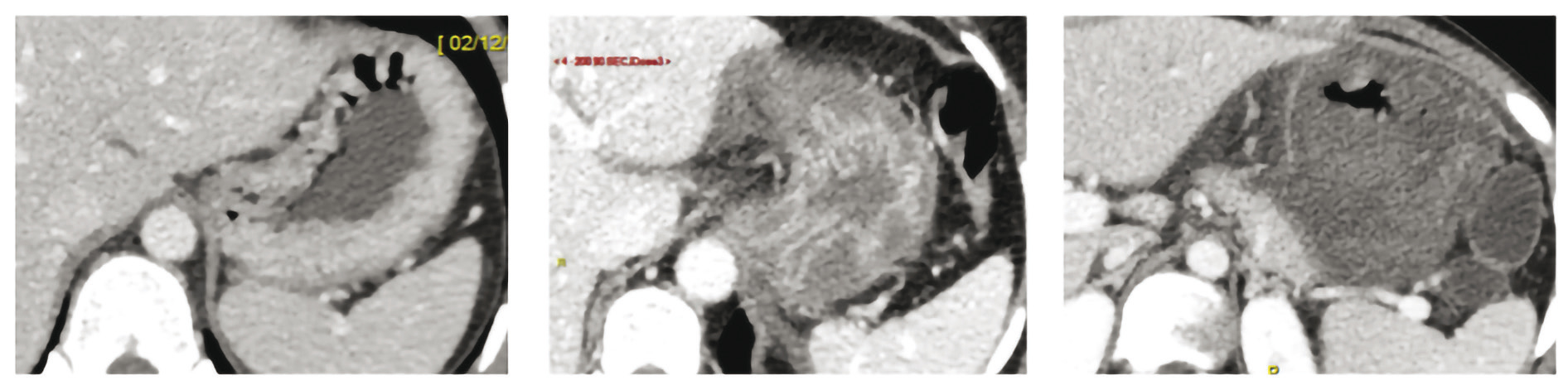
Sur le plan gastrique, les lésions ont été classées en 3 grades de sévérité.
• Le stade I est un estomac normal.
• Le stade II est caractérisé par un oedème pariétal avec prise de contraste conservée sans discontinuité.
• Le stade III révèle l'absence de prise de contraste pariétale localisée ou étendue, souvent prédominante au niveau de la face postérieure de la grosse tubérosité. Elle doit conduire à une prise en charge chirurgicale en urgence devant le risque de péritonite caustique par perforation gastrique.
On peut noter deux « astuces » dans la prise en charge :
• L'existence d'un stade III oesophagien sans stade III gastrique est exceptionnelle.
• Il n'existe pas non plus de stade III du 1/3 supérieur de l'œsophage suspendu sans stade III du bas oesophage.
E. P. & Q. R.– Suite au bilan lésionnel, en cas de stades III quel traitement chirurgical est adéquat en urgence ?
Pr P. C.– Le risque évolutif, sans prise en charge chirurgicale, de la nécrose oesophagienne transmurale est la nécrose trachéale de contiguïté ; pour l'estomac nécrosé, la péritonite caustique est quasi-systématiquement mortelle. Le but est donc de ne pas perdre de temps sur la prise en charge chirurgicale en urgence pour l'exérèse des structures faisant l'objet d'une nécrose transmurale.
Il faudra réaliser une fibroscopie trachéo-bronchique systématique en cas d'oesophagectomie envisagée.
L'apparition de signes de nécrose de la trachée (souvent postérieure/ gauche) contre-indique la réalisation oesophagectomie par stripping.
Les possibilités chirurgicales sont :
• L'oesogastrectomie totale (OGT) avec stripping de l'oesophage (si absence de nécrose trachéale). Patient en décubitus dorsal, les deux bras le long du corps. On réalisera pour cela un abord cervical et une laparotomie.
• L'oesogastrectomie totale (OGT) sans stripping de l'oesophage (si présence d'un patch de nécrose trachéale). On réalisera une thoracotomie pour une dissection oesophagienne prudente et un patch pulmonaire sur la trachée pour la réparation trachéale (5).
• La gastrectomie totale (GT) avec anastomose oeso-jéjunale, s'il n'existe pas de grade III oesophagien.
L'oesophage apparaît brûlé dans la plupart des cas dans sa portion distale, mais s'il saigne à la section, l'anastomose oeso-jéjunale peut être réalisée. Il persiste un risque de sténose oesophagienne secondaire, mais qui pourra être traitée par dilatation (6). Cette anastomose oesogastrique étant à haut risque de fistule, il convient d'en réaliser un drainage adéquat : drain thoracique trans-hiatal et lame de Delbet sur le moignon duodénal.
En cas de nécrose étendue au colon transverse associée à la nécrose oesogastrique, une colectomie peut être réalisée. Celle-ci ne majore pas la mortalité postopératoire, mais peut compromettre les possibilités de reconstruction ultérieure par coloplastie.
Lorsque la nécrose s'étend au second duodénum, une DPC doit être envisagée, augmentant la mortalité à 30-40 % (versus 5 % en l'absence de DPC). Les anastomoses pancréatico et bilio-digestives doivent être réalisées dans le même temps (6).
Lorsque la nécrose digestive s'étend à plus de la moitié du grêle, aucune résection ne sera pas réalisée, compte tenu des chances très limitées de survie.
Quelques points auxquels il faut porter attention : essayer de ne pas léser le récurrent lors de l'abord cervical puisque cela conditionnera les résultats fonctionnels après reconstruction.
Lors du stripping de l'oesophage, il ne faut pas avoir peur des saignements médiastinaux, qui sont inexistants si l'oesophagectomie est réalisée à bon escient. Il faut bien veiller à la mise en place d'une jéjunostomie d'alimentation, et un drainage optimal du médiastin postérieur par le hiatus et du moignon duodénal en fin d'intervention.
E. P. & Q. R.– Ok donc le but à la phase initiale est de ne pas retarder le délai de prise en charge au bloc opératoire si celle-ci est indiquée.
Quelle est la prise en charge du patient au décours de l'évaluation initiale ?
Pr P. C.– Alors, le patient va nécessiter différents soins lors de sa prise en charge en hospitalisation :
• Après oesogastrectomie, la prise en charge initiale a lieu en réanimation.
• Une évaluation psychiatrique quasi-systématique est nécessaire car la plupart des ingestions par accident conduisent à des brûlures graves. Ce sont essentiellement des Tentatives de Suicide (TS).
• Une évaluation ORL en cas de signes ORL.
• Une réalimentation précoce en l'absence de résection digestive, dès J1 si le patient est capable d'avaler. Les formes peu sévères se réalimenteront facilement et un retour au domicile pourra être envisagé rapidement (sous réserve de l'évaluation psychiatrique). Pour ce qui est des formes plus sévères (Iia et IIb), ce sont souvent des lésions de l'hypopharynx qui empêchent une réalimentation satisfaisante. Il convient dans ces cas de mettre en place rapidement une alimentation parentérale et de discuter la pose d'une jéjunostomie.
• Des IPP peuvent être introduits pour traiter les reflux d'une sécrétion acide résiduelle (pas de preuve de son intérêt, mais fait systématiquement).
• Il faudra veiller pour les atteintes sévères orales, à la mise en place de vaseline intra-buccale et péri-buccale régulière avec exercices de traction de la langue pour éviter les risques de microstomie (fermeture des commissures labiales) et de microglossie au long terme (rétraction de la langue), dramatiques sur le plan fonctionnel.
À noter l'absence d'intérêt démontré des antibiotiques, de la somatostatine ou des corticoïdes.
E. P. & Q. R.– Quelles sont les évolutions après ingestion de caustique et quels traitements possibles ?
Pr P. C.– La complication la plus fréquente est la sténose oesophagienne séquellaire (30 % des cas).
On revoit systématiquement le patient en rendez-vous à 1 mois pour évaluer l'apparition d'une dysphagie révélatrice de sténose. On évalue les caractéristiques des sténoses au mieux par TOGD.
Ces sténoses peuvent être situées à différents étages :
• Les sténoses de l'hypopharynx sont traitée par colopharyngoplastie (7).
La réalisation d'une trachéotomie est systématique lors de cette intervention.
Son but est double : prévenir l'asphyxie par l'œdème post-opératoire de la muqueuse colique à hauteur de la margelle laryngée et protéger les voies respiratoires des fausses routes lors de la réalimentation. Le patient nécessitera une rééducation post-opératoire à la déglutition longue et souvent fastidieuse.
• Les sténoses de l'antre sont traitées par antrectomie avec reconstruction par anastomose gastro-jéjunale sur anse en Y. À noter qu'il y a peu de résultats satisfaisant de la dilatation antrale endoscopique, d'où la prise en charge chirurgicale d'emblée.
• Les sténoses de l'oesophage sont traitées de première intention par la dilatation endoscopique itérative (à ne pas réaliser avant 6 semaines). Son taux de succès est de 40 %.
Une dilatation est considérée comme un échec lorsque la première n'a pu être réalisée, en raison notamment d'une obstruction oesophagienne complète, ou s'il existe une récidive de sténose après 5 à 7 dilatations (sténose dite réfractaire à la dilatation) ou encore lors d'une perforation de la dilatation.
On ne dilate plus au-delà de 7 dilatations car alors apparait un risque de cancer de l'oesophage.
En cas d'échec, le meilleur substitut pour une reconstruction est l'estomac (gastroplastie), si celui-ci n'a pas été retiré initialement et ne fait pas l'objet de sténose. C'est une intervention moins morbide avec de meilleurs résultats fonctionnels (100 %) et une durée d'hospitalisation plus courte par rapport à la coloplastie. Si la gastroplastie a été réalisée pour sténose, il faut retirer l'oesophage dans le même temps et ne pas réaliser d'exclusion oesophagienne, source de complication (mucocèle, abcès sous-phrénique).
Si l'estomac n'est pas utilisable, la reconstruction sera réalisée par une coloplastie médiastinale antérieure (rétrosternale).
À l'hôpital Saint-Louis, la coloplastie droite est privilégiée (possibilité de coloplastie gauche en cas de nécrose postopératoire, alors que l'inverse n'est pas toujours possible).
À noter qu'il s'agit d'une procédure redevable de centre expert des reconstructions oesophagiennes, à la différence de l'OGT en urgence, qui doit, à mon sens, être réalisable par tout chirurgien viscéral, puisque le pronostic vital dépend de la rapidité de l'exérèse viscérale.
On doit attendre 6 mois avant d'envisager une reconstruction et il faudra au préalable :
• Une évaluation psychiatrique.
• Un examen ORL approfondi, à la recherche de séquelles ORL, qui modifient la technique chirurgicale.
• Une coloscopie si âge supérieur à 55 ans ou antécédents personnels ou familiaux de néoplasie colique.
E. P. & Q. R.– Finalement après traitement des séquelles et/ou remise en continuité, doit-on continuer à suivre le patient ?
Pr P. C.– Absolument, il faut continuer le suivi, à vie en cas de reconstruction par coloplastie, en raison de la possibilité de survenue de complications tardives : sténoses, jabots et reflux. Ces complications peuvent nécessiter des ré-interventions complexes (8).
Si on est en échec de première coloplastie, il ne faut pas partir du principe que plus rien n'est réalisable. On peut réaliser une seconde coloplastie, mais cette situation relève certainement d'un centre expert.
E. P. & Q. R.– A-t-on des perspectives d'amélioration finalement dans nos pratiques ?
Pr P. C.– Oui, nous allons démarrer un essai clinique pour évaluer un substitut oesophagien issu de l'ingénierie tissulaire dans le traitement des sténoses courtes oesophagiennes réfractaires aux dilatations endoscopiques (ESO-GRAFT).
Références
1. Challine A, Maggiori L, Katsahian S, et al. Outcomes Associated With Caustic Ingestion Among Adults in a National Prospective Database in France. JAMA Surg 2022; 157(2): 112-9.
2. Chirica M, Resche-Rigon M, Bongrand NM, et al. Surgery for caustic injuries of the upper gastrointestinal tract. Ann Surg 2012; 256(6): 994-1001.
3. Chirica M, Resche-Rigon M, Pariente B, et al. Computed tomography evaluation of high-grade esophageal necrosis after corrosive ingestion to avoid unnecessary esophagectomy. Surg Endosc 2015; 29: 1452-61.
4. Bruzzi M, Chirica M, Resche-Rigon M, et al. Emergency Computed Tomography Predicts Caustic Esophageal Stricture Formation. Ann Surg 2019; 270(1): 109-14.
5. Benjamin B, Agueb R, Vuarnesson H, et al. Tracheobronchial Necrosis After Caustic Ingestion. Ann Surg 2016; 263: 808-13
6. Chirica M, Kraemer A, Petrascu E, et al. Esophagojejunostomy after total gastrectomy for caustic injuries. Dis Esophagus 2014; 27: 122-7.
7. Lefrancois M, Gaujoux S, Resche-Rigon M, et al. Oesophago-gastrectomy and pancreatoduodenectomy for caustic injury. Br J Surg 2011; 98(7): 983-90.
8. Chirica M, Chaisemartin C, Goagsen N, et al. Colopharyngosplasty for the treatment of severe Pharyngooesophageal Caustic Injuries. Ann Surg 2007 ; 246 : 721-727.
9. Voron T, Anyla M, Corte H, et al. The cervicosternolaparotomy approach for the treatment of graft dysfunction after retrosternal esophageal reconstruction for caustic injuries. J Thorac Cardiovasc Surg. 2016 Nov;152(5):1378-1385.

