
Durant notre internat, un des premiers gestes que nous apprenons est de réaliser une gastroscopie. Les polypes gastriques représentent entre 1 à 6 % des gastroscopies et il existe plusieurs types de polypes impliquant des conduites à tenir pouvant être différentes.
Cet article est basé principalement sur le travail du United European Gastroenterology (UEG) et vise à donner une vision claire et synthétique des polypes gastriques que nous serons amenés à rencontrer dès les premiers mois de notre formation. Il ne traitera pas des critères de qualité d'une gastroscopie, des adénocarcinomes, des tumeurs sous-muqueuses, des métastases gastriques ou des lymphomes.
Polype glandulo-kystique ou fundique (70 % des polypes gastriques)
Ils apparaissent petits, brillants avec des laci vasculaires visibles en surface. Ils prédominent dans le fundus et le corps gastrique et sont souvent associés à la prise d'IPP.
Histologie : Dilatation des glandes fundiques. La dysplasie est rare.
Conduite à tenir
• Résection indiquée si :
• Polype > 1 cm
• Localisation : antre
• Aspect ulcéré
• Si > 20 polypes, réaliser une coloscopie pour éliminer une polypose adénomateuse familiale (PAF). En cas de PAF confirmée, il faut une surveillance par gastroscopie tous les 2 ans pour dépister un adénome.
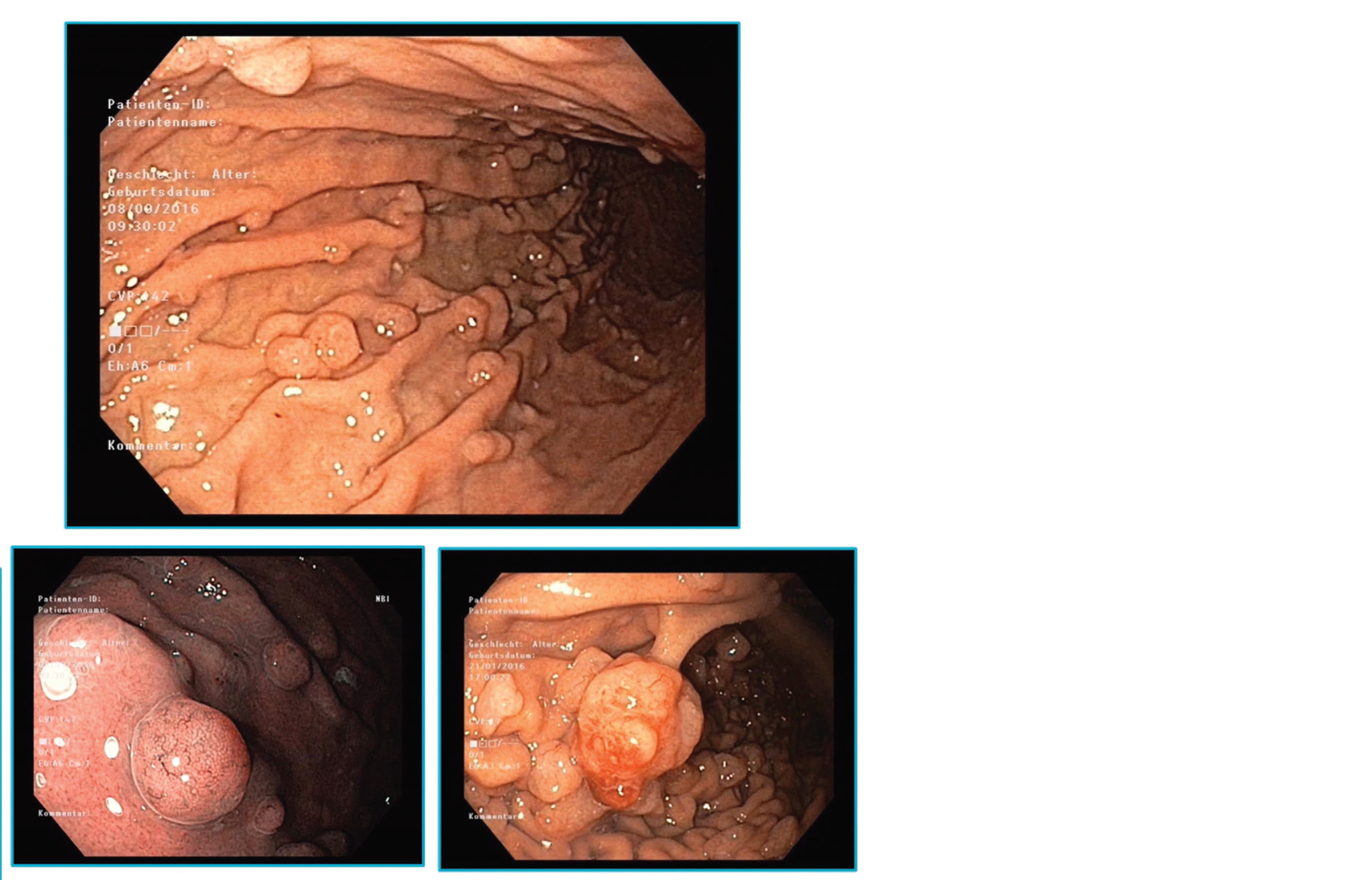
Figure 1 · Polypes glandulokystiques ou fundiques
Polype hyperplasique (20 % des polypes gastriques)
Ils sont plus fréquents dans les régions à forte prévalence d'Helicobacter pylori.
Leur aspect est sessile ou pédiculé, de 5 à 15 mm, parfois ulcéré. Ils sont uniques, le plus souvent antraux, ou multiples dans le corps. Ils peuvent avoir un aspect en dôme hyperhémié avec des glandes allongées et une vascularisation homogène. Malgré son aspect possiblement hyperhémié, ce polype est rarement la cause d'anémie ferriprive.

Figure 2 · Polype hyperplasique unique de l'antre
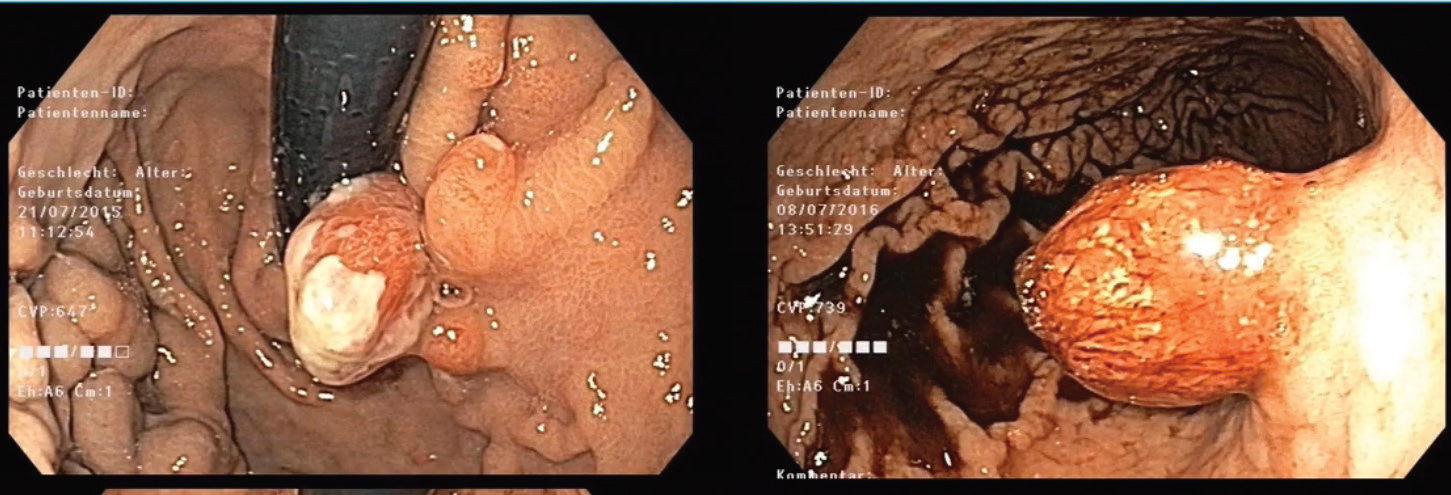
Figure 3 · Polype hyperplasique en forme de dôme hyperhémié
Associations fréquentes
Gastrite atrophique liée à H. pylori, gastrite réactionnelle (ulcère, gastrostomie), gastrite auto-immune (Biermer). L'anémie ferriprive est rare malgré l'aspect parfois hémorragique.
Histologie
Hyperprolifération inflammatoire de la muqueuse gastrique. On distingue plusieurs sous-types : polype inflammatoire, hyperplasie fovéolaire polypoïde, gastrite kystique polypoïde (post-gastrectomie).
Risque de dysplasie ou cancer
La dysplasie est retrouvée dans 5–20 % des cas, et un adénocarcinome dans environ 2 %. Les facteurs de risque sont une taille > 1cm, un aspect Paris 0-Ip et un antécédent de gastrectomie.
Conduite à tenir
• Résection d'emblée si polype unique > 5 mm par anse diathermique.
• En cas de polypes multiples, réséquer les plus volumineux pour ne pas méconnaître un adénocarcinome.
• Si polype < 10 mm et infection à H. pylori, l'éradication doit être systématique car elle peut entraîner une régression spontanée.
Surveillance
• Non nécessaire après résection d'un petit polype hyperplasique isolé, sans dysplasie ni gastrite chronique.
• En cas de gastrite chronique, la surveillance dépend du score anatomopathologique OLGA :
• OLGA III–IV FOGD tous les 3 ans.
• OLGA I–II pas de bénéfice démontré d'une surveillance systématique.
Polype adénomateux (1% des polypes gastriques)
Il s'agit d'une lésion précancéreuse : 75 % évoluent vers un adénocarcinome. De plus, 30 % sont
synchrones, surtout en cas de gastrite atrophique. Ils peuvent avoir un aspect Paris 0-Is (plan) ou 0-IIa (sessile surélevé).
Conduite à tenir
• Résection en bloc obligatoire.
• Surveillance :
• Dysplasie de bas grade : gastroscopie de contrôle dans un délai d'un an maximum.
• Dysplasie de haut grade : gastroscopie de contrôle a 6-12 mois.
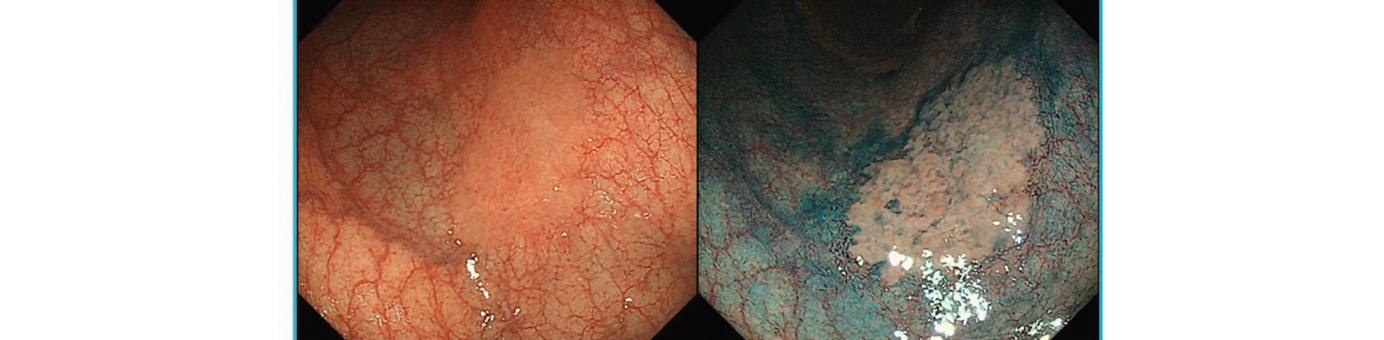
Figure 4 · Adénome gastrique pédiculé Paris 0-Ip retiré à l'anse froide
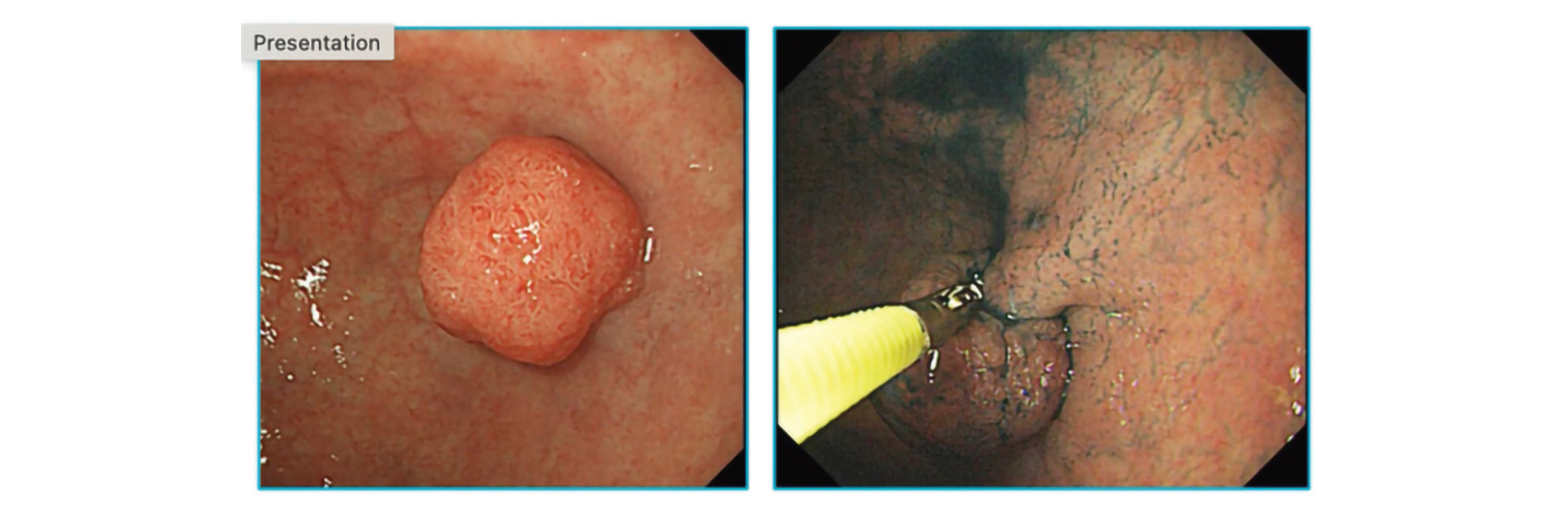
Figure 5 · Adénome gastrique plan Paris 0-IIb qui va probablement nécessiter une dissection sous-muqueuse…
Le cas particulier de l'adénome gastrique de type fovéolaire
L'adénome gastrique de type fovéolaire (FGA : foveolar-type gastric adenoma) est une lésion précancéreuse qui peut ressembler morphologiquement à un petit polype hyperplasique gastrique chez les personnes non infectées par H. Pylori (HpN-GHP : Hp-naive gastric hyperplastic polyp).
Son aspect macroscopique lui rend une différenciation difficile, même après biopsie. En anglais, on le décrit avec une « raspberry appearance » (= un aspect en framboise pour les moins bilingues d'entre nous).
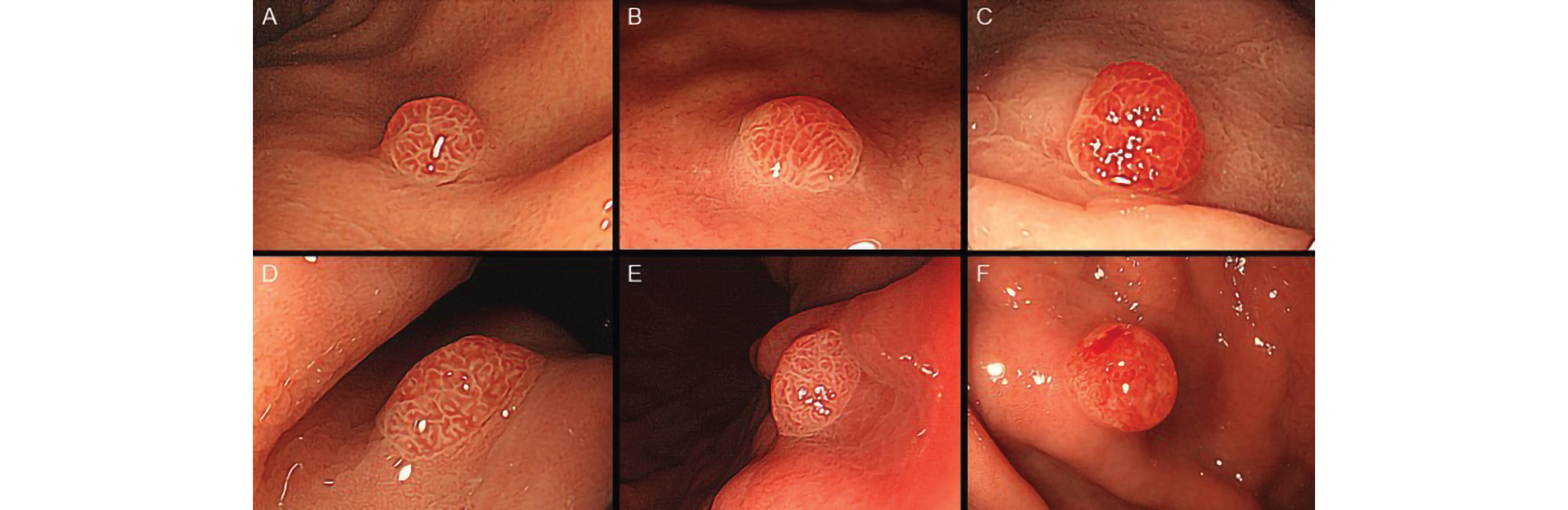
Figure 6 · Un adénome gastrique (A, B, C) et un polype hyperplasique HpN-GHP (D, E, F)
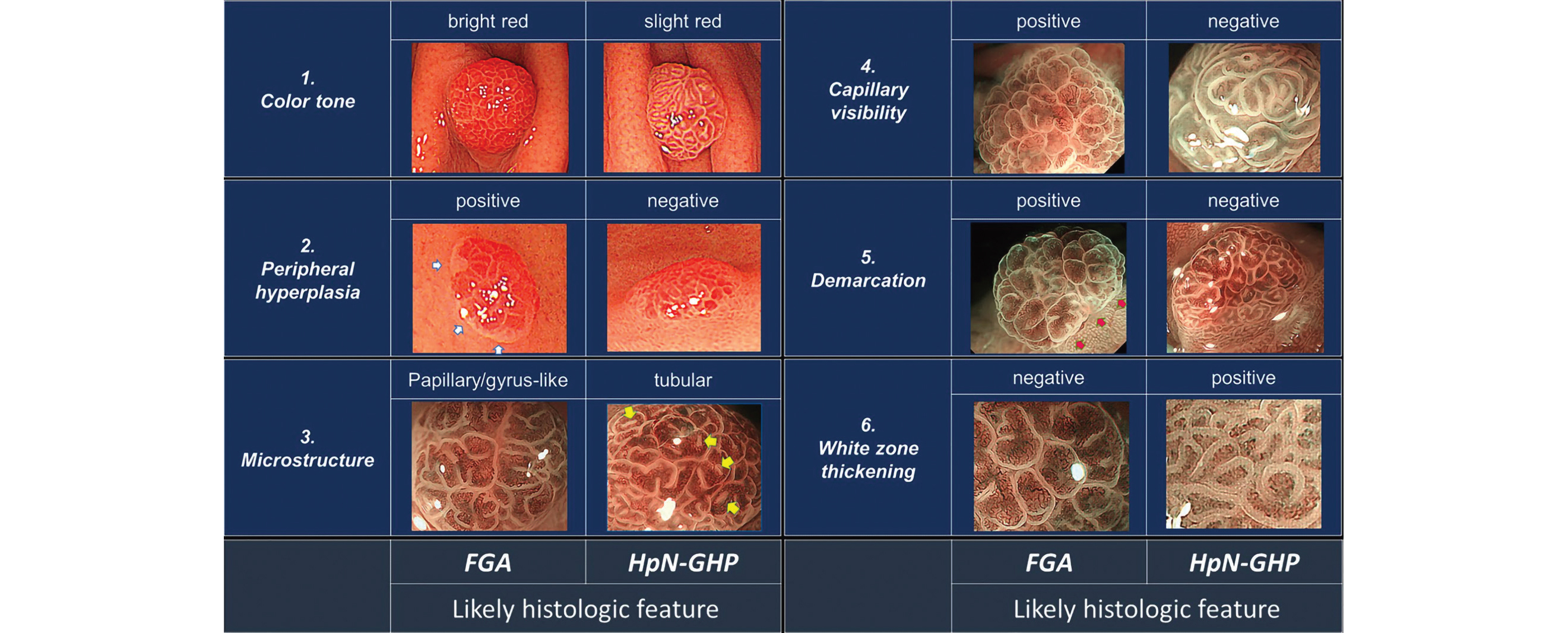
Figure 7 · L'adénome gastrique de type fovéolaire, en comparaison avec le polype hyperplasique HpN-GHP, est rouge vif avec une hyperplasie des glandes à sa périphérie, a une microstructure plutôt papillaire avec des circonvolutions (en opposition avec la présence de tubules), des micro-vaisseaux visibles en chromo-endoscopie, une démarcation basale nette et l'absence de l'épaississement blanchâtre au niveau des circonvolutions. On considère que la présence de quatre critères sur six permet de le classer comme un adénome gastrique à type fovéolaire, et donc à la résection en bloc systématique
En conclusion
Devant un polype gastrique, toujours se poser les questions suivantes :
• Quelle est sa taille ?
• Quelle est sa localisation ?
• Y a-t-il un contexte (IPP, gastrite, H. pylori, PAF, Biermer…) ?
• Quelle est son apparence (forme, vascularisation, ulcération) ?
En cas de doute, la biopsie du polype seule est rarement suffi sante_ : la résection est souvent nécessaire pour caractérisation histologique complète.
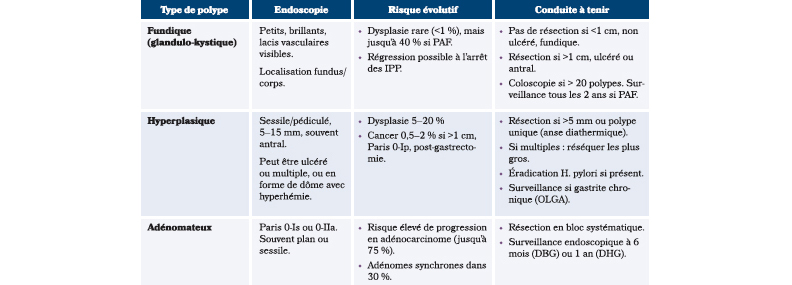
Et pour avoir une source toujours prête dans sa galerie photo, voici un tableau récapitulatif pour résumer l'article
Références
• UEG Online Course – Gastric Polyps (2018).
• Islam RS, et al. Gastric polyps: a review of clinical, endoscopic, and histopathologic features and management decisions. Gastroenterol Hepatol 2013 ; 9: 640–651.
• Shaib YH, et al. Management of gastric polyps: an endoscopy-based approach._ Clin Gastroenterol Hepatol 2013; 11: 1374–1384.
• Dinis-Ribeiro M, et al. Management of precancerous conditions and lesions in the stomach (MAPS): guideline from the European Society of Gastrointestinal Endoscopy (ESGE), European Helicobacter Study Group (EHSG), European Society of Pathology (ESP), and the Sociedade Portuguesa de Endoscopia Digestiva (SPED)._Endoscopy_2012; 44: 74–94.
• Shibagaki, K., Ishimura, N., Kotani, S. et al. Endoscopic diff erential diagnosis between foveolar-type gastric adenoma and gastric hyperplastic polyps in Helicobacter pylori-naïve patients. Gastric Cancer 2023 ; 26 : 1002–1011.

Tiffany VO
Interne en HGE à Rouen

