En 2024 est sorti le nouveau consensus de prise en charge de l'hyperparathyroïdie (HPT) primaire. En effet, les dernières recommandations dataient de 2005 et avaient d'ailleurs inauguré la série des traditionnels consensus annuels de la SFE.
Celui-ci a été écrit par les membres de la Société Français d'Endocrinologie, de l'Association Française de Chirurgie Endocrinienne et la Société Française de Médecine Nucléaire.
Nous vous proposons, à travers cet article, de reprendre les chapitres un par un en ciblant les points forts et de vous lister les recommandations, dont nous vous rappelons, d'ailleurs, la gradation :
- A : recommandation forte, ++++, preuves de très grande qualité, études prospectives randomisées.
- B : recommandation faible, +++, preuves de bonne qualité, études prospectives de cohorte.
- C : neutres (ne se prononce pas).
- ++, preuves de qualité moyenne : études de registres, études rétrospectives.
- +, preuve de qualité faible : cas cliniques.
- Accord d'experts : pas de données scientifiques disponibles.
Introduction :
les parathyroïdes, ces glandes singulières qui sécrètent la PTH
Les parathyroïdes sont ainsi dénommées du fait de leur proximité avec la thyroïde. 96 % d'entre elles sont situées dans le cou. On distingue une paire de P3 et une paire de P4. Des glandes surnuméraires sont possibles.
- Les P4 dérivent de la 4.me poche branchiale, avec une aire de dispersion limitée, en arrière du lobe thyroïdien.
- Les P3 dérivent de la 3.me poche brancuale, avec une aire de dispersion large qui va de l'angle mandibulaire au médiastin...
La sécrétion de PTH est majoritairement régulée par le récepteur CaSR. Il fait partie de la famille des nutrient-sensors, ces répéteurs sensibles aux nutriments, visitables substrats cellulaires du lien entre nutrition et endocrinologie. Le CaSR est présent sur les cellules parathyroïdiennes et les cellules du tubule rénal.
La PTH est sécrétée en cas de déplétion calcique et a donc pour rôle d'augmenter la calcémie par différents mécanismes.
- Elle stimule la 1-α hydroxylase dans le tubule proximal du néphron, activant la 25 vitamine D (hormone de réserve peu active) en 1-25 vitamine D (calcitriol), véritable hormone active qui stimule l'absorption intestinale de phosphore et de calcium.
- Elle augmente le remodelage osseux.
- Elle stimule la réabsorption rénale du calcium tout en inhibant celle du phosphore.
Ainsi, la plupart des hyperparathyroïdies sont secondaires, principalement dues à un déficit en vitamine D et à une insuffisance rénale du fait de la réduction néphrotique qui entraîne une perte des fonctions sécrétoires et des clairances.
- La réduction néphrotique entraîne une perte de la fonction endocrine et sécrétoire et donc, de la 1α-hydroxylase, qui mène à un défaut de réabsorption rénale du calcium et qui est le 1er mécanisme favorisant l'hypocalcémie.
- La réduction néphrotique diminue la clairance rénale de phosphore et favorise une hyperphosphorémie qui augmente la production de FGF23, diminuant ainsi la vitamine D active qui est le second mécanisme favorisant l'hypocalcémie
- La réduction néphrotique entra.ne une diminution du CaSR et donc une résistance à la PTH.
- Tous ces processus entraînent une hypersécrétion de PTH et une hyperplasie des glandes parathyroïdiennes.
L'hyperparathyroïdie primaire (HPP) résulte d'une secretion inappropriée de PTH par un adénome parathyroïdien unique ou double, une hyperplasie multiglandulaire et, fort heureusement, dans moins de 1% des cas par le rarissime mais redoutable carcinome parathyroïdien.
Parmi les étiologies de l'HPP :
- La plus fréquente, est de loin, l'adénome sporadique (95 %).
- Puis suivent les formes familiales (5-10 %) liées essentiellement aux mutations de MENINE, RET, CDC73 (ex-HRPT2).

Épidémiologie
Chez l'adulte
20-100/100.000 patients-années Prédominance féminine (75 %) surtout après la ménopause.
Chez l'enfant
2-5/100.000 enfants-année prédominance masculine (60 %).
Chez la femme enceinte
1 % des grossesses.
La prévalence augmente avec l'âge :
5 % des patients ont moins de 40 ans.
85 % ont plus de 50 ans.
65 % ont plus de 60 ans.
La prévalence est plus élevée dans les populations Noires et Asiatiques. Cette prévalence est encore plus élevée lorsque l'on prend en considération les HPP normocalcémiques.
Le diagnostic
80 % des HPP sont dites asymptomatiques et ce n'est qu'à l'anamnèse qu'on retrouvera une notion d'ostéodensitométrie pathologique, de chondrocalcinose, d'anomalies du bilan rénal.
Note du relecteur : Devant toute déminéralisation osseuse, toute lithiase urinaire et toute néphropathie, il faut évoquer l'HPP.
La clinique est peu spécifique et surtout non corrélée au degré d'hypercalcémie ou de PTH.
- Les signes classiques sont liés au syndrome d'hypercalcémie et aux complications rénales et osseuses.
- On note des signes non classiques, retrouvés sur des études d'associations, qui peuvent ne pas régresser après chirurgie : HTA, nausées, vomissements, constipation, dépression, anxiété, idées suicidaires délires, troubles cognitifs.
Le diagnostic est biologique :
- Hypercalcémie à PTH inadaptée
- En l'absence de déficit en vitamine D (éventuellement corrigée).
- En l'absence d'hypocalciurie ou avec FeCa supérieur à 2 % (pour éliminer l'hypercalcémie hypocalciurique bénigne familiale).
On dosera donc : calcémie totale (éventuellement ionisée), phosphatémie, PTH, cr.atinin.mie, 25 vitamine D calciurie des 24h ou fraction éjectée du calcium (FeCa).
En cas d'HPP normocalcémique ou d'hypercalcémie à PTH inadaptée mais dans les normes, il faut s'assurer d'apports calciques répondant aux besoins, et normaliser la vitamine D au moins 6 mois.
Pour les diagnostics encore douteux : on peut réaliser un test de charge calcique. En l'absence d'HPP, on en attend une augmentation du calcium ionisé et une diminution de la PTH après 1g de calcium oral.
Note du relecteur : Cette sémiologie des signes non classiques, floue et difficile à appréhender, que j'appelle “malfoutose”, bien connue des cliniciens, est un pan important de la pathologie parathyroïdienne. Cela doit mener à des études plus approfondies et dépasser nos raisonnements classiques. Rappelons par exemple que dans les dernières recommandations européennes sur l'hypoparathyroïdie, la qualité de vie et la prise en compte des symptômes a détrôné l'objectif calcémique. Cela traduit un heureux retour en force de la clinique holistique dans nos démarches et le consensus considère même que cela peut affiner l'indication chirurgicale.
Note du relecteur : Après des années de domination des esprits et des conférences d'internat, l'utilisation de la calcémie corrigée par l'albumine est invalidée et ne doit donc plus être d'actualité : elle augmente le taux de diagnostic erronés. En cas d'hypoalbuminémie, il faut préférer la calcémie ionisée.
L'HPP normocalcémique concerne 0,1 à 9 % des patients. Pour l'affirmer, il faut rechercher et éliminer :
1. Une carence en vitamine D.
2. Une insuffisance rénale.
3. Une hypercalciurie idiopathique.
4. Une malabsorption.
5. Un traitement par diurétiques de l'anse, dénosumab, biphosphonates ou phosphate.
Retentissement
Rénal : calculs urinaires, néphrocalcinose, néphropathie tubulo-interstitielle chronique, insuffisance rénale.
Le d.pistage comprend :
1. Une évaluation de la fonction rénale : un dosage de créatininémie avec calcul du DFG.
2. Une analyse d'urine.
- Sur 24h : hypercalciurie de débit sur 24h : F supérieur à 6,25 mmol/24h (250mg/24h), H supérieur à 7,5 mmol/24h (300 mg/24h).
- Sur 2éme échantillon à jeun : hypercalciurie de concentration sur échantillon (supérieur à 3,8 mmol/l ou 150 mg/l).
3. Une imagerie rénale recherchant calculs et néphrocalcinose : échographie ou scanner rénal low dose.
Un avis néphrologique est recommandé en cas de DFG inférieur à 60 ml/min et un avis urologique en cas de calculs ou de rein unique.
Osseux : Tumeurs brunes, ostéite fibrokystiques, ostéoporose, chondrocalcinose, sacroiliites, fractures (poignet, rachis).
Le d.pistage comprend :
1. Une densitométrie osseuse (DMO) : rachis lombaire, fémur total, col fémoral, 1/3 proximal du radius.
2. La mesure de la taille.
3. Une imagerie du rachis dorsolombaire (face/profil ou EOS ou vertebral fracture assessment en DMO).
4. La recherche syst.matique des autres facteurs de risqué d'ostéoporose.
Les marqueurs du remodelage osseux peuvent être dosés : CTX, PAL osseuses, ostéocalcine.
L'atteinte de l'os cortical est causée directement par l'hypersécrétion de PTH et peut donc être aussi présenté en cas d'HPP normocalcémique.
Un avis rhumatologique est recommandé si :
- HPP normocalcémique avec atteinte osseuse isolée.
- Fracture il y a moins de 2 ans.
- Perte plus de 1 DS en moins de 2 ans.
- Refus ou contre-indication (CI)à la chirurgie.
- Traitement anti-ostéoporotique en cours (arrêter pour chirurgie).
Note du relecteur : Insistez, ré-insistez sur vos prescriptions d'ostéodensitométrie pour la mesure au poignet, atteinte spécifique de l'hyperparathyroïdie qui n'est plus systématiquement réalisée… surlignez-le en fluo, mettez “+++++” à côté… avec un peu de chance, cela attirera l'œil.
Cardiaque : ECG pour rechercher des ESA, ESV, raccourcissement du QT.
On note également un effet métabolique par inhibition de la lipolyse adipocytaire induite par les catécholamines, pouvant augmenter le risque de surcharge pondérale, trouble du métabolique glucidique et anomalies lipidiques, tout ceci augmentant le risque et la mortalité cardiovasculaire.
Diagnostics différentiels
Eliminer les facteurs susceptibles de masquer ou induire hypercalcémie ou hypercalciurie
Hyperparathormonémie sans augmentation de l'absorption intestinale du calcium
Carence en vitamine D (dosage).
Insuffisance rénale (mesure du eDFG), Malabsorption et alimentation très pauvre en calcium (maladies inflammatoires du tube digestif, maladie cœliaque, chirurgie bariatrique...), corticothérapies
Causes iatrogènes
Diurétiques (parfois iSGLT2), supplémentation excessive en vitamine D ou en calcium.
Biphosphonates, denosumab, lithium (HyperPTH sans élévation de résorption osseuse nette), inhibiteurs du check point immunitaire.

Génétique et HPP syndromiques
10 % des HPP sont d'origine génétiques, syndromiques ou isolées.
Les gènes à rechercher en 1e intention sont :
- MEN1, CDKN1B, RET, CDC73 qui sont des syndromes.
- CASR, GNA11, AP2S1, GCM2 qui causent des HPT primaires isolées, toutes autosomiques dominantes.
En 2nde intention : CDKN1A, CDKN2B, CDKN2C, PRUNE2, PRAD1, TRPV6. Si le panel revient non contributif le séquençage en très haut débit après passage en RCP Plan France Médecines Génomique (PFMG) se justifie.
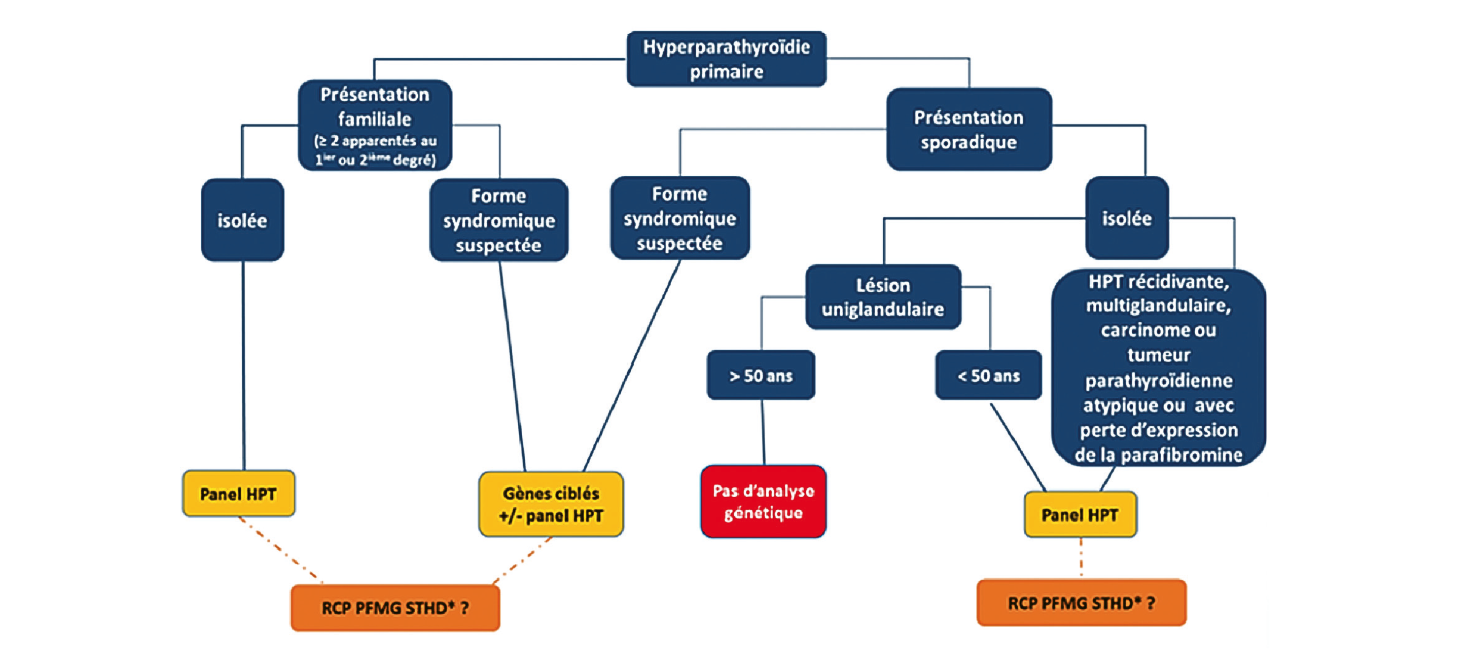
Indications de la recherche génétique
1. Histoire personnelle ou familiale avec un syndrome existant NEM1, NEM2A, NEM2B, HPT-JT.
2. Histoire familiale : supérieur où égale 2 apparentés au 1e ou 2e degré présentant une HPP.
3. Sujet jeune inférieur à 30-35 ans, voire inférieur à 50 ans.
Les phénotypes les plus associés aux formes génétiques sont les suivants :
1. Récidive
2. Forme multiglandulaire.
3. Carcinome parathyroïdien (CDC73)
4. Tumeurs parathyroïdiennes atypiques, perte de la parafibromine.
La plus connue est la NEM1
- HPP chez plus de 90 % des patients.
- Le plus souvent avant 40 ans.
- Avec une atteinte multiglandulaire.
- Le dépistage dans cette population consiste en une calcémie annuelle.
La NEM 2A
- 20-30 % des sujets atteints.
- Vers 30-40 ans.
- Plutôt un adénome unique ou double.
- Rappel classique 1 : pour tout sujet qui va se faire opérer d'une HPP, il est préférable de doser une calcitonine pour ne pas méconnaître un CMT et le traiter dans le même temps (et le temps opératoire n'est pas le même !!).
- Rappel classique 2 : pour tout sujet qui va se faire opérer d'un CMT, il faut rechercher une HPP pour la traiter dans le même temps.
- Rappel classique 3 (et l'anesthésiste vous dira merci !!) : éliminer un phéochromocytome en cas de mutation de RET avant toute induction anesthésique.
Le syndrome HPT I jaw tumor est induit par une mutation de CDC73 (ex HRPT2) :
- Autosomique dominant forte pénétrance.
- Survenant avant 30 ans.
- Dont l'hypercalcémie est volontiers sévère.
- Et peut être liée un carcinome parathyroïdien une atteinte mono ou pluri glandulaire.
- Entraînant des tumeurs osseuses maxillo-mandibulaires, rénales, utérines.
- A noter que le risque de récidive post-chirurgical est de 25 %.
Formes cliniques aux âges de la vie
Chez les nouveau-nés et nourrissons
- L'HPP est le plus souvent asymptomatique
- Liée à une mutation germinale (70 % des cas) du g.ne CaSR, aggravé par une carence maternelle en vitamine D.
- En cas de mutation homozygote inactivatrice, l'hypercalcémie est s.v.re avec un retentissement important.
Chez les enfants et les adolescents, l'HPP est sévère et symptomatique, en lien avec les mutations décrites précédemment.
La grossesse entraîne des modifications spécifiques :
- Une augmentation de l'absorption intestinale du calcium et donc de la calciurie.
- Le placenta et la glande mammaire secrètent de la PTHrp.
- En cas d'HPP pendant la grossesse, il faut rechercher une mutation et une HHF.
- Les imageries à privilégier sont l'échographie et l'IRM.
- Les biphosphonates sont contre-indiqués.
- La surveillance biologique doit être au moins mensuelle.
En cas de nécessité de chirurgie, il faut la réaliser au 2e trimestre.
En l'absence de prise en charge, il existe un risque d'hypercalcémie sévère en post-partum immédiat par arrêt du transport vers le placenta. Il est recommandé de surveiller le calcium ionisé toutes les 48h jusque 1-2 semaines post partum, puis tous les 2 mois la calcémie et créatinine pendant l'allaitement.
L'HPP est fréquente après 65 ans et donne volontiers des fractures vertébrales en raison du risque augmenté d'ostéoporose. La place de la chirurgie reste sûre et efficace chez le sujet âgé. A noter que la nécessité d'hyperhydratation est moins stricte car la calciurie moins élevée.
Cancer parathyroïdien
Le cancer parathyroïdien représenté moins de 1 % des causes d'HPP, et le sex ratio est 1/1.
Une mutation germinale est retrouvée dans. -1/3 des cancers, principalement CDC73.
La clinique est s.v.re, en lien avec l'hypercalcémie ou le syndrome tumoral.
La suspicion de carcinome parathyroïdien contre-indique toute cytoponction à l'aiguille fine en raison du risque d'ensemencement.
La prise en charge est médicale (cinacalcet) si besoin et chirurgicale de préférence R0, sans curage +/- radiothérapie.
On note 30 à 67 % de rechute en 2 à 5 ans et 50 % de décès par hypercalcémie en cas de métastase.
La survie à 5 ans est de 60 à 95 % et 57-66 % à 10 ans.
En discuter en RCP ENDOCAN en cas de maladie locorégionale ou métastatique (os, poumon, foie, ganglion, cerveau).
Le suivi s'effectue par échographie + scanner cervico-thoracique et calcémie tous les 3 mois pendant 2 ans puis tous les 6 mois pendant 3 ans puis annuellement.
On note des tumeurs potentielles de malignité incertaine avec risque de rechute et notamment les tumeurs à perte d'expression de la parafibromine.
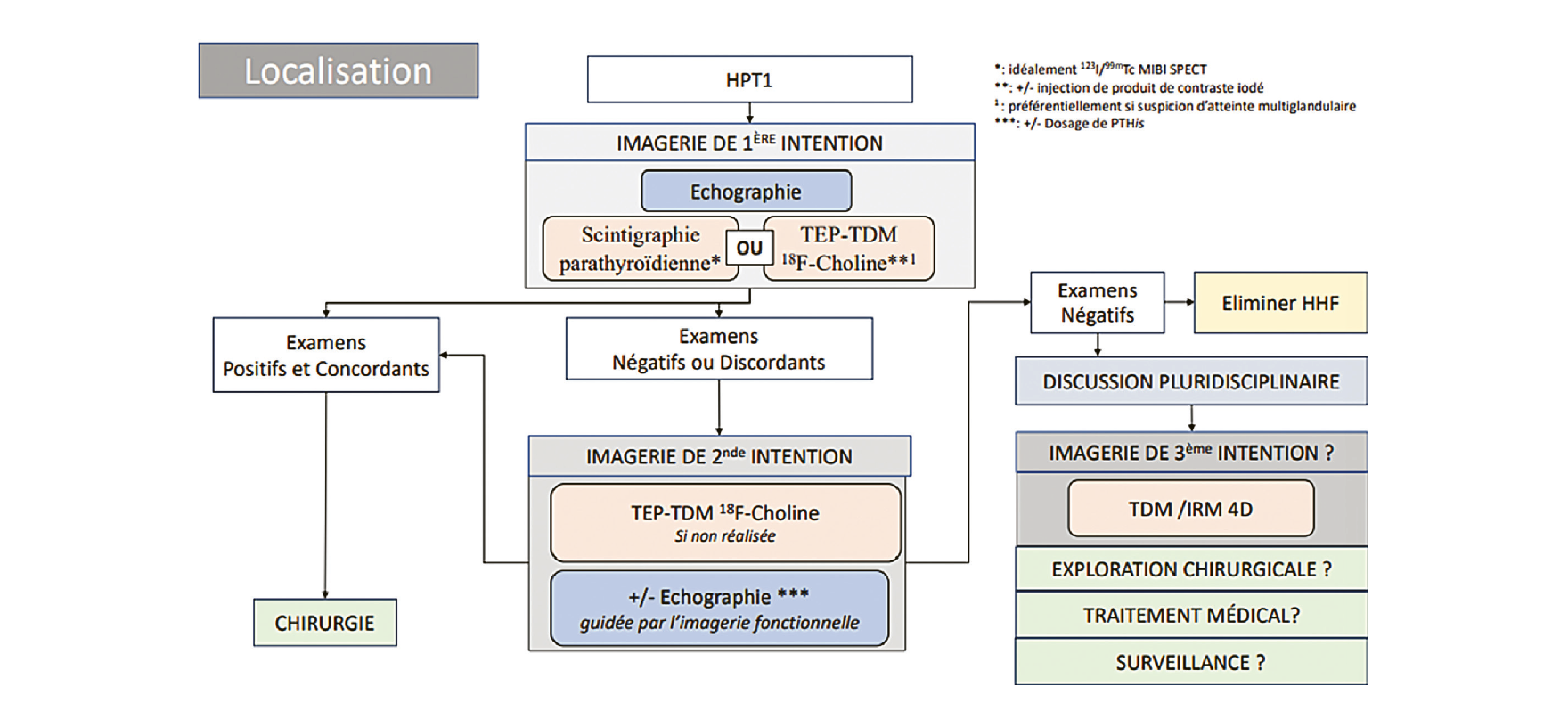
Imagerie parathyroïdienne
Note du relecteur : On dit classiquement que l'imagerie ne doit être réalisée qu'en cas de chirurgie indiquée… or l'imagerie n'a pas qu'un rôle de localisation de l'adénome car l'étude approfondie de la thyroïde et du cou peut poser une indication de cervicotomie pour une autre raison et faire, in fine, se reposer la question de l'ablation de l'adénome puisque ce n'est pas ce dernier qui motive la cervicotomie. J'encourage les lecteurs motivés à se former à l'échographie et à contribuer ainsi à affiner le raisonnement thérapeutique de leurs patients atteints d'HPP.
Traitement
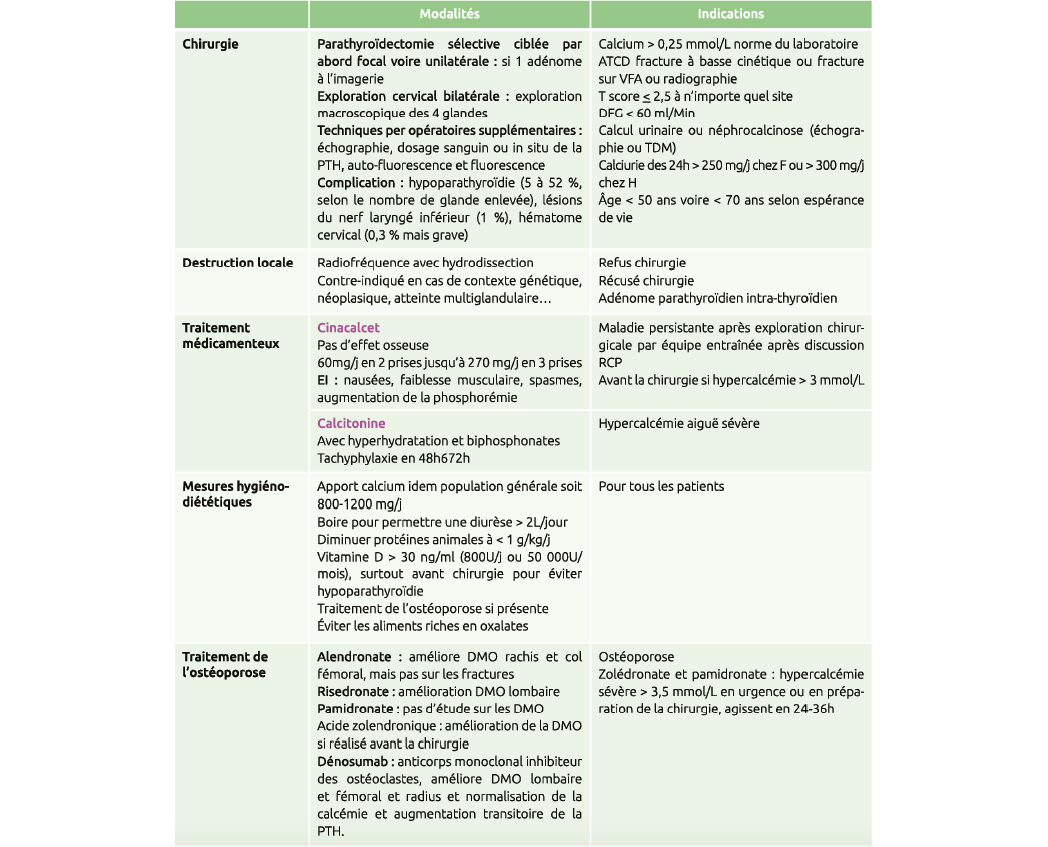
Note du relecteur : Ce consensus officialise la place de la thermoablation. L'évolution des techniques rend possible le traitement d'un adénome extrathyroïdien mais l'indication élective est sans nul doute le traitement des adénomes parathyroïdiens intrathyroïdiens qui obligent au sacrifice du lobe concerné.
Classification anatomopathologique (OMS 2022)
Adénome : tumeur bénigne Adénomes multiples sont difficiles à diffrencier des hyperplasies.
Tumeurs parathyroïdiennes atypiques (TPA) : non invasive à potentiel de malignité incertain. Présentation clinico-biologique plus proches des carcinomes que des adénomes. Critéres histologiques / cytologique en l'absence de critéres formels de carcinome. En cas de perte de CDC73, risque de récidive.
Carcinome : au moins 1 critéres de malignité. (angio-invasion, embole endolymphatique, engainement périnerveux,
infitration, métastases). Recherche de mutation constitutive CDC73.
Tumeurs parafibromine déficientes : adénome, TPA ou carcinome. Parafibromine codée par CDC73, mutation constitutive ou somatique. Risque de récidive locale et atteinte multiglandulaire.
Maladie multiglandulaire : adénome multiples coalescents. Doit faire rechercher NEM.
Hyperplasie parathyroïdienne : en cas de stimuli chroniques (lithium, insuffisance rénale).
Parathyromatose : foyers microscopique parathyroïdien sur le site d'une chirurgie ou biopsie.
Suivi post-chirurgical
Le dosage de la calcémie s'effectue le lendemain de la chirurgie, puis. J8, puis si symptômes évocateurs.
En cas d'hypocalcémie, il faut doser également : Ph, PTH, Mg, 25 OH vitamine D et calciurie.
Une PTH post-chirurgicale supérieur à 10 ng/ml est à faible risque d'hypoparathyroïdie.
Une PTH élevée n'est pas signe de persistance. L'hypoparathyroïdie persistante supérieur à 6-12 mois est considère comme permanente et doit être surveillée mensuellement pendant 12 mois. Elle doit être supplémentée par vitamine D active, et sels de calcium, selon le nombre de glandes restante.
Le syndrome de l'os avide survient entre le 3e et le 5e jour, il nécessite une hospitalisation pour supplémentation en calcium, magnésium, vitamine D active. La surveillance clinicobiologique ultérieure s'effectue à 1 an, puis annuellement en cas d'âge inférieur à 50 ans ou génétique, avec une imagerie urinaire ou ostéodensitométrie selon le retentissement pré-chirurgical.
En l'absence de chirurgie, on suit tous les 3 mois la calcémie, puis avec la vitamine D, calciurie et fonction rénale à 1 an. En cas d'utilisation de thiazidique, la calciurie doit être bisannuelle.
Figure 1 : Arbre décisionnel : indications de l'analyse génétique Abréviations :
HPT : hyperparathyroïdie ; PFMG : Plan France Médecine Génomique ; RCP : réunion de concertation multidisciplinaire ;
STHD : séquençage Très Haut Débit

Persistance ou récidive
• Elle concerne 2,5 à 5 % des sujets opérés.
• Les HPP normocalc.miques ont plus de risque de persistance ou récidive.
• En cas de PTH élevée persistante (inferieur à 6 mois) ou récidivante (supérieur à 6 mois), il faut :
1. S'assurer que l'adénome à bien été retiré sur l'anatomopathologie.
2. Rechercher un adénome ectopique ou une autre localisation.
3. Eliminer une autre cause (voir chapitre correspondant).
4. Evoquer une parathyromatose.
• Si la récidive est confirmée et un second adénome localisé et retiré : penser à l'étude génétique jusqu'au NGS.
• La prise en charge est chirurgicale, après localisation certaine avec 2 examens performants, c'est-à-dire 1 imagerie fonctionnelle et 1 anatomique (cf. l'arbre décisionnel de la localisation page 37).
Anaïs SEGUI
Interne EDN à Angers

Dr Edouard GHANASSIA
Endocrino-diabétologue,
Échographiste - Sète, Paris

