
Introduction
L'étude FINEARTS-HF a été présentée à l'occasion de l'ESC 2024 le premier septembre 2024 à Londres, avec publication concomitante dans le New England Journal of Médicine (1).
Contexte
Les inhibiteurs des récepteurs aux minéralocorticoïdes réduisent le risque de morbi-mortalité chez les patients insuffisants cardiaques à FEVG altérée (2, 5). À ce jour, il n'existe pas de données solides concernant les patients insuffisants cardiaques avec fraction d'éjection ventriculaire gauche (FEVG) modérément altérée ou préservée, malgré l'intérêt hysiopathologique suggéré par l'essai TOPCAT il y a dix ans. Cet essai avait testé la spironolactone, un antagoniste de type stéroïdien, chez des patients avec insuffisance cardiaque à FEVG préservée (ICFEP), montrant des résultats prometteurs mais limités (5, 6).
La FINERENONE, antagoniste non stéroïdien avec mécanisme d'action différent, a récemment montré la réduction des événements cardiovasculaires incluant les épisodes d'insuffisance cardiaque chez les patients diabétiques de type 2 et insuffisants rénaux (7, 8), justifiant son évaluation chez les patients insuffisants cardiaques avec FEVG supérieure à 40 %.
Méthodes
L'étude FINEART-HF est un essai multicentrique contrôlé randomisé en double aveugle, avec randomisation 1 pour 1. Les critères d'inclusion étaient les suivants :
• Âge supérieure à 40 ans ;
• Insuffisance cardiaque symptomatique ;
• FEVG supérieure ou égale à 40 % ;
• Documentation d'une atteinte cardiaque structurelle ;
• Élévation du NTproBNP.
Les critères d'exclusion étaient les suivants :
• Potassium supérieure à 5 mmol/l ou DFG inférieure à 25 ml/m2 ;
• Utilisation d'antagonistes aux minéralocorticoïdes dans les 30 jours précédents l'inclusion
• Antécédent de cardiopathie du péri-partum, de cardiopathie induite par les chimiothérapies, ou de cardiopathie infiltrative type amylose ;
• Diagnostic différentiel expliquant les symptômes.
Le groupe testé recevait une dose de 20 à 40 mg de FINERENONE en fonction du débit de filtration glomérulaire (Figure 1).

Figure 1 : Design de l'étude FINEART-HF.
Le critère de jugement principal est un critère composite comprenant :
• Nombre d'épisode d'insuffisance cardiaque (hospitalisé, récemment hospitalisé, consultation pour insuffisance cardiaque sans nécessité d'hospitalisation) ;
• Décès d'origine cardiovasculaire.
Les critères de jugements secondaires sont les suivants :
• Nombre d'épisodes d'insuffisance cardiaque seul ;
• Valeur du questionnaire de Kansas City à 6, 9 et 12 mois ;
• Amélioration du score NYHA à 12 mois ;
• Décès d'origine cardiovasculaire seul ;
• Décès toute cause ;
• Critère composite rénal (diminution DFG supérieure ou égale à 50 % ou DFG inférieure à 15 ml/min/1.73m2, nécessité de greffe rénale ou de dialyse chronique).
Résultats
Entre septembre 2020 et Janvier 2023, 7463 patients ont été screenés, parmi 654 centres dans 37 pays différents, pour un total de 6016 patients randomisés, dont 6001 analysés dans l'analyse d'efficacité (3003 dans le groupe test et 2998 dans le groupe placebo). La médiane de suivi était de 32 mois.
Les caractéristiques des patients étaient comparables (Table 1), avec notamment :
• Une FEVG de 53 8 % ;
• Une majorité de stade II de la NYHA (69.1 %) ;
• 20.3 % hospitalisés dans les 7 jours d'un épisode d'insuffisance cardiaque ;
• 85 % des patients sous bétabloquant ;
• 35 % sous IEC ;
• 36 % sous ARAII ;
• 8.5 % sous ENTRESTO ;
• 13.6 % sous iSGLT2.
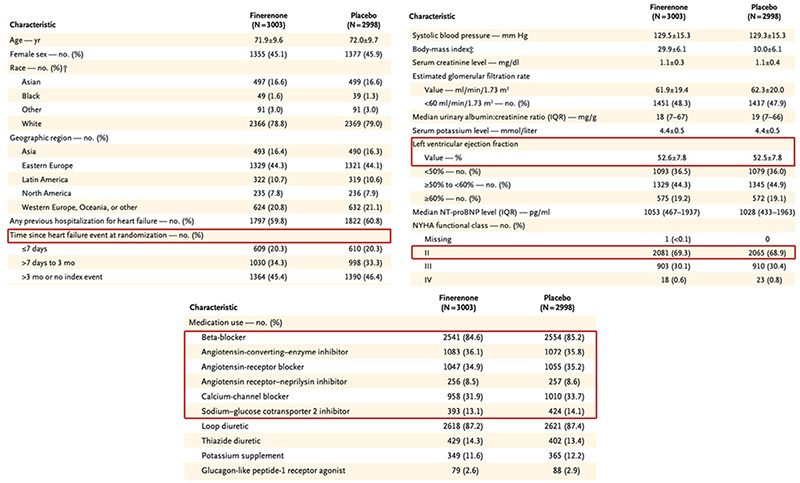
Table 1 : Caractéristiques des patients.
Les résultats sur le critère de jugement principal montrent :
• 1083 événements (36 %) dans le groupe traité, contre 1283 (43 %) dans le groupe placebo (RR 0,84 ; IC 95 % 0,74-0,95 ; p = 0,007).
Pour chaque élément du critère composite, les résultats étaient les suivants :
• Épisodes d'insuffisance cardiaque : 842 événements (28 %) dans le groupe traité, contre 1024 (34 %) dans le groupe placebo (RR 0,82 ; IC 95 % 0,71-0,94 ; p = 0,006) ;
• Décès d'origine cardiovasculaire : 242 événements (8,1 %) dans le groupe traité, contre 260 (8,7 %) dans le groupe placebo (HR 0,93 ; IC 95 % 0,78-1,11).
Ces résultats sont représentés sous la forme de courbes d'incidence cumulée (Figure 2), et sont retrouvés également dans les différents sous-groupes définis à priori, notamment dans les sous-groupes FEVG (supérieure à 60 % ou inférieure à 60 %), et avec ou sans traitement par iSGLT2 (Table 2).
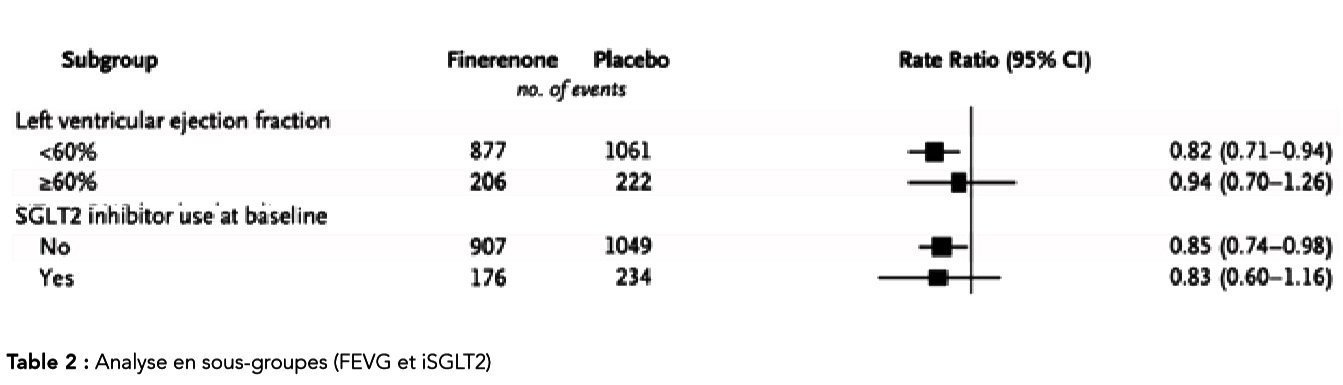
Table 2 : Analyse en sous-groupes (FEVG et iSGLT2).
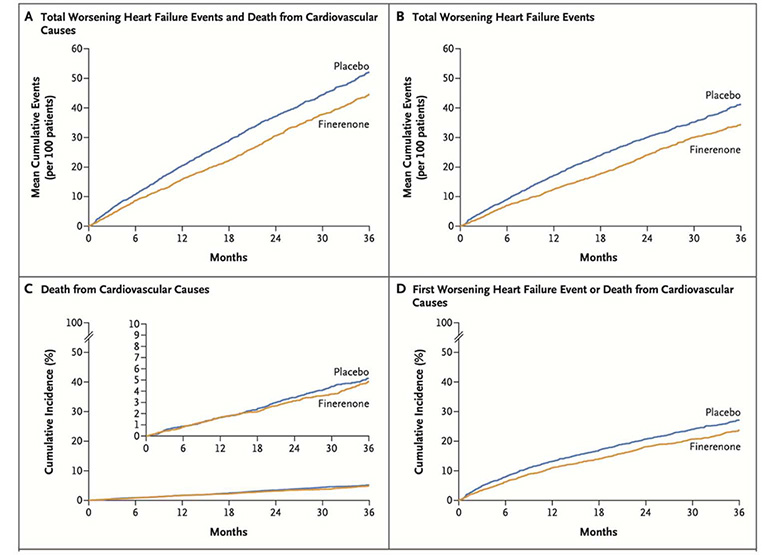
Figure 2 : Courbes d'incidence cumulée du critère de jugement principal et de ses composants
Concernant les critères secondaires, on note :
• Une augmentation moyenne du KCCQ score de 8.0±0.3 dans le groupe Finerenone contre 6.4±0.3 dans le groupe Placebo (difference, 1.6 points ; 95 % CI, 0.8 to 2.3; P inférieure à0.001), soit une différence statistiquement significative.
• Une amélioration de la NYHA chez 557 patients (18.6 %) du groupe Finerenone et chez 553 patients (18.4 %) du groupe placebo (odds ratio, 1.01; 95 % CI, 0.88 to 1.15).
• Survenue du critère composite rénal chez 75 patients (2.5 %) pour le groupe testé de et 55 patients (1.8 %) pour le groupe placebo (hazard ratio, 1.33; 95 % CI, 0.94 to 1.89).
• 491 patients (16.4 %) décédés (toute cause) dans le groupe Finerenone contre 522 patients (17.4 %) dans le groupe placebo (hazard ratio, 0.93; 95 % CI, 0.83 to 1.06).
Concernant l'analyse de sécurité, on remarque :
• Pour les évènements indésirables graves : 1157 patients (38.7 %) pour le groupe Finerenone et 1213 patients (40.5 %) dans le groupe placebo.
• L'absence de décès par hyperkaliémie, avec hospitalisations un peu plus fréquentes pour ce motif dans le groupe testé.
• Enfin fréquence plus importante de la pression artérielle systolique inférieure à 100 mmHg dans le groupe testé sans majoration de l'inobservance thérapeutique.
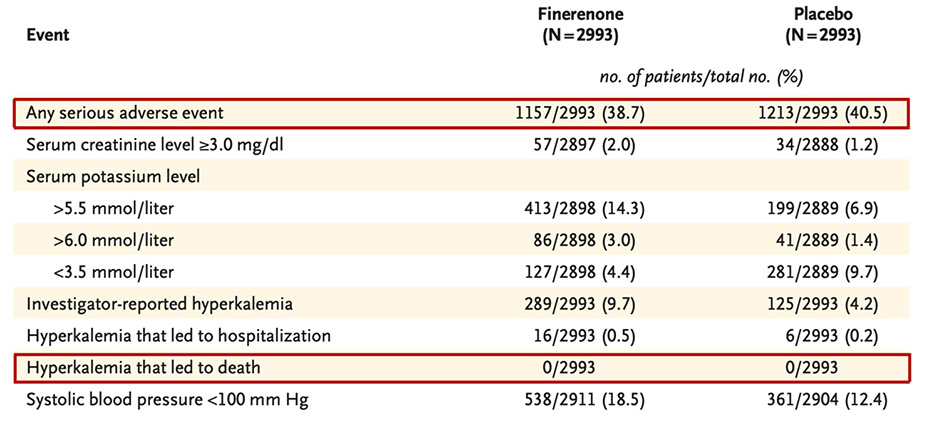
Table 3 : Analyse de sécurité.
Discussion
L'étude FINEART-HF montre que le traitement par FINERENONE diminue significativement la fréquence de survenue du critère de jugement principal composite chez les patients insuffisants cardiaques avec FEVG supérieure à 40 %, quels que soient les différents sous groupes présentés.
Pour les critères secondaires, on retrouve une amélioration modérée du KCCQ, et l'absence d'augmentation de la survenue des évènements indésirables graves, notamment pas d'hyperkaliémie compliquée.
L'étude TOPCAT (5), qui utilisait un schéma similaire avec un antagoniste stéroïdien des écepteurs aux minéralocorticoïdes, n'avait pas, à l'époque, démontré de différence ignificative sur le critère de jugement composite associant le décès d'origine cardiovasculaire, l'arrêt cardiaque ressuscité ou l'hospitalisation pour insuffisance cardiaque. Toutefois, une analyse post hoc avait révélé un effet bénéfique des MRA dans la population nord-américaine.
L'efficacité d'effet de la FINERENONE persiste dans les sous-groupes analysés et en articulier pour le sousgroupe des inhibiteurs du sGLT2, seul traitement validé actuellement pour l'insuffisance cardiaque à FEVG préservée.
Ce travail ne démontre toutefois pas de bénéfice de la finérénone chez les patients insuffisants cardiaques atteints de maladie rénale chronique, contrairement aux données écentes de la littérature qui ont motivé cette étude et qui soulignent l'intérêt des antagonistes des récepteurs aux minéralocorticoïdes chez les patients souffrant d'insuffisance rénale et de diabète de type 2.
Quelques limitations du design de l'étude sont à noter.
Tout d'abord, la faible représentation des patients de couleur, ainsi que le nombre réduit de participants dans certaines analyses de sous-groupes, réduisent la puissance statistique et compliquent l'interprétation des résultats. De plus, les données concernant d'autres molécules de la même classe ne sont pas fournies. Enfin, l'inclusion d'un nombre important de patients avec une FEVG modérément altérée, dont le phénotype est plus proche de celui des patients avec FEVG réduite, pourrait entraîner une surestimation des bénéfices observés.
Messages clés
L'étude FINEARTS-HF a démontré que l'utilisation de la Finerenone dans l'ICFEP et l'IC FEMR, un nouvel ARM induit une :
• Réduction significative du risque de survenue de décès d'origine cardiovasculaire ou d'épisodes d'insuffisance cardiaque ;
• Amélioration de la qualité de vie des patients ;
• Sécurité d'utilisation avec contrôle du risque d'événements indésirables graves.
La Finerenone est donc un nouveau traitement pour la prise en charge de l'ICFEP, en association avec les inhibiteurs des SGLT2.
Auteur

Charles NOGAREDE
CHU de Rouen
Relectrice

Dr Emmanuelle BERTHELOT
CHU Kremlin-Bicêtre Paris, présidente du GICC de la SFC
Références
• Solomon, S. D., McMurray, J. J., Vaduganathan, M., et al. Finerenone in heart failure with mildly reduced or preserved ejection fraction. New Engl J Med 2024.
• Pitt B, Zannad F, Remme WJ, et al. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. N Engl J Med 1999;341: 709-17.
• Zannad F, McMurray JJV, Krum H, et al. Eplerenone in patients with systolic heart failure and mild symptoms. N Engl J Med 011;364:11-21.
• Pitt B, Remme W, Zannad F, et al. Eplerenone, a selective aldosterone blocker, in patients with left ventricular dys- function after myocardial infarction.N Engl J Med 2003;348:1309-21.
• Pitt B, Pfeffer MA, Assmann SF, et al. Spironolactone for heart failure with preserved ejection fraction. N Engl J Med 2014; 370:1383-92.
• Pfeffer MA, Claggett B, Assmann SF, et al. Regional variation in patients and outcomes in the Treatment of Preserved Cardiac Function Heart Failure with an Aldosterone Antagonist (TOPCAT) trial. Circulation 2015; 131:34-42.
• Kolkhof P, Delbeck M, Kretschmer A, et al. Finerenone, a novel sélective nonsteroidal mineralocorticoid receptor antagonist protects from rat cardiorenal injury. J Cardiovasc Pharmacol 2014; 64:69-78.
• Bakris GL, Agarwal R, Anker SD, et al. Effect of finerenone on chronic kidney disease outcomes in type 2 diabetes. N Engl J Med 2020; 383:2219-29.

