Introduction
La maladie de Rendu-Osler (ou télangiectasie hémorragique héréditaire, THH) est une pathologie rare à transmission autosomique dominante, touchant 1 sur 3000 à 5000 habitants, et se caractérisant par une dérégulation de l’angiogenèse responsable de télangiectasies cutanéo-muqueuses et de shunt viscéraux1. Un de ces types de shunt droite/gauche est représenté par les malformations artério-veineuses pulmonaires (MAVP), correspondant à une communication anormale entre une artère pulmonaire et une veine pulmonaire via un sac anévrismal (parfois entre une artère systémique de type bronchique dans 5 % des cas), et sont associées dans 80 % des cas à la télangiectasie hémorragique héréditaire (15 à 33 % des THH ont des MAVP)1.
Malformations artério-veineuses pulmonaires
Les MAVP sont des communications anormales entre une artère pulmonaire et une veine pulmonaire, à haut débit, dans un réseau à faible résistance, responsables d’un shunt gauche/droite3. Elles peuvent être simples (alimentées par une artère segmentaire pouvant donner une ou plusieurs branches) ou complexes (alimentées par plusieurs artères segmentaires ou drainées par plusieurs veines). Dans le cadre de la THH, elles sont le plus souvent multiples, bilatérales, et prédominantes dans les lobes inférieurs. 5 % des patients ont une forme diffuse, correspondant à la présence de MAVP sur toutes les artères segmentaires pulmonaires2.
Clinique
La dyspnée d’effort est modérée et présente uniquement chez la moitié des patients avec un shunt droite/gauche, justifiant un depistage systématique. L’hypoxémie est d’installation progressive2.
Examens complémentaires
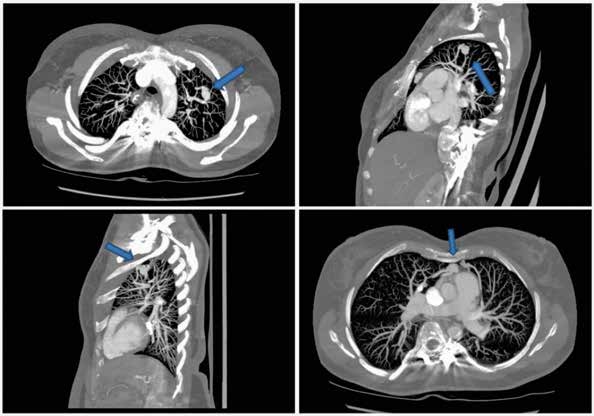
TDM : Le dépistage des MAVP repose sur le scanner thoracique, au mieux avec injection de produit de contraste au temps mixte artériel pulmonaire/systémique, permettant la mise en évidence d’une image nodulaire communiquant avec une artère et une veine pulmonaire. (Figure 1)
Echocardiographie trans-thoracique : Elle permet le dépistage du shunt gauche/droite par injection de solution saline mélangée à une petite quantité d’air dans la circulation veineuse systémique. Le shunt est confirmé si les bulles apparaissent dans le ventricule gauche 4 à 8 cycles cardiaque après l’injection2.
Complications
Neurologiquement, le risque est dominé par l’embolie paradoxale, pouvant être soit à l’origine d’un accident vasculaire cérébral ischémique dans le cadre d’un embol fibrino-cruorique, soit à l’origine d’un abcès dans le cadre d’un embol septique. Ces complications surviennent
en général chez des patients jeunes et peuvent être révélateurs de la maladie.
- Une rupture de MAVP peut être à l’origine selon son site de rupture d’un hémothorax (rupture intra-pleurale) ou d’une hémoptysie (rupture intra-pulmonaire).
Traitement
Le traitement à pour premier but d’éviter les complications des MAVP liées au shunt droite/ gauche, et pour second but d’améliorer l’hématose et la dyspnée d’effort. Toute MAVP dont le diamètre de l’artère afférente est supérieur à 3 mm justifie un traitement (certaines équipes plaçant le cutoff à 2 mm5). La référence est aujourd’hui l’embolisation par voie endovasculaire, qui a supplanté les traitements chirurgicaux (lobectomie, résection atypique).
Procédure d’embolisation
La procédure est réalisée en salle d’angiographie avec capteur monoplan, sous anesthésie locale avec sédation intraveineuse, ou selon le souhait du patient sous anesthésie générale, au mieux par une technique de « Jet-ventilation » permettant de s’affranchir des mouvements respiratoires lors du cathétérisme et donnant plus de confort à l’opérateur.
Il est réalisé en général une session par poumon, espacée d’au moins 1 à 2 semaines. Les patients bénéficient d’une antibioprophylaxie avant le geste, et d’une anticoagulation par héparinothérapie IV en cours de procédure.
L’ensemble des cathéters et micro-cathéters sont utilisés avec un Y à valve relié à des poches de pression pour éviter tout passage d’air dans le système pouvant être responsable d’embolie paradoxale. Une grande rigueur est nécessaire lors des injections de produit de contraste et des rinçages pour éviter tout passage de micro-bulles.
- Ponction de la veine fémorale avec mise en place d’un introducteur 6 French (Terumo®, Tokyo, Japan).
- Cathétérisme du réseau artériel pulmonaire à l’aide d’une sonde de type « Pig-tail » 4 French (Boston Scientific®, Marlborough, MA, USA), mise en place dans le tronc.
- Réalisation de sérigraphies de face, obliques, (6 images/sec) et rotationnelles 3D pour confirmer la présence de MAVP, préciser leurs afférences artérielles et permettre un guidage par des système de Road-map/Smart-mask et Emboguide (Philips®, Amsterdam, Pays-Bas).
- Manoeuvre d’échange sur guide hydrophile 0,035“ Stiff (Terumo®, Tokyo, Japan) et mise en place d’un cathéter Neuronmax 6 French (Penumbra Inc®, Alameda, Californie, USA) pour accroitre la stabilité du système, puis éventuellement mise en place coaxiale d’un microcathéter permettant un cathétérisme distal séléctif de la MAVP
- Les techniques d’embolisation sont multiples : par coils6, historiquement décrite, permet d’occlure le sac anévrismal et de reculer sur l’artère afférente. Le risque est dominé par le passage dans la circulation veineuse pulmonaire d’un coil avec risque d’embolie paradoxale, et par la reperméabilisation à distance de la MAVP.
- En cas de MAVP proximale sur une artère de gros calibre, une embolisation par macroplug peut être réalisée, permettant de tester l’efficacité du système avant un détachement contrôlé.
- En cas de MAVP de petite taille, une embolisation par microplugs peut être réalisée, permettant la même sécurité qu’un macroplug sur des artères de plus petit calibre7
Figure 2 : Artériographie diagnostique au temps artériel pulmonaire.
A - Cathéter « pig-tail » dans l’artère pulmonaire droite, avec mise en évidence de petites MAVP distales dans le lobe supérieur droit, et de deux MAVP dont une volumineuse du lobe moyen.
B - Contrôle final post-embolisation. Embolisation de deux MAVP du lobe supérieur droit par micro-plugs, complètement dévascularisées. Embolisation de la volumineuse MAVP du lobe moyen par coils et macro-plug.
Figure 3 : Traitement d’une reperméabilisation de MAVP embolisée par coils.
A. Reperméabilisation de la MAVP, avec retour veineux précoce.
B - Complément d’embolisation par macro-plug. Contrôle montrant une bonne dévascularisation de la MAVP.
Suivi
En cas de succès de l’embolisation sans complication, un contrôle à 6 mois/1 an par angioscanner thoracique et echocardiographie trans-thoracique peut être réalisé pour vérifier la reperméabilisation ou la bonne occlusion de la MAVP, la présence ou l’absence de nouvelle lésion et la persistance ou l’absence de shunt3.
Conclusion
Les malformations artério-veineuses pulmonaires, présentes principalement dans le cadre de la maladie de Rendu-Osler, sont responsables d’une importante morbi-mortalité justifiant un traitement dès que l’artère afférente est supérieure à 3 mm.
L’embolisation est aujourd’hui le gold standard, avec une importante réussite technique compte tenu du matériel existant et quand elle est réalisée par un opérateur entraîné.
Les patients justifient un suivi au long terme en raison du risque de reperméabilisation à distance.
Références
- Duffau, Lazarro, et Viallard, « Maladie de Rendu-Osler », EMC.
- Khouatra et al., « Malformations artérioveineuses pulmonaires », EMC.
- M.E Faugnan et al, “International guidelines for the diagnosis and management of hereditary haemorrhagic telangiectasia”, J Med Genet. 2011 Feb;48(2):73-87.
- Saboo SS et al, “Pulmonary arteriovenous malformations: diagnosis”, Cardiovasc Diagn Ther. 2018 Jun;8(3):325-337.
- Chamarthy MR et al, Pulmonary arteriovenous malformations: endovascular therapy, Cardiovasc Diagn Ther. 2018 Jun;8(3):338-349.
- Shimoira M et al, “Usefulness of Hydrogel-Coated Coils in Embolization of Pulmonary Arteriovenous Malformations”, Cardiovasc Intervent Radiol. 2018 Jun;41(6):848-855.
- Boatta E, “Pulmonary Arteriovenous Malformations Embolized Using a Micro Vascular Plug System: Technical Note on a Preliminary Experience”.
Article paru dans la revue “Union Nationale des Internes et Jeunes Radiologues” / UNIR N°33

