
« 2024 ESC Guidelines for the management of atrial fibrillation developed in collaborationwith the European Association for Cardio-Thoracic Surgery (EACTS) »
Introduction
Les nouvelles recommandations ESC de 2024 sur la fibrillation atriale apportent des mises à jour depuis 2020. Ces 4 dernières années ont en effet été marquées par l'essor de l'ablation de fibrillation atriale, la multiplication des appareils connectés avec surveillance rythmique, mais surtout par une évolution sociétale mettant en avant le principe d'équité et de prise en charge holistique.
L'article ci-dessous, suit les chapitres de la recommandation et souligne les nouveautés de cette année.
I/ Définition et bilan initial
La fibrillation atriale (FA) est une arythmie supraventriculaire caractérisée par une activation atriale désorganisée sans onde P, objectivée par un électrocardiogramme (ECG) monopiste ou 12 dérivations.
Différentes classifications existent, la plus commune stratifie sur la durée des épisodes (paroxystique, persistante, permanente).
Première nouveauté de ces nouvelles recommandations est l'abandon de la durée minimale de 30 secondes monopiste pour le diagnostic de la FA, durée désormais laissée à l'appréciation du clinicien, ceci en raison de l'augmentation des dispositifs connectés.
Le diagnostic par photo-pléthysmographie, basé sur l'irrégularité du pouls, reste non recommandé.
II/ Prise en charge de la FA : Concept de AF-CARE
Ces nouvelles recommandations introduisent le concept d'AF-CARE. Le classique « ABC » (Anticoagulation, Better control, Comorbidity) est remplacé par « CARE », structurés autour de 4 piliers :
• Comorbidité : identification et prise en charge des comorbidités ;
• Anticoagulation : prévention du risque thromboembolique et gestion du risque hémorragique;
• Réduction des symptômes : contrôle du rythme et de fréquence pour améliorer la qualité de vie ;
• Évaluation et Réévaluation : suivi continue et ajustement des traitements selonl'évolution clinique.
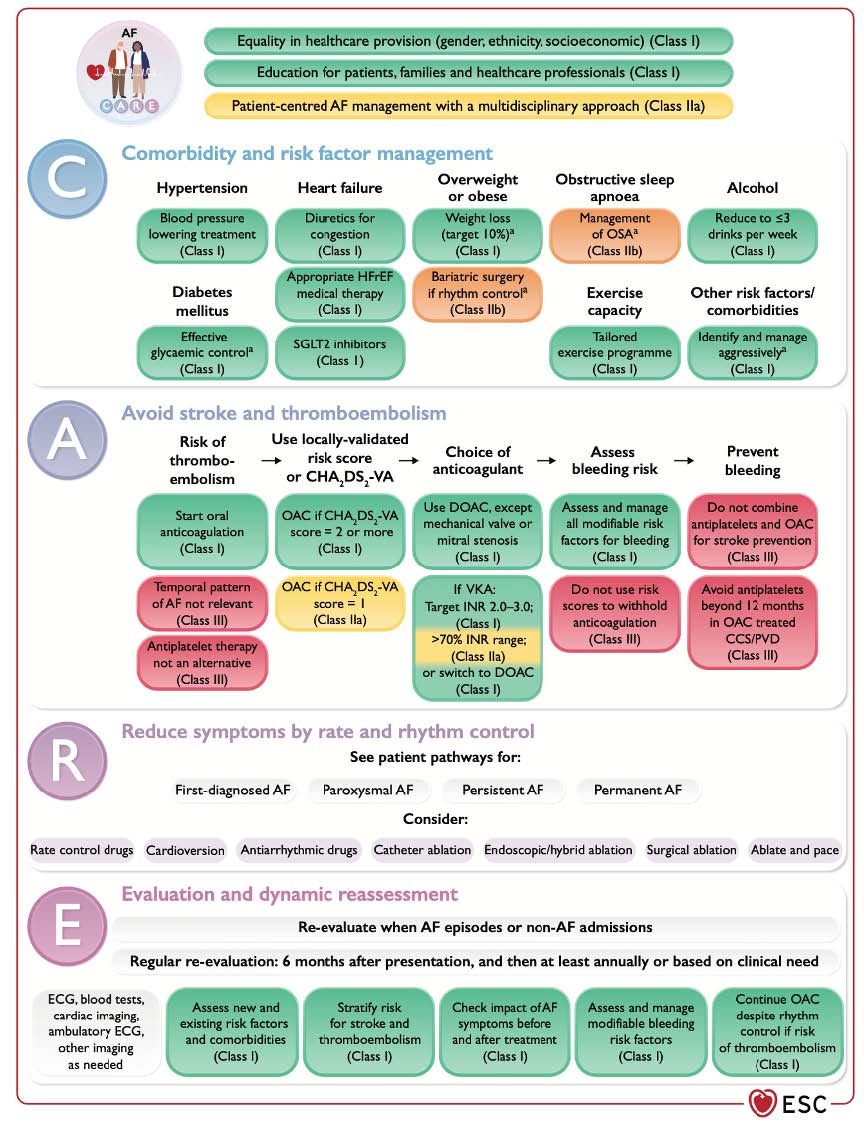
Figure 1 : Résumé de la nouvelle recommandation FA – ESC 2024
II-1/ C pour COMORBIDITÉ à évaluer et prendre en charge
Les comorbidités et facteurs de risques sont le premier pilier de la prise en charge. Trop souvent mis de côté, leur identification et gestion apparait au grade I-B.
La recommandation insiste tout particulièrement sur les 6 facteurs de risques suivants :
• La tension artérielle : en lien avec la nouvelle recommandation HTA 2024) ;
• Le diabète : avec des guidelines elles aussi récemment mis à jour ;
• La gestion de l'insuffisance cardiaque : contrôle de volémie, ISGLT2, traitement de l'ICFER…
• Le surpoids et l'obésité : avec un objectif de perte pondéral ≥ 10 % ;
• L'éthylisme : diminution à 3 unités ou moins par semaine ;
• La sédentarité : à combattre par un programme personnalisé d'activité physique.
Ces six points entrent dans la recommandation au grade I.
De manière plus spécifique, on note le « recul » de la gestion de l'apnée du sommeil (grade IIB-B), avec un dépistage par questionnaire seul désormais déconseillé (grade III-B). Enfin la chirurgie bariatrique entre dans la recommandation si l'IMC ≥ 40 (grade IIB-C).
II-2/ A pour ANTICOAGULATION pour diminuer le risqué d'AVC et d'emboles
La fibrillation atriale constitue un facteur de risque majeur de thrombo-embolie, multipliant par 5 le risque d'AVC ischémique. Le risque « cut-off » est généralement fixé à 0.6-1 % d'évènement embolique annuelle pour que la balance soit favorable à l'introduction d'un traitement anticoagulant.
Pour évaluer ce risque, le score CHA2DS2VASc a été simplifié en CHA2DS2VA (Tableau 1), n'incluant plus le sexe féminin. Les indications d'anticoagulation en cas de FA sont désormais :
• CHA2DS2VA ≥ 2 : Anticoagulation recommandée (grade I).
• CHA2DS2VA = 1 : Anticoagulation recommandée (grade IIA).

En pratique, les indications d'anticoagulation sont les mêmes. La recommandation ouvre la possibilité d'utilisation de score de risque locaux, mais le type d'épisode (paroxystique, persistant, permanent) ne doit pas intervenir dans la prise de décision de prise en charge.
Quelques cas particuliers à connaître : l'anticoagulation est systématique en cas de FA associée à une CMH ou amylose cardiaque (grade I-B).
Enfin, chez les patients avec FA infraclinique (dépisté par matériel endovasculaire ou portatif sans piste ECG) : une anticoagulation peut être débutée si le risque hémorragique est faible (grade IIB-B).
Les anticoagulants oraux directs (AOD) comme l'apixaban, le dabigatran, l'edoxaban et le rivaroxaban sont préférés aux AVK en raison de leur efficacité équivalente et de leur profil de sécurité supérieur, notamment une réduction de 50 % des hémorragies intra-crâniennes. Ils sont contre-indiqués chez les patients avec des valves cardiaques mécaniques ou une sténose mitrale modérée à sévère.
Lors des interventions chirurgicales cardiaques, la fermeture chirurgicale de l'auricule est désormais recommandée comme traitement adjuvant (grade I-B), conformément aux résultats de l'étude LAOOS III.
Cette fermeture doit s'ajouter au traitement anticoagulant et est conseillée lors de procédures endoscopiques ou d'ablation de FA hybride.
En cas de contre-indication à l'anticoagulation, la fermeture de l'auricule par des moyens chirurgicaux dédiés ou interventionnels doit être envisagée au cas par cas (grade IIb-C).
L'évaluation du risque de saignement est essentielle lors de l'initiation de l'AOD. Les facteurs de risque modifiables, tels que l'hypertension, l'alcoolisme et l'utilisation non nécessaire d'antiplaquettaires ou d'anti-inflammatoires, doivent être gérés pour améliorer la sécurité du traitement. Les scores de risque de saignement ne sont pas recommandés pour décider de l'initiation ou de l'arrêt de l'AODs, afin d'éviter une sous-utilisation de l'anticoagulation. Le score HAS-BLED quitte aussi la recommandation.
En cas de saignement, une interruption temporaire des anticoagulants et des interventions spécifiques, telles que l'administration de CCP ou d'antidotes spécifiques pour les AOD, sont recommandées. Une réévaluation et une réintroduction du traitement doit être envisagée après résolution de la cause du saignement, sauf contre-indication absolue.
II-3/ R pour RÉDUCTION DES SYMPTÔMES par contrôle de fréquence et rythme
Le choix d'une stratégie de contrôle de fréquence avecou sans contrôle de rythme est à évaluer et mettre en place dans les 12 mois, en concertation avec le patient (grade IIa). Plutôt que de choisir exclusivement entre le contrôle de la fréquence et le contrôle du rythme, la plupart des patients bénéficient d'une approche combinée, régulièrement réévaluée lors des suivis.
Le contrôle fréquentiel est ainsi essentiel chez tous les patients. L'objectif est de maintenir une fréquence cardiaque inférieure à 110 bpm (grade IIA). Le choix du bradycardisant est guidé par la FEVG : bétabloquant et digoxine si FE < 40 %, et possibilité d'utilisation d'inhibiteur calcique si FE > 40 % (grade I). En cas d'instabilité hémodynamique ou de dégradation sévère de la FEVG, les options thérapeutiques ont été révisées : en plus de l'amiodarone IV (déjà recommandée en 2020), la digoxine, l'esmolol (BREVIBLOC®) et le landiolol (RAPIBLOC ®) peuvent être envisagés (grade IIb-B).
Le contrôle du rythme vise à restaurer et maintenir un rythme sinusal par des interventions telles que la cardioversion, les antiarythmiques, et les ablations par cathéter ou chirurgicales. Il doit être considéré chez tous les patients présentant une fibrillation atriale. La cardioversion électrique est recommandée en urgence pour les patients hémodynamiquement instables. Pour les patients stables, une approche de « wait-and-see » peut être envisagée (grade IIA), permettant une cardioversion spontanée avant d'initier une cardioversion planifiée.
La sécurité prime lors de la cardioversion. Les patients avec une FA non datée ou de plus de 24h (au lieu de 48h précédemment) doivent bénéficier d'une ETO ou recevoir une anticoagulation adéquate pendant au moins 3 semaines avant la cardioversion pour exclure la présence de thrombus auriculaire gauche. Les modalités de cardioversion, qu'elles soient pharmacologiques ou électriques, restent inchangées depuis 2020 : la flécaïnide est préférée si coeur sain, et l'amiodarone si coeur altéré.
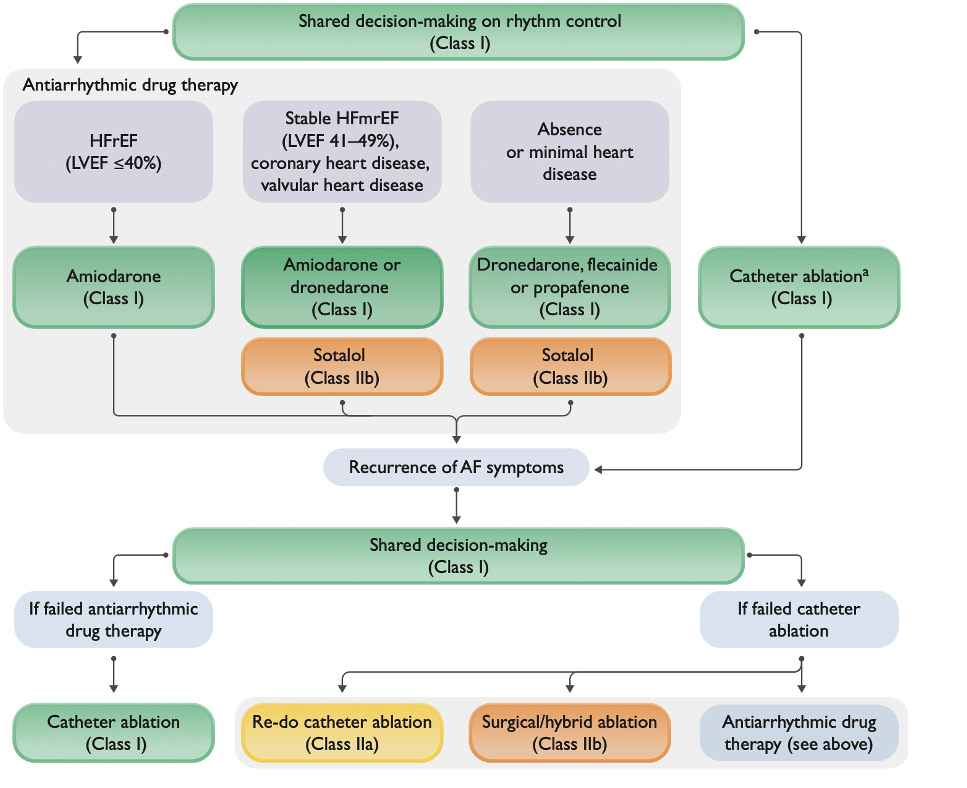
Figure 2 : Contrôle du rythme dans la FA paroxystique
Dans un second temps, se discutera la mise en place d'une stratégie pour maintien de contrôle du rythme par méthode ablative et/ou par anti-arythmique.
On note une refonte des algorithmes de contrôle du rythme selon la « temporalité » de la fibrillation atriale :
• FA Paroxystique : L'ablation est proposée en première intention (grade I-A), équivalente aux antiarythmiques (grade I), selon l'évaluation et les préférences du patient.
• FA Persistante : Les antiarythmiques sont prioritaires (grade I), avec l'ablation réservée aux patients sélectionnés (grade IIb-C) ou en cas de résistance/intolérance aux AA (grade I-A).
Cas particuliers : Indication si suspicion forte de tachycardiomyopathie (grade I), brady-FA ou pause réductionnelle (IIA), et patient à FE altérée (grade IIA).
L'ablation doit être réalisée après 3 semaines d'anticoagulations bien conduite (grade I), sans switch ou interruption durant la procédure (grade IA). On pourra y associer une imagerie additionnelle (ETO ou par scanner cardiaque dédié) chez les patients à haut risque thromboembolique (grade IIa).
Après l'ablation, l'anticoagulation orale doit être maintenue pendant un minimum de deux mois, puis poursuivie en fonction du score CHA2DS2-VA, indépendamment du succès de la procédure (classe I-C).
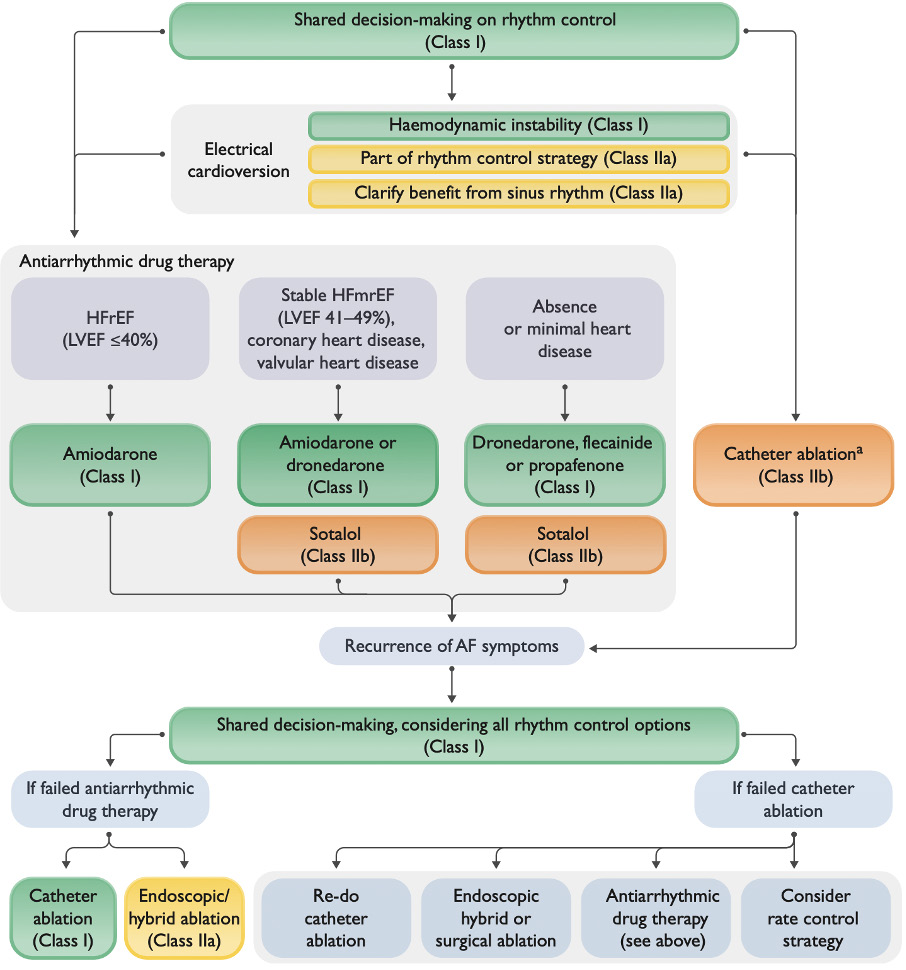
Figure 3 : Contrôle du rythme dans la FA persistante
Les ablations endoscopiques et hybrides, combinant des approches endocardiques et épicardiques, offrent des stratégies avancées pour les patients avec FA persistante ou réfractaire aux traitements médicamenteux.
Ces techniques nécessitent une expertise multidisciplinaire et sont recommandées dans des centres expérimentés pour optimiser les résultats et minimiser les complications.
Chez les patients suivant une stratégie exclusive de contrôle de la fréquence, l'ablation du noeud auriculoventriculaire peut être envisagée en cas de résistance (grade IIa-B). Dans ce contexte, une resynchronisation cardiaque devrait être proposée si le patient a été hospitalisé au moins une fois pour insuffisance cardiaque (grade IIa-B).
II-4/ E pour Evaluation and dynamic reassessment
Le volet [E] de l'AF-CARE englobe les activités nécessaires à l'évaluation des comorbidités et facteurs de risques associés à la fibrillation atriale, guidant le traitement et permettant de fournir une évaluation dynamique.
Le patient mais aussi l'ensemble des acteurs de santé (infirmier, pharmaciens, médecin traitant, cardiologue) doivent contribuer à la prise en charge. De nombreuses études mettent en avant la nécessité d'une meilleure information des professionnelles de santé afin de mieux connaître et appliquer les recommandations.
Le bilan initial de la fibrillation atriale est le suivant :
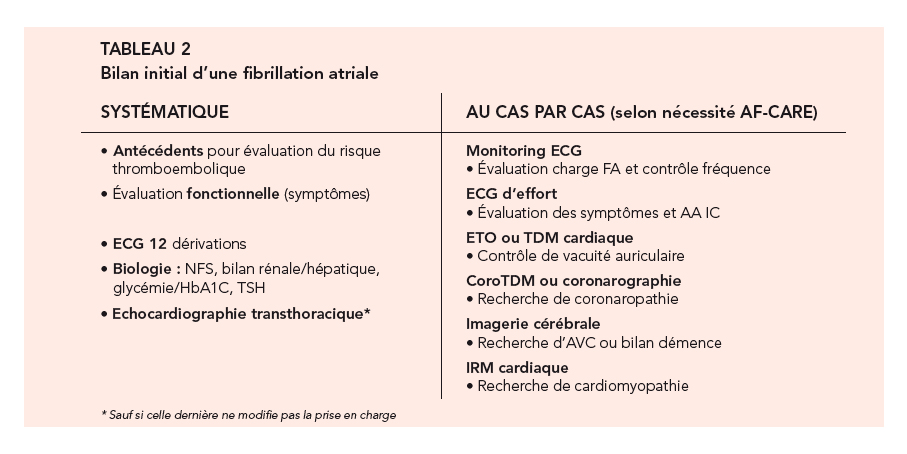
III/ Cas spécifiques
La section 9 des recommandations ESC détaille le parcours AF-CARE dans divers contextes cliniques.
Chez le patient instable hémodynamiquement, la cardioversion électrique urgente est privilégiée, l'amiodarone sera à considérer en seconde ligne. Le contrôle de fréquence par bétabloquant et amiodarone pourrait être similaire dans ce contexte, avec la mise avant ici du landiolol (RAPIBLOC®).
Chez le patient coronarien, la recommandation n'évolue pas. On préfèrera les AOD aux AVK, avec une triple et double thérapie aussi courte que nécessaire. Le clopidogrel est recommandé comme inhibiteur P2Y12.
Chez le patient vasculaire, les AOD seuls sont généralement suffisants, avec une courte durée d'antiplaquettaires post-revascularisation.
Chez le patient cérébrolésé, après un AVC, l'introduction d'une anticoagulation est à déterminer de manière pluridisciplinaire.
Chez le patient facteurs précipitants (infection, alcool, péricardite…), une anticoagulation est conseillée (grade IIa) si le CHADSVA ≥ 2.
Chez le patient postopératoire, il est désormais conseillé d'instaurer une anticoagulation (grade IIa) en cas de FA, que la chirurgie soit non cardiaque, ou cardiaque ce qui est une nouveauté de la recommandation.
Chez le patient avec cardiopathie congénitale, les recommandations ont été simplifiées et stipulent uniquement l'indication d'une anticoagulation en grade IIa, indépendamment du risque thromboembolique.
IV/ Screening
En 2019, 60 millions de personnes sont atteintes de fibrillation atriale. L'incidence double toutes les quelques décennies du fait du vieillissement de la population mais aussi de l'augmentation des facteurs de risques.
Ces dernières années, les outils de détection se sont multipliés et sophistiqués. L'arrivée des techniques d'intelligence artificielle permet le traitement d'un volume de données exponentiel.
Le dépistage de la fibrillation auriculaire (FA) est recommandé dans les situations suivantes :
• Routinièrement lors d'un examen médical chez les patients âgés de 65 ans ou plus, ou présentant des facteurs de risque (grade I).
• Organisé chez les patients âgés de 75 ans ou plus, ou âgés de 65 ans ou plus avec un risque thromboembolique élevé (grade IIa).
• Systématiquement par un monitoring prolongé dans le cadre du bilan d'une embolie cryptogénique (grade I).
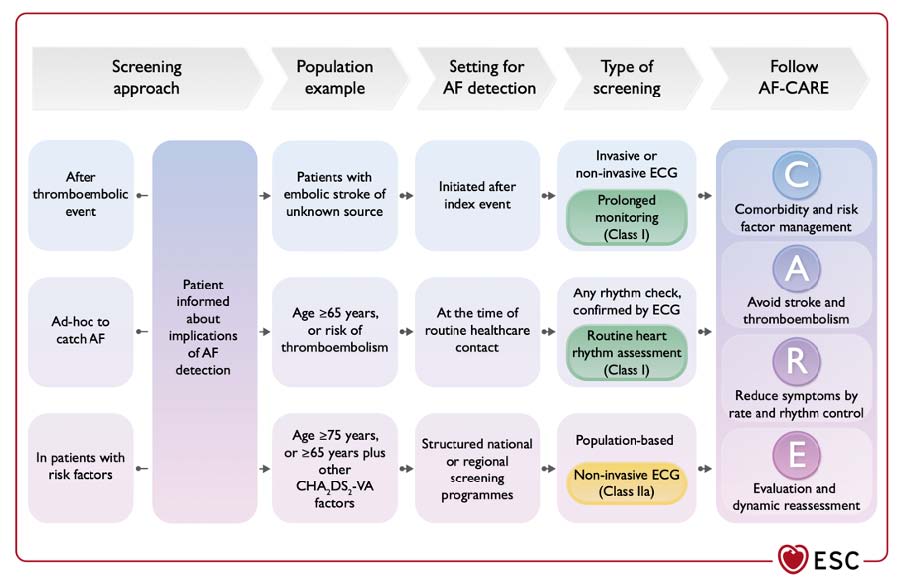
Figure 4 : Indication de dépistage de la fibrillation atriale
En conclusion, cette nouvelle recommandation est surtout une mise à jour des guidelines de 2020.
Ces nouvelles recommandations, intégrant mises à jour et innovations depuis 2020, soulignent l'importance de l'ablation, désormais en première ligne pour la fibrillation atriale paroxystique et en seconde ligne pour la fibrillation atriale persistante. Par ailleurs, le concept d'AF-CARE met en avant la gestion des comorbidités et l'éducation autour de la fibrillation atriale. La prise en charge doit ainsi être multidisciplinaire et centrée sur le patient, reflétant une approche holistique et personnalisée de cette arythmie.
Résumé en 10 points clés à retenir
• La prise en charge de FA doit suivre la méthode AF-CARE (comorbidité, anticoagulation, réduction des symptômes, évaluation).
• Les comorbidités (HTA, insuffisance cardiaque, alcool, sédentarité, surpoids, diabète) doivent être recherchées et prises en charge.
• L'évaluation du risque thromboembolique doit se faire par le score CHA2DS2VA ou équivalent local. Le sexe féminin n'entre plus en compte dans l'évaluation.
• L'anticoagulation doit se faire pour un score ≥ 2 (grade I) ou ≥ 1 (grade IIA), préférentiellemnet par AOD.
• La fermeture d'auricule est recommandée systématiquement en cas de chirurgie cardiaque et fibrillation atriale.
• Le contrôle de fréquence est systématique avec un objectif < 110 bpm obtenu par bétabloquant, digoxine ou inhibiteur calcique selon la FEVG.
• L'ablation de fibrillation atriale entre en première ligne si paroxystique, deuxième ligne si persistante, elle reste indiquée par ailleurs si FE altérée, ou bradyFA.
• L'évaluation initiale doit être répétée pour suivre l'évolution de la maladie, du patient et de ses comorbidités.
• Un patient avec fibrillation atriale sur « facteur précipitant » doit aussi bénéficier d'une anticoagulation si son risque thromboembolique est évalué haut (CHADSVA ≥ 2).
• La prise en charge doit être pluridisciplinaire et inclure l'éducation et la participation de tous les acteurs de santé.
Auteur

Redwane RAKZA
CHU de Rennes
Relecteur

Pr Frédéric SACHER
CHU de Bordeaux,
Président du Groupe
Rythmologie de la SFC

