
Étude OCEAN (1)
Présentation d'une étude multicentrique randomisée évaluant l'Octréotide versus le traitement standard dans les angiodysplasies digestives symptomatiques.
Contexte
L'hémorragie digestive (HD) causée par les angiodysplasies représente 4% des HD hautes (2) avec peu de traitements et dont l'efficacité est limitée à long terme. En effet, environ 1/3 des patients présentent une récidive des saignements dans les deux ans après un traitement par plasma argon (3).
Les angiodysplasies digestives sont des petits vaisseaux tortueux et dilatés dépourvus de couche musculaire lisse situés dans la muqueuse ou la sous-muqueuse digestive.
C'est l'anomalie vasculaire acquise responsable de saignement la plus fréquente. Elles sont responsables d'anémie ferriprive et nécessitent des supplémentations martiales et transfusions régulières malgré les traitements endoscopiques.
La gestion des antiagrégants/anticoagulants, la dépendance en transfusion de culots globulaires (CGR) et en perfusion de fer entraînent une baisse de la qualité de vie ainsi que des coûts de soins importants.
Des études récentes se sont penchées sur l'intérêt des analogues de la somatostatine via leurs propriétés anti-angiogéniques notamment en agissant sur la voie du VEGF et également en diminuant le flux duodénal et splanchnique par vasoconstriction induisant une hypoxie vasculaire, l'amélioration de la fonction plaquettaire et l'augmentation des concentrations d'hémoglobine (4) (5). Mais ces données se basent sur des études rétrospectives avec de faibles effectifs reprises dans une méta analyse (4).
C'est dans ce contexte qu'a été conçue l'étude contrôlée randomisée OCEAN visant à évaluer l'efficacité de l'Octréotide à libération prolongée pour réduire les besoins transfusionnels et en supplémentation martiale chez des patients souffrant d'anémie réfractaire due à des angiodysplasies.
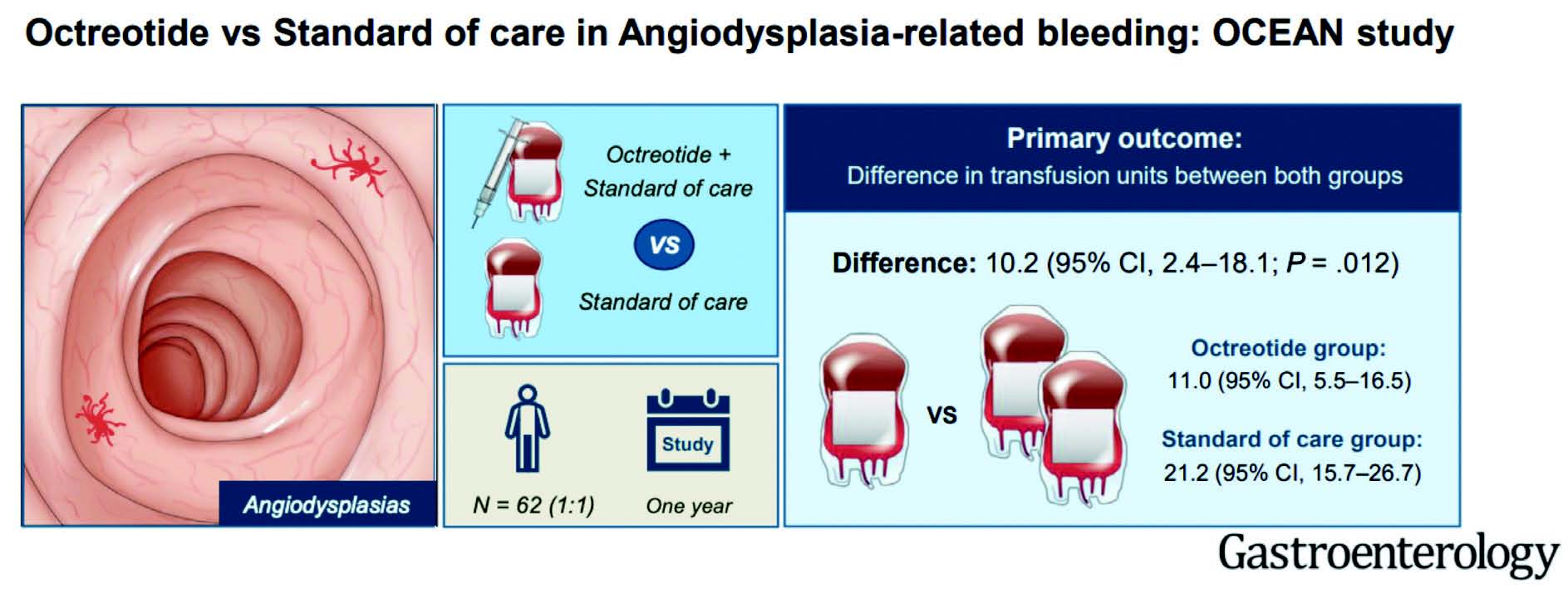
Méthodologie de l'étude
Il s'agit d'une étude de supériorité, contrôlée, randomisée ouverte avec une puissance suffisante pour évaluer l'efficacité de l'Octréotide dans le traitement des angiodysplasies symptomatiques. Elle a été conduite dans 17 hôpitaux hollandais en randomisant 62 patients en 1:1, 31 dans le groupe Octréotide + traitement standard et 31 dans le groupe traitement standard seul (support transfusionnel et supplémentation martiale) et stratifiant en fonction de la prise d'antithrombotique et le type de transfusion (seulement perfusion de fer ou transfusion de CGR). L'essai a été réalisé en aveugle pour le comité d'évaluation des résultats, mais pas pour les patients ni pour les médecins.
Pour être éligible les patients devaient avoir:
• Des angiodysplasies digestives documentées endoscopiquement.
• Une anémie réfractaire aux transfusions (_4/an CGR et/ou en fer).
• Au moins un traitement endoscopique.
Étaient exclus les patients présentant: une cirrhose Child-Pugh C ou une insuffisance hépatocellulaire, un diabète déséquilibré, des symptômes de lithiase biliaire, une pathologie hémorragique ou hématologique héréditaire, un cancer actif, un dispositif d'assistance cardiaque, les femmes enceintes ou allaitantes.
Les patients du groupe Octréotide recevaient 40 mg par voie intramusculaire tous les 28 jours pendant 52_ semaines. Dans les deux groupes, les patients pouvaient en plus recevoir un traitement endoscopique, de l'acide tranexamique ou arrêter des traitements antiagrégants/ anticoagulants si besoin. L'utilisation d'autres traitements antiangiogéniques (ex_ : thalidomide/bevacizumab) était contre-indiquée. Si le médecin jugeait que le traitement standard n'était plus approprié, les patients du groupe de traitement standard pouvaient commencer à prendre de l'Octréotide au cours de l'année d'étude mais cela était considéré comme une violation du protocole et les participants ont été retirés de certaines analyses.
Les patients étaient suivis à S0, S4, S16, S28, S52 et S60 avec un examen clinique, un bilan biologique et l'évaluation des symptômes rapportés par les patients et les infirmières qui administrent l'Octréotide.
La biologie comprenait notamment un bilan hépatique, une glycémie et une hémoglobine glyquée car les effets indésirables les plus connus de l'Octréotide sont l'apparition d'une pathologie lithiasique vésiculaire, un déséquilibre du diabète (inhibition de l'insuline et glucagon), des symptômes digestifs en lien avec une diminution de la sécrétion des enzymes pancréatiques. Une supplémentation était alors introduite en cas de symptômes digestifs.
Le critère de jugement principal était la différence moyenne en nombre de transfusions de CGR et perfusions de fer.
Les critères de jugement secondaires comprenaient_:
• La proportion de patients dans les deux groupes avec réduction de 50 % (définie comme une bonne réponse) et de 100_ % (définie comme une réponse complète) du nombre d'unités de transfusion reçues au cours de l'année d'étude par rapport à la base.
• La proportion de patients ayant besoin de traitements concomitants (ex_ : traitement endoscopique par plasma argon).
• La différence moyenne en nombre de procédures endoscopique entre les 2 groupes.
• La différence moyenne d'épisodes hémorragiques (définis par la réalisation de soins hospitaliers en lien avec l'anémie).
• Le recours aux soins de santé (comprenant les hospitalisations, les soins ambulatoires et les admissions aux urgences).
• L'évaluation du taux d'hémoglobine et de ferritine.
L'étude comportait également des mesures de la fatigue via le questionnaire Multidimensionnal Fatigue Inventory (MFI-20) évaluant 20 items et de la qualité de vie via 36 items du questionnaire Short Form Health Survery (SF-36).
Résultats
Sur les 79 patients éligibles, 62 ont été randomisés (âgé de 72 +/- 11 ans, 32 hommes) de septembre 2015 à avril 2021. La plupart avait au moins une comorbidité (cardiaque, diabète, insuffisance rénale) et 79_ % d'entre eux étaient sous antiagrégant ou anticoagulant.
Les angiodysplasies étaient principalement localisées dans l'intestin grêle (54 sur 62 [87_%]), suivi du côlon (30 [48_%]) et de l'estomac (17 [27_%]).
L'anémie était connue et suivie depuis une période médiane de 6_ans (IQR, 3-10) avec réalisation de 8 procédures endoscopiques (IQR, 7-21,5). Dans l'année avant l'inclusion, les patients ont eu besoin de 20,4 +/- 15.6 transfusions en moyenne et 2,4 +/- 2 procédures endoscopiques.
Le nombre total de transfusion était plus bas dans le groupe Octréotide (11.0; 95_% CI, 5.5–16.5 vs 21.2; 95_% CI, 15.7–26.7) que dans le groupe standard soit une réduction médiane du nombre de transfusion de 10,2 unités (95% CI, 2.4–18.1 ; p=0.012).
On note également une réduction du nombre d'endoscopies annuelles de 0.9 (95_% CI, 0.3–1.5).
Il y avait plus de bonnes réponses au traitement (réduction de 50 % du nombre d'unités de transfusion reçues au cours de l'année d'étude par rapport à la base) dans le groupe Octréotide (61_% vs 19_%) et plus de réponses complètes (réduction de 100_%) (19_% vs 3_%).
Au cours de l'année d'étude, les patients sous Octréotide ont eu moins d'épisodes hémorragiques que les patients sous traitement standard (différence de 3,2 ; 95_%_CI 0,2 - 6,6) et ont moins de recours aux soins de santé. Les taux d'hémoglobine étaient numériquement plus élevés chez les patients sous Octréotide à la fin de l'année d'étude (7,1 [95 %_ CI, 6,6-7,6] mmol/L vs 6,8 [95 %_ CI, 6,3-7,2 mmol/L), tandis que les taux de ferritine étaient comparables entre les groupes. Les patients sous Octréotide semblaient moins fatigués avec une meilleure qualité de vie.
Concernant la sécurité du traitement, sur les 50 effets indésirables recensés chez 22 patients traités par Octréotide (71_ % contre 68_ % dans le groupe traitement standard), 31 sont probablement en lien avec l'Octréotide. Ils comprennent des troubles gastro-intestinaux (19/50) (parmi eux 5 ont reçu une supplémentation en enzymes pancréatiques), des douleurs au site d'injection (9/50), un déséquilibre du diabète (3/50) (parmi eux 2 ont eu besoin de réajuster leur traitement antidiabétique).
Les effets indésirables liés à l'anémie ont été signalés par les patients des deux groupes, en particulier par ceux qui recevaient le traitement standard (14 sur 50 pour le groupe Octréotide contre 27 sur 37 pour le groupe traitement standard).
On note 2 effets indésirables graves dans le groupe Octréotide avec l'apparition d'une angiocholite et une hypoglycémie avec troubles neurologiques (perte de connaissance). Il y a eu 5 décès (16_%) dans le groupe Octréotide (3 d'une cause non en lien avec le traitement, 1 d'un choc hémorragique, et 1 d'une cause inconnue) vs 2 (6_%) dans le groupe standard.
En analyse per protocole avec ajustement des covariables, 23 patients sous Octréotide ont nécessité un nombre moyen de 8,7 (95_%_CI, 2,4-15,1) unités de transfusion, contre 21,5 (95 %_CI, 15,8- 27,3) unités de transfusion pour 28 patients recevant le traitement standard. L'Octréotide a réduit le nombre d'unités de transfusion de 12,8 (95 %_CI, 4,2-21,4) unités.
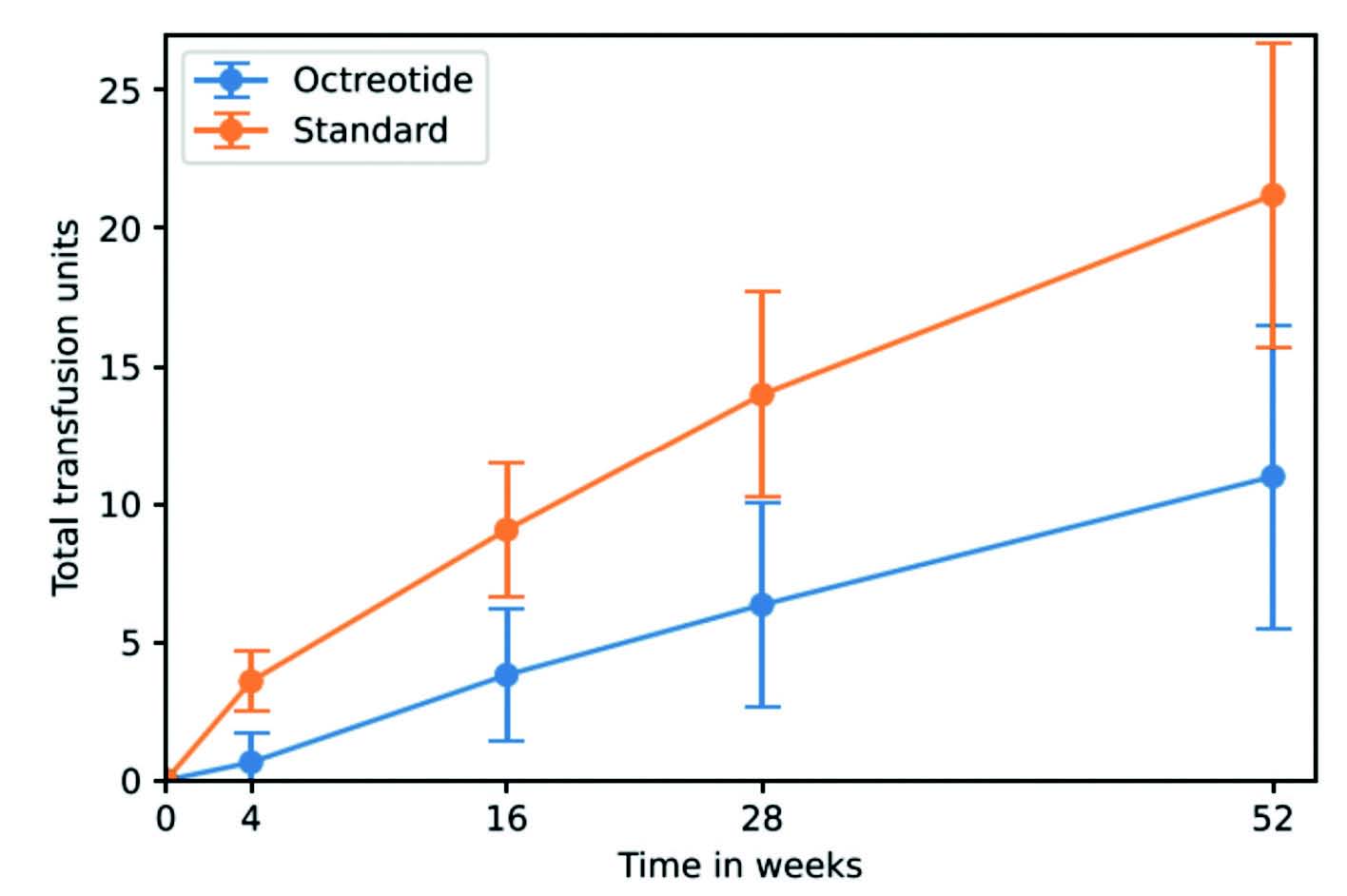
The mean number of transfusion units patients in the octreotide group and standard of care group received during the study is shown. The difference in transfusion units between groups was unrelated to the treatment duration (P = .76). The error bars indicate the standard deviation.
Discussion
Cet essai randomisé, multicentrique montre que l'Octréotide est supérieur au traitement standard pour réduire les besoins transfusionnels des patients suivis pour anémie réfractaire liée à des angiodysplasies. L'amélioration est rapide dès le premier mois et a persisté de façon constante pendant l'année de l'étude. Les patients sous Octréotide ont une qualité de vie globalement meilleure.
Les effets indésirables liés à l'Octréotide sont fréquents (65 %) mais rarement sévères.
D'après ces résultats, l'Octréotide devrait faire partie de l'algorithme de traitement des angiodysplasies gastro-intestinales, ce qui est en adéquation avec la littérature existante.
Parmi les limites, on note que les patients et les médecins n'étaient pas en aveugle sur le traitement délivré. Cinq patients du groupe standard ont reçu de l'Octréotide durant l'étude. Les traitements concomitants, et notamment l'utilisation de plasma argon par voie endoscopique, étaient plus utilisés dans le groupe standard pouvant entraîner des résultats biaisés.
Une analyse ajustée sur les traitements concomitants montre une différence en besoins transfusionnels plus importante entre les deux groupes (différence de 10,2 dans l'analyse principale et 16,4 dans l'analyse ajustée). Malgré la randomisation, les patients du groupe Octréotide avaient plus de transfusions dans l'année avant l'inclusion (22,6 vs 18). Des analyses de covariance ont été réalisées pour contrôler cette différence. Comparativement aux autres études, les patients étaient traités avec une forte dose d'Octréotide, mais une méta analyse antérieure n'a pas objectivé de lien entre la dose et l'effet thérapeutique mais les effets indésirables étant plus fréquents avec des doses plus importantes_(4).
Conclusion
• L'Octréotide est supérieur au traitement standard pour la réduction du besoin transfusionnel.
• Le bénéfice est visible dès le premier mois et persiste tout le long de l'étude.
• L'Octréotide permet également une diminution des épisodes de saignement, de recours aux soins, des procédures endoscopiques, améliore la qualité de vie avec moins de fatigue avec un impact sur la santé mentale.
• Les effets indésirables sont tolérables et de faible intensité.
• L'Octréotide peut donc être utilisé dans le traitement des anémies réfractaires secondaires aux saignements sur angiodysplasies digestives.
Inès LEVEQUE
Un grand merci au Dr Morgane STOUVENOT
(Service de Gastro-entérologie, CHU de Besançon) pour sa relecture et ses corrections.
Bibliographie
1. Goltstein LCMJ, Grooteman KV, Bernts LHP, Scheffer RCH, Laheij RJF, Gilissen LPL, et al. Standard of Care Versus Octreotide in Angiodysplasia-Related Bleeding (the OCEAN Study): A Multicenter Randomized Controlled Trial. Gastroenterology. avr 2024;166(4):690-703.
2. Moretó M, Figa M, Ojembarrena E, Zaballa M. Vascular malformations of the stomach and duodenum: an endoscopic classification. Endoscopy. nov 1986;18(6):227-9.
3. Jackson CS, Gerson LB. Management of gastrointestinal angiodysplastic lesions (GIADs): a systematic review and meta-analysis. Am J Gastroenterol. avr 2014;109(4):474-83; quiz 484.
4. Goltstein LCMJ, Grooteman KV, Rocco A, Holleran G, Frago S, Salgueiro PS, et al. Effectiveness and predictors of response to somatostatin analogues in patients with gastrointestinal angiodysplasias: a systematic review and individual patient data meta-analysis. Lancet Gastroenterol Hepatol. nov 2021;6(11):922-32.
5. Aslam M, Idrees H, Ferdinandy P, Helyes Z, Hamm C, Schulz R. Somatostatin Primes Endothelial Cells for Agonist-Induced Hyperpermeability and Angiogenesis In Vitro. Int J Mol Sci. 13 mars 2022;23(6):3098.

