Rappels d’embryologie
Le septum inter-atrial se forme à partir de 3 structures qui vont fusionner :
• Septum primum (SeP) : représente la première partie de la cloison inter-atriale, il descend du toit de l’oreillette,
• Epine vestibulaire : (origine mésenchymateuse) vient de plus bas et avance vers l’avant. En bas et en avant se situent les bourgeons du canal atrio-ventriculaire,
• Septum secondum (SeS) : descend également du toit de l’oreillette.
4 Types anatomiques de CIA
CIA ostium secundum (OS)
- 75 % des CIA découvertes à l’âge adulte, avec des localisations et tailles et morphologies variées.
- Située en plein dans le septum inter-atrial. au niveau de la fosse ovale.
- Liée à l’absence de fermeture de l’ostium secondum (situé dans le septum primum).
- Elle est très bien visible en échographie cardiaque en quatre cavités, parasternal petit axe ou sous-costal. Le shunt couleur gauche-droit est mieux visible en petit axe ou sous-costal car en 4 cavités, le flux est souvent perpendiculaire au shunt et plus difficile à voir. Il est important d’identifier la présence de rebords lorsqu’on envisage une fermeture percutanée, surtout en postérieur et inférieur.
CIA ostium primum (OP)
- 15 % des CIA de l’adulte.
- Correspond à la CIA sur canal atrio-ventriculaire (CAV).
- Le diagnostic est posé sur la coupe 4 cavités où on visualise un alignement des valves mitrale et tricuspide dans le même plan (absence de décalage mitro-tricuspidien) et une communication inter-auriculaire antérieure et basse, collée aux valves AV.
Il s’y associe une fente de la valve mitrale au niveau de son feuillet antérieur pouvant se compliquer d’une insuffisance mitrale plus ou moins importante.
CIA sinus venosus
- 10 % des CIA de l’adulte.
- Associée à un retour des veines pulmonaires anormal (RVPA) qu’il faudra toujours rechercher en pratique !
CIA du sinus coronaire
- Rare.
- Secondaire à un défaut de formation du toit du sinus coronaire avec pour conséquence un abouchement partiel ou total du sinus coronaire dans l’oreillette gauche permettant un shunt gauche-droit au travers de ce sinus coronaire perforé (unroofed coronary sinus).
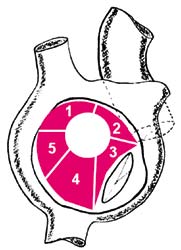
Quatre types anatomiques de CIA
Schéma du Dr. Roux
Physiopathologie
Le débit de shunt au travers d’une CIA dépend de la taille de la CIA et du régime de pressions. Une large CIA entraine une égalisation des pressions entre les deux oreillettes, et un shunt gauche-droit préférentiel en raison d’une compliance ventriculaire droite plus importante. De ce fait, toutes les conditions qui entraînent une augmentation de pression dans l’OG (cardiopathie hypertrophique, rétrécissement mitral) vont majorer le shunt gauche-droit par la CIA. A l’inverse, les conditions qui diminuent la compliance ventriculaire droite, comme une hypertension pulmonaire importante, une sténose pulmonaire ou tricuspide peuvent inverser le shunt qui deviendra droit-gauche.
Un shunt est considéré comme significatif lorsque le Qp/Qs (rapport entre le débit systémique et le débit pulmonaire) est supérieur à 1.5 ou lorsqu’il entraîne une dilatation des cavités droites.
Diagnostic clinique / ECG / RXT
Cliniquement, une CIA donne un souffle systolique au foyer pulmonaire, avec un dédoublement fixe du B2, correspondant à l’hyperdébit pulmonaire. Rarement, il s’y associe une dyspnée d’intensité variable, parfois tardive lorsqu’il existe une hypertension pulmonaire. Il faut également penser au shunt atrial en cas de troubles du rythme supra-ventriculaire (FA/flutter/TAF) à un âge jeune (vers 30-40 ans).
L’ECG peut montrer des signes de surcharge atriale et ventriculaire droite (axe droit, BBD, hypertrophie VD), et les troubles du rythme supra-ventriculaires décrits. Il est à noter qu’en cas de BAV 1 associé il faut penser à la forme familiale associée à une mutation du gène NKX 2.5.
La radiographie thoracique peut montrer : cardiomégalie par dilatation des cavités droites, avec une saillie du bord inférieur droit (OD) et de l’arc moyen gauche (AP), ainsi qu’une hypervascularisation pulmonaire.
Diagnostic ETT
L’ETT permet d’affirmer le diagnostic (type anatomique, mesure des berges si CIA OS), d’apprécier le retentissement (dilatation des cavités droites, mesure éventuelle du Qp/Qs) et la sévérité (présence d’une hypertension pulmonaire), ainsi que de guider la prise en charge (fermeture percutanée ou chirurgicale).
L’ETO est précieuse pour préciser l’anatomie de la CIA, rechercher un RVPA associé mais est surtout utilisée au cours de la procédure de fermeture percutanée de CIA ostium secundum.
Apport de l’IRM
L’IRM est l’examen de référence pour la mesure de la taille du ventricule droit et l’évaluation de sa fonction. C’est aussi l’examen de choix pour éliminer une anomalie des retours veineux pulmonaires associée. Pour les patients contre-indiqués à l’IRM, le scanner ou le cathétérisme cardiaque peuvent apporter les informations manquantes à l’échocardiographie.
Prise en charge par cathétérisme interventionnel ou chirurgie
La prise en charge par cathétérisme interventionnel ou chirurgie sous CEC dépend du type de CIA. Les CIA OS isolées, quand l’anatomie le permet, doivent être fermées par voie percutanée. Toutes les autres formes de CIA sont fermées chirurgicalement. Il faut noter que la CIA entraine un sur-risque de mortalité, qu’elle ait été fermée ou non, mais sa fermeture permet de diminuer ce risque sans pour autant le rendre égal à celui de la population générale.
La fermeture percutanée des CIA ostium secundum est réalisée par voie veineuse fémorale, au moyen d’une prothèse à double disque. Plusieurs conditions anatomiques de ces CIA OS sont requises, notamment [diamètre de CIA maximal + 14 mm] < longueur totale du SIA (mesurée en apical 4 cavités), des berges de CIA > 5mm (facultatif en rétro-aortique) et si possible un septum non floppy (en effet, sur un rebord très souple, très anévrysmal, la prothèse peut ne pas tenir et il existe alors un risque embolique). Le geste est suivi d’une anti-agrégation plaquettaire de 6 mois minimum, durée nécesssaire pour une endothéliatation complète de la prothèse. La fermeture percutanée des CIA OS isolée a montré une nette supériorité par rapport à la chirurgie. Les complications sont rares, et par argument de fréquence : hématome au point de ponction, embolie ou lésion rétro-aortique (dans le cas de CIA très larges avec des tailles de prothèses > 40 mm).
La fermeture chirurgicale peut se faire par sternotomie médiane classique, thoracotomie sous-mammaire droite (préférée chez l’adolescente ou la femme adulte) ou postéro-latérale droite. Elle s’adresse à tous les types de CIA.
Il faut noter qu’une CIA OS avec une dilatation de l’anneau tricuspide doit elle aussi être fermée par voie percutanée. Il a été montré une diminution spontanée du diamètre de l’anneau après fermeture.
Quelles indications de fermeture ?
- CIA symptomatiques avec surcharge ventriculaire droite et des RVP (résistances vasculaires pulmonaires) < 5 UW (classe IB).
- CIA avec Qp/Qs > 1,5 (mesuré en écho, IRM ou par cathétérisme cardiaque) avec RVP < 5 UW ou RVP > 5UW mais PAP < 2/3 pressions systémiques ou RVP < 2/3 RVS (résistances systémiques) (classe IIB).
- Embolie paradoxale et/ou syndrome platypnéeortodéoxie (classe IIa).
La présence d’une hypertension pulmonaire fixée, secondaire (syndrome d’Eisenmenger) ou non à la CIA est une contre-indication absolue à la fermeture de la CIA.
Histoire naturelle de la CIA et risque rythmique
Les CIA retentissantes sont associées à une augmentation de la morbi-mortalité. Néanmoins, les patients dont le shunt est refermé avant l’âge de 25 ans, ont une survie égale à celle des patients sans CIA.
La prévalence d’une arythmie supra-ventriculaire droite augmente progressivement après l’âge de 11 ans du fait de la dilatation de l’oreillette droite, et est présente chez 52 % des patients après 60 ans. Le risque relatif de flutter auriculaire ou fibrillation auriculaire (FA) en post-opératoire est plus important après 40 ans. A l’inverse, ce risque de flutter, FA ou dysfonction sinusale est quasi-inexistant lorsque la CIA est refermée dans l’enfance ou adolescence.
L’aptitude aérobie est modérément diminuée en présence d’une CIA (médiane de la VO2 pic à 75 % de la théorique). Une étude a montré une amélioration d’environ 15 % de la VO2 pic à 6 mois après la fermeture percutanée de CIA, indépendamment de la taille de la CIA ou de l’âge.
Cas particulier de la CIA du sujet âgé ou « CIA vieillie »
La découverte d’une CIA avec dilatation des cavités droites chez le sujet âgé présentant une dyspnée doit amener à la fermeture du défaut septal car elle permet l’amélioration de la symptomatologie et l’amélioration du pronostic à long terme. Après 40 ans, la fermeture de la CIA ne diminue pas le risque d’arythmie supra-ventriculaire. Ainsi, il est important de discuter chez le sujet âgé de l’opportunité d’un geste d’ablation par radiofréquence avant la fermeture percutanée de la CIA.
CIA et Grossesse ?
Les CIA sont habituellement bien tolérées pendant la grossesse. Un suivi cardiologique est néanmoins nécessaire devant le risque d’embolie paradoxale, d’AVC, d’arythmie ou d’insuffisance cardiaque. Idéalement, la CIA doit être fermée avant la grossesse pour diminuer ce risque.
Conclusion
Dès que le diagnostic de CIA retentissante est posé, celle-ci doit être fermée, de préférence par voie percutanée si l’anatomie le permet. La fermeture percutanée précoce a grandement amélioré la survie à long terme de ces patients. Une CIA, même fermée, nécessite un suivi prolongé avant le développement de complication.
Référence
- Atrial septal defects in the adult: recent progress and overview. Webb G, Gatzoulis MA. Circulation. 2006 Oct 10;114(15):1645-53.
- ACC/AHA 2008 Guidelines for the Management of Adults with Congenital Heart Disease: Executive Summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Webb GD et al. Circulation. 2008 Dec 2;118(23):2395-451. doi: 10.1161.
- Grown-Up Congenital Heart Disease (Management of). ESC Clinical Practice Guidelines 2010
Article paru dans la revue “Collèges des Cardiologues en Formation” / CCF N°6

