Introduction
L'étude RHEIA a été présentée par le Pr Hélène Eltchaninoff (co-investigatrice principale avec le Dr Didier Tchétché) lors du congrès de l'ESC 2024 à Londres. L'objectif de l'étude RHEIA était de comparer le TAVI utilisant une valve expandable par ballonnet à la chirurgie dans une population exclusivement féminine.
Rappel des recommandations concernant le rétrécissement aortique
Le rétrécissement aortique (Rac) serré se définit selon les recommandations ESC 2021(1) sur les valvulopathies par des critères échocardiographiques :
• Vitesse maximale en doppler continu (Vmax) inférieure à 4 m/s ;
• Gradient moyen transvalvulaire en doppler continu (Gmoy) supérieure à 40 mmHg ;
• Surface inférieure à 1 cm2 ou inférieure à 0,6 cm2/m2.
Il existe dans ce cas, si le patient est symptomatique (ou présente des symptômes lors d'une épreuve d'effort), une indication de grade IB à une intervention percutanée ou chirurgicale.
Dans le cas d'un Rac bas débit-bas gradient (Gmoy inférieure à 40 mmHg et S inférieure à 1 cm2, Stroke volume indexé ou Svi inférieure à 35 mL/m2), plusieurs situations se présentent :
• La FEVG est altérée (inférieure à 50 %) et il existe une réserve contractile (on objective en échographie-dobutamine un gradient moyen supérieur à 40 mmHg) : il existe une indication d'intervention de grade IB ;
• La FEVG est altérée (inférieure à 50 %), il n'existe pas de réserve contractile en échographie de stress : il existe une indication à réaliser un score calcique valvulaire (SCV) ; - SCV supérieure à 1200 (femme) ou supérieure à 2000 (homme) : indication d'intervention de grade IIa.
• La FEVG est préservée (supérieure à 50 %) et l'échographie-dobutamine n'a pas d'intérêt. Si le score calcique valvulaire est SCV supérieure à 1200 (femme) ou supérieure à 2000 (homme) : indication d'intervention de grade IIa.
Concernant les patients asymptomatiques, il existe - outre les critères de l'épreuve d'effort décrits ci-dessus - certaines indications d'intervention devant un Rac serré avec des paramètres échocardiographiques de gravité :
• Présence d'une dysfonction VG (FEVG inférieure à 50 %) (grade IB) ;
• Présence d'une dysfonction VG débutante (FEVG inférieure à 55 %) sans autre cause (grade IIa) ;
• Vmax supérieure à 5 m/s (grade IIa) ;
• Gradient moyen supérieure à 60 mmHg (grade IIa) ;
• Calcifications aortiques sévères et progression de la Vmax supérieure à 0,3 m/s/an (grade IIa).
Enfin, devant un patient asymptomatique avec Rac serré, une diminution de la tension artérielle à l'effort de 20 mmHg ou une élévation du BNP de plus de trois fois la norme pour l'âge mènera à une prise en charge avec une recommandation de grade IIa.
Les recommandations de l'ESC nous indiquent des modalités de prise en charge différentes selon l'âge et le risque chirurgical du patient :
• Remplacement valvulaire chirurgical si patient de moins de 75 ans à faible risque chirurgical
(EuroSCORE II inférieure à 4 %) ;
• Remplacement valvulaire chirurgical si un critère parmi : indication de pontage aortocoronaire, chirurgie de valve ou intervention sur l'aorte ;
• TAVI par voie fémorale si patient de 75 ans ou plus, EuroSCORE II supérieure à 8 % ou patient inopérable.
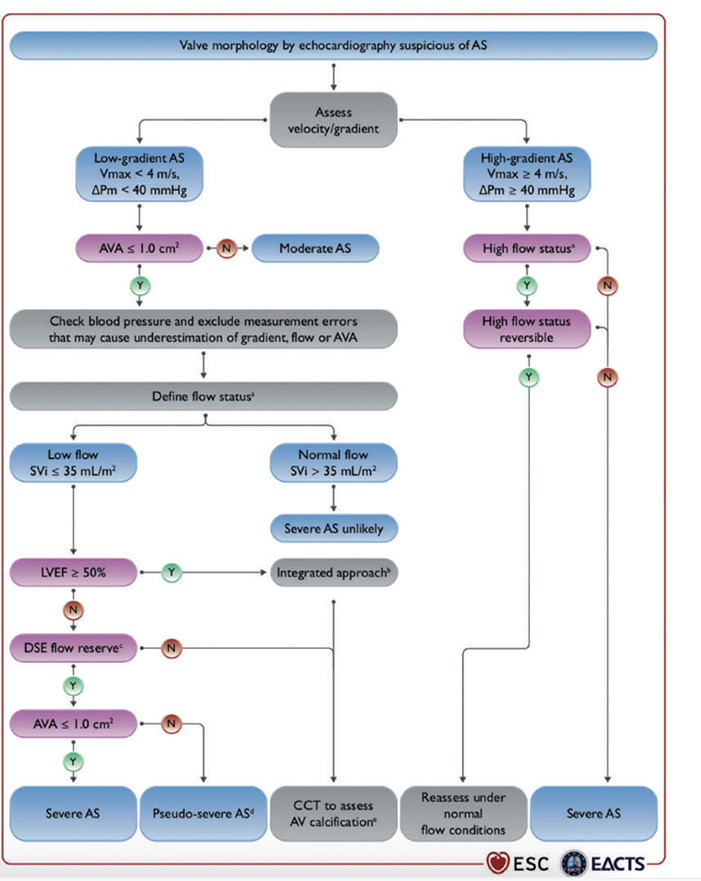
Figure 1 : Algorithme diagnostic concernant la sévérité d'un rétrécissement aortique proposé par les recommandations valvulopathies de l'ESC 2021
Les recommandations américaines de 2020 (2) de leur côté sont plus permissives avec le TAVI :
• Patient de moins de 65 ans ou espérance de vie de plus de 20 ans : option chirurgicale privilégiée ;
• Patient âge de 65 à 80 ans : option chirurgicale ou percutanée selon la décision de la Heart team ;
• Patient de plus de 80 ans : TAVI à privilégier.
Contexte de l'étude
Le remplacement valvulaire aortique percutané (TAVI) est désormais une alternative sure et efficace au remplacement valvulaire aortique chirurgical pour la prise en charge du rétrécissement aortique sévère (1), quel que soit le risque chirurgical (2).
Les analyses en sous-groupes des récentes études s'étant intéressées aux patients à bas risque suggèrent un bénéfice supérieur chez les femmes (3), notamment dans l'essai PARTNER-3 qui a comparé le TAVI avec valve expandable par ballonnet à la chirurgie chez des patients à bas risque(4). Cependant, le nombre de femmes dans ces études était souvent faible, ne permettant pas d'obtenir une puissance statistique suffisante (uniquement 30 % de femmes dans l'étude PARTNER-3 par exemple).
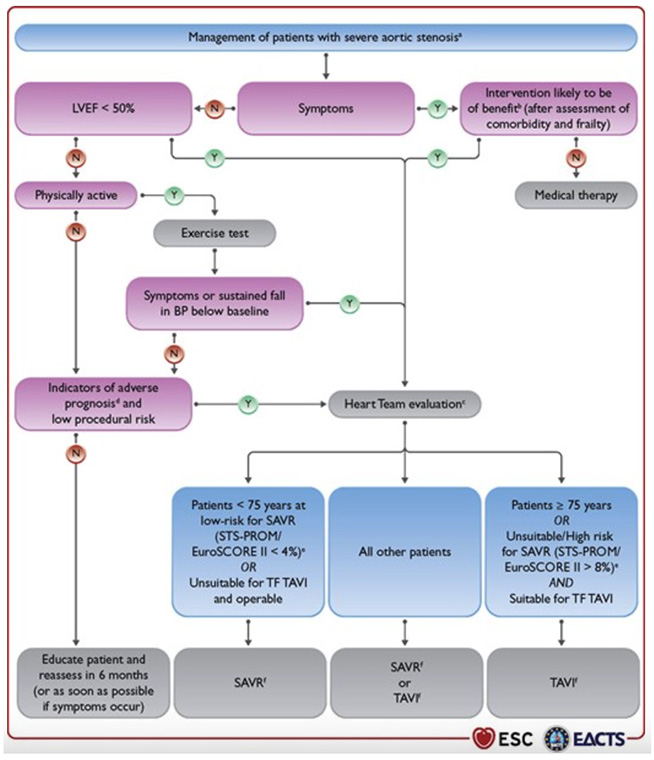
Figure 2 : Algorithme de prise en charge du rétrécissement aortique serré selon les recommandations valvulopathies de l'ESC 2021
Méthode
Il s'agit d'un essai contrôlé randomisé ayant inclus exclusivement des femmes avec rétrécissement aortique sévère, quel que soit leur risque chirurgical et qui étaient randomisées TAVI (valve Sapien 3 ou Sapien 3 Ultra) ou chirurgie (valves commercialement disponibles). Les patientes avec une valve bicuspide ou une maladie coronaire complexe
étaient exclues. Le critère de jugement principal était le critère composite à 1 an de la ortalité toute cause, des AVC et des réhospitalisations pour une cause en rapport avec la valve, la procédure ou pour insuffisance cardiaque.
Résultats
Au total, 443 patientes ont été inclues dans 48 centres répartis dans 12 pays en Europe (âge moyen de 73 ans, STS score 2.1 %, petit anneau aortique chez 75 % des patientes). La majorité des patientes du groupe TAVI a été traitée avec une valve de 23 mm, alors que les tailles les plus couramment utilisées dans le roupe chirurgie étaient de 21 et 23 mm.
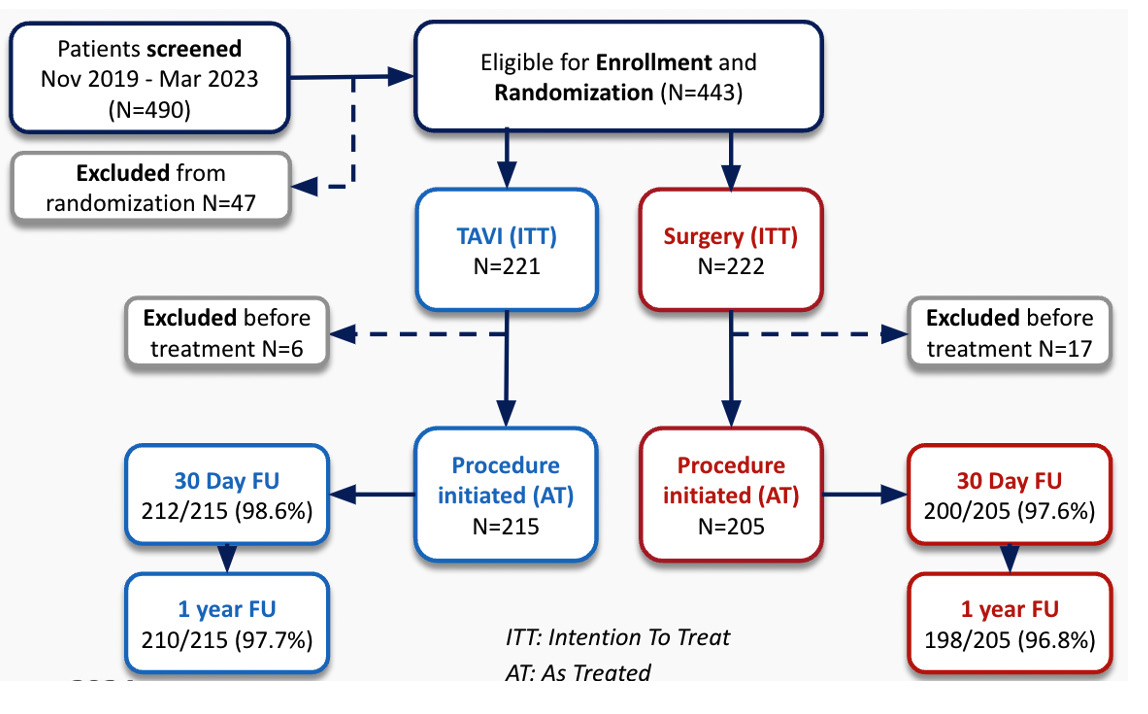
Figure 3 : Flow-chart de l'étude RHEIA
À 1 an, l'incidence du critère de jugement principal a été significativement plus faible dans le groupe TAVI (8,9 %) que dans le groupe chirurgie (15,6 %) (hazard ratio (HR) 0,55, intervalle de confiance à 95 % [0,34-0,88], p=0,03).
La différence de risque absolu entre les deux groupes de -6,8 % et la borne supérieure de l'intervalle de confiance permettent de confirmer la non-infériorité mais aussi la supériorité du TAVI par rapport à la chirurgie dans cette analyse.
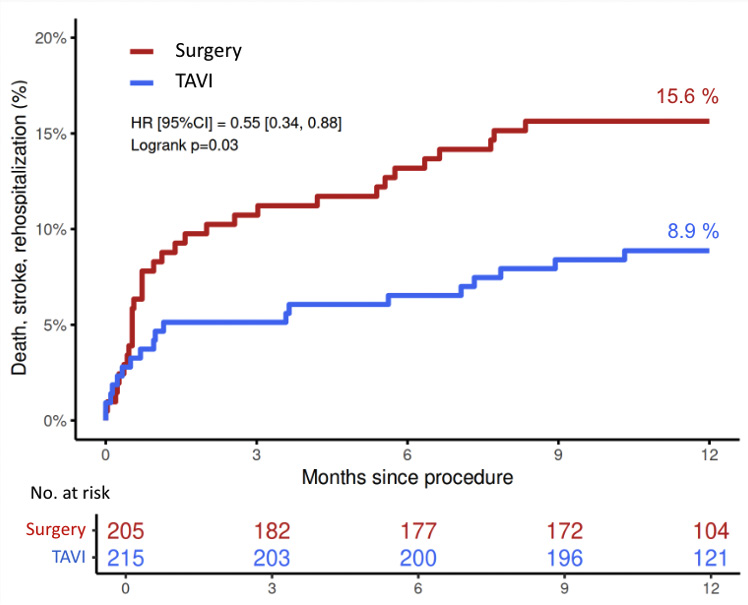
Figure 4 : Résultats de l'étude RHEIA sur le critère de jugement principal.
L'analyse individuelle des composants du critère principal ne retrouve pas de différence entre les deux groupes sur la mortalité et les AVC. En revanche, le taux de réhospitalisations à 1 an était significativement plus faible dans le groupe TAVI (4.8 %) comparé au groupe chirurgie (11.4 %, p=0.02).
La procédure TAVI a été associée à une plus faible incidence de fibrillation atriale que la chirurgie à 1 an (3.3 % vs. 28.8 %, respectivement ; p inférieure à 0.001) et une durée d'hospitalisation réduite (4 jours vs 9 jours). 90 % des patients sont rentrés directement à domicile après un TAVI contre 49 % après chirurgie. On observe cependant un taux plus élevé de pacemaker (8.8 % vs. 2.9 %, respectivement ; p=0.01) et de fuites paravalvulaires modérées (mild) à un n (15.5 % vs. 2.4 %, respectivement ; p inférieure à 0.001)
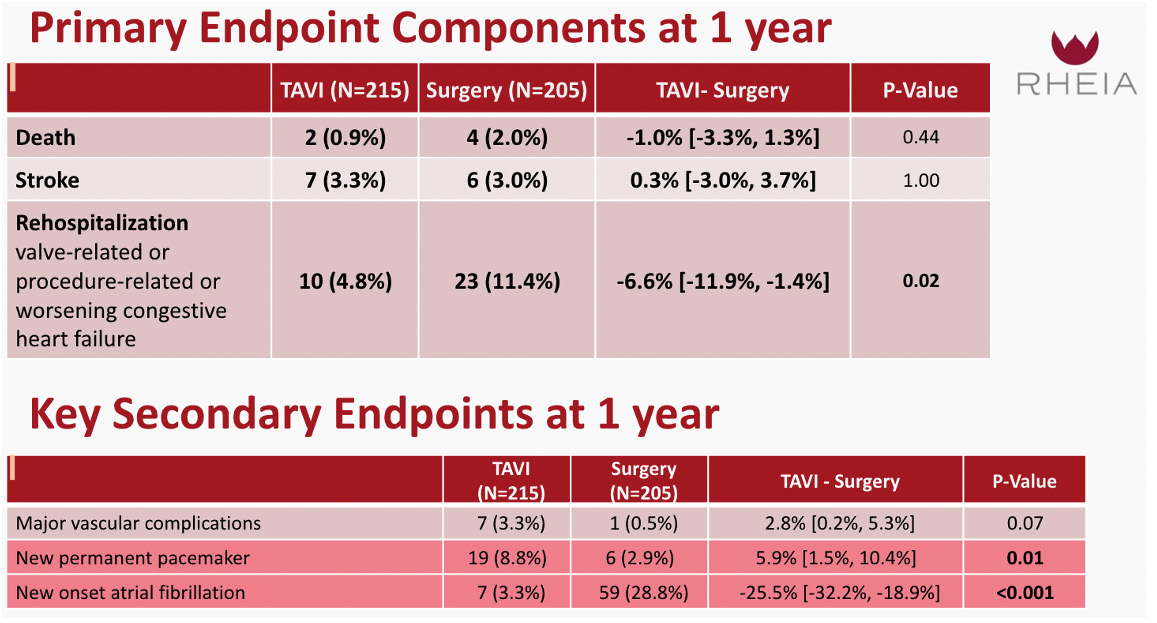
Figure 5 : Résultats individuels des composants du critère de jugement principal et critères de jugement secondaires
Conclusion
Dans l'étude RHEIA, le TAVI réalisé avec une valve expandable par ballonnet a été supérieur au remplacement valvulaire aortique chirurgical sur le critère composite à un an de décès, VC et réhospitalisations chez des femmes avec rétrécissement aortique sévère et valve tricuspide.
Il s'agit du premier essai randomisé sur le TAVI exclusivement dédié aux femmes. Il démontre la supériorité du TAVI avec valve expandable par ballonnet sur les événements cliniques à 1 an, avec un critère principal composite plus bas et liée essentiellement aux ré-hospitalisations moins fréquentes. Le gain sur la durée d'hospitalisation laisse envisager un bénéfice quant à l'utilisation des ressources de santé. Un suivi à plus long terme serait intéressant pour confirmer les résultats à 1 an et suivre l'évolution clinique et échocardiographique dans les 2 groupes.
Auteur

Arthur SOUQUET
CHU de Paris
Relectrice

Pr Hélène ELTCHANINOFF
CHU de Rouen
Références
• Vahanian A, Beyersdorf F, Praz F, Milojevic M, Baldus S, Bauersachs J et al, Guidelines for the management of valvular heart disease, Eur Heart J, 2021,vol 43,561–632.
• M. Otto C, A. Nishimura R,O. Bonow R, A. Carabello B, P. Erwin J et al, Federico Gentile, Guideline for the Management of Patients With Valvular Heart Disease, Circulation, 2021, vol 143, e72-e227.
• Popma JJ, Deeb GM, Yakubov SJ, Mumtaz M, Gada H, O'Hair D, et al. Transcatheter Aortic-Valve Replacement with a Self-Expanding Valve in Low-Risk Patients. N Engl J Med N Engl J Med; 2019; 380:1706–15.
• Forrest JK, Deeb GM, Yakubov SJ, Rovin JD, Mumtaz M, Gada H, et al. 2-Year Outcomes After Transcatheter Versus Surgical Aortic Valve Replacement in Low-Risk Patients. J Am Coll Cardiol J Am Coll Cardiol; 2022;79:882–96.
• Siontis GC, et al. Transcatheter aortic valve implantation vs surgical aortic valve replacement for treatment of severe aortic stenosis: a meta-analysis of randomized trails. Eur Heart J 2016. 37(47): 3503-3512.
• Mack MJ, Leon MB, Thourani VH, et al. Transcatheter aortic valve implantation with a balloon-expandable valve in low risk patients. N Engl J Med 2019;380:1695-1705.

