Le mystère de la non-réponse à la resynchronisation
Indications de la resynchronisation
La resynchronisation cardiaque (ou CRT pour Cardiac Resynchronisation Therapy) est une stratégie thérapeutique de rythmologie interventionnelle utilisée dans le traitement de l’insuffisance cardiaque.
Selon les recommandations actuelles, elle est indiquée chez les patients souffrant d’insuffisance cardiaque symptomatique avec FEVG altérée avec QRS > 130ms.
Les recommandations de la société Européenne de cardiologie sont reprises dans le tableau 1 (1).
La resynchronisation dans ces indications apporte une amélioration échographique (remodelage inverse) (2), un bénéfice en termes de morbidité, de mortalité et de qualité de vie (3, 4).
Rationnel physiopathologique de la resynchronisation cardiaque
La présence d’un BBG peut entraîner un asynchronisme interventriculaire et intraventriculaire du fait de la contraction tardive de la paroi latérale du VG (qui peut alors être inefficace si elle survient lorsque la valve aortique est déjà refermée) et une diminution de la phase de remplissage VG. Un BBG peut également favoriser ou majorer une insuffisance mitrale par contraction tardive des muscles papillaires. La resynchronisation permet de corriger ces asynchronismes intraventriculaire et interventriculaire et favorise le remodelage inverse. De façon similaire, la stimulation ventriculaire droite fréquente peut s’avérer délétère en entraînant un asynchronisme et une dysfonction systolique ventriculaire gauche symptomatique chez certains patients (3).
Technique classique d’implantation
La stimulation biventriculaire implique la mise en place de 2 sondes ventriculaires par voie endovasculaire veineuse. La sonde ventriculaire gauche est positionnée via le sinus coronaire dans une veine latérale ou postéro-latérale donc sur le versant épicardique du VG. Les sondes sont ensuite connectées à un boîtier de pacemaker ou de DAI selon l’indication. Une sonde atriale est associée ou non selon l’indication.
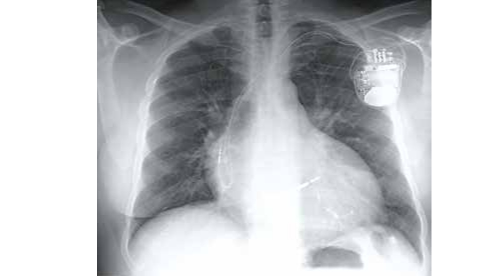
Figure 2 : Cliché thoracique patient porteur de prothèse avec resynchronisation cardiaque.
Evaluation de la réponse à la CRT
Il n’existe actuellement pas de consensus sur la définition précise de la réponse à la CRT.
En pratique, différents critères de réponse sont évalués sur des données cliniques (statut NYHA, amélioration des symptômes et de la qualité de vie, ralentissement de la progression de la cardiopathie, diminution de la fréquence des hospitalisations, diminution de mortalité) et échographiques (diminution du DTSVG de 15 à 25 %, amélioration de la FEVG à 6 mois, homogénéisation du speckle tracking) (5). Ils permettent notamment de définir les patients dit « super-répondeurs » qui correspondent aux patients qui normalisent leur FEVG suite à une resynchronisation.
Cependant, actuellement 30 % des patients implantés demeurent non-répondeurs à la resynchronisation.
L’optimisation de la CRT en pratique
Lors de l’implantation, le cardiologue/rythmologue cherche à positionner la sonde VG dans une branche latérale ou postéro-latérale du sinus coronaire qui correspond le plus souvent à la zone d’activation ventriculaire la plus tardive.
Le rythmologue peut apprécier durant la procédure le délai entre l’activation ventriculaire (mesurée par la sonde VD ou sur le QRS de surface) et la sonde VG afin de choisir le délai d’activation le plus long selon la position des sondes.
On cherchera ensuite à obtenir le QRS le plus fin possible sur l’ECG lors de l’optimisation. Différents vecteurs de stimulation sont disponibles permettant d’affiner le QRS selon la localisation des électrodes de stimulation et le délai choisi entre les stimulations VD et VG, on essaye en général de stimuler avec l’électrode de la sonde VG la plus éloignée de la sonde VD. Les sondes VG quadripolaires offrent un plus grand choix de sites de stimulation et une meilleure optimisation de la CRT.
Un délai AV court sera programmé pour favoriser une stimulation biventriculaire permanente. (Les limites supérieures et inférieures de fréquence cardiaque, les amplitudes de stimulation sont d’autres paramètres importants dans la programmation initiale).
L’échographie n’est pas utilisée systématiquement en pratique clinique quotidienne, mais réservée aux cas des patients non répondeurs à l’optimisation classique.
Figure 3 : ECG avant et après CRT
Critères de réponse à la CRT
Nous l’avons vu, 30 % des patients sont non-répondeurs à la CRT. La question est de déterminer, avant l’implantation, quel patient est susceptible de répondre favorablement à la resynchronisation. Différentes études réalisées depuis l’utilisation de la CRT ont identifié certains critères prédictifs (5–9).
Critères de bonne réponse à la CRT :
- Sexe féminin.
- Largeur du QRS (plus large est le QRS, meilleures sont les chances de réponse).
- Aspect du bloc de branche : BBG typique.
- Etiologie de la cardiopathie : cardiopathie non ischémique.
Critères de non-réponse à la CRT :
- Cardiopathie ischémique (présence d’une cicatrice non propice au remodelage inverse).
- Age > 70 ans.
- FEVG < 20 %.
- Grande dysfonction VD.
- Statut NYHA 4.
Figure 4 : Critères de réponse à la CRT (Adapté de A. Auricchio et al, Non.responders to cardiac resynchronization therapy) (5)
Que faire en cas de patient nonrépondeur à la CRT ?
- Rechercher une aggravation de la cardiopathie sous-jacente.
- Interpréter l’ECG pour vérifier la stimulation biventriculaire et la largeur/morphologie du QRS. (Généralement en cas de stimulation biventriculaire on observe un QRS plus fin avec une onde R en V1 et une onde S voire un aspect QS en D1-aVL car la stimulation VG donne un vecteur de dépolarisation qui fuit les dérivations latérales hautes).
- Réaliser une radiographie de thorax pour vérifier l’absence de déplacement de la sonde ventriculaire gauche.
- Il convient d’effectuer un contrôle de la prothèse (Pacemaker ou DAI) pour vérifier le taux de stimulation bi-ventriculaire qui reflète le taux de resynchronisation.
- Le taux de stimulation recherché est de plus de 99 % et on commence à perdre le bénéfice de la resynchronisation dès que le taux de stimulation biventriculaire passe en dessous de 98 %.
Plusieurs explications à un mauvais pourcentage de resynchronisation sont alors à rechercher :
- La présence d’ESV nombreuses (pas de stimulation bi-ventriculaire efficace en cas d’ESV). Dans ce cas on proposera un traitement antiarythmique ou une procédure d’ablation.
- La survenue de tachycardie supraventriculaire (TSV) et surtout la FA avec conduction AV spontanée rapide empêchant la stimulation biventriculaire. On proposera dans ce cas une stratégie de contrôle de rythme ou à défaut un contrôle de fréquence, voir ablation du NAV en cas d’échec.
A noter que les ESV et les TSV expliquent environ 1/3 des cas de non-réponse à la resynchronisation.
- Un Holter ECG/et ou une épreuve d’effort peut permettre de rechercher une perte de resynchronisation à l’effort chez les sujets jeunes.
- Un suivi du matériel implanté en télécardiologie peut également aider à détecter rapidement une perte de resynchronisation et son origine chez les patients fragiles.
En cas de pourcentage correct de stimulation biventriculaire (et en l’absence de mauvais réglage de la prothèse, par exemple perte de capture VG sur erreur d’auto-seuil, ou élévation de seuil VG sur léger déplacement de sonde) on pourra proposer une optimisation plus précise de la CRT avec support échocardiographique.
Optimisation de la CRT avec échographie cardiaque
Largement utilisée il y a quelques années, elle n’est plus réalisée de façon systématique actuellement, hormis dans quelques centres spécialisés. Elle consiste essentiellement à optimiser le délai-AV et le délai VV sous échographie. L’optimisation sous contrôle échographique reste cependant recommandée en cas de non-réponse à la resynchronisation après optimisation classique.
Alternatives à la technique d’implantation classique
Des alternatives peuvent être proposées en cas d’échec d’implantation de la sonde VG par la technique classique (dans 5 à 15 % des cas du fait par exemple d’une impossibilité de cathétériser le sinus coronaire).
Ainsi l’implantation d’une sonde VG épicardique par voie chirurgicale (mini-thoracotomie) pourra être proposée.
Plus récemment, la stimulation Hissienne est une technique dans laquelle une sonde spécifique est placée dans le ventricule droit en regard du faisceau de His. La technique consiste à capturer les voies de conductions rapides et permet d’obtenir un QRS fin et une resynchronisation.
Des techniques de stimulation biventriculaire endocardique existent, mais présentent des risques supplémentaires (ponction transseptale), sont associées à un risque thrombo-embolique important et nécessitent une anticoagulation curative.
Utilisation de l’imagerie en préprocédural
L’imagerie cardiaque peut être utile avant l’implantation du device :
- L’échographie cardiaque permet de mettre en évidence les asynchronismes atrio-ventriculaires, interventriculaires et intraventriculaires. (Suivi en post-procédure).
- L’IRM cardiaque permet la mise en évidence de cicatrices au niveau de la région latérale qui est associée à un moindre remodelage ventriculaire. (L’asynchronisme s’évalue également en IRM).
- La scintigraphie myocardique permet d’identifier des zones non viables (postéro-latéral).
- Le scanner et l’IRM cardiaque pour analyser l’anatomie du sinus coronaire. Ces techniques ne sont pas utilisées de façon systématique avant resynchronisation (9,10).
Sonde ventriculaire gauche arythmogène : mythe ou réalité ?
L’inversion de la séquence d’activation normale de la paroi VG (épicardique vers endocardique), prolonge l’intervalle QT et augmente la dispersion transmurale de la repolarisation préexistante, créant le substrat pour les arythmies ventriculaires réentrantes. Plusieurs cas d’ESV avec phénomène R sur T déclenchant des arythmies ventriculaires suivant la mise en place d’une stimulation biventriculaire ont été rapportés. Ceci soulève la question de l’effet pro-arythmogène de la stimulation bi-ventriculaire dans certaines situations, particulièrement en cas de facteur favorisant associé tel qu’une prolongation du QT préexistante. Ces cas restent extrêmement rares.
La resynchronisation dans l’avenir
Différents algorithmes qui visent à obtenir une fusion optimale entre QRS spontané et stimulation ou encore, des capteurs hémodynamiques pourraient permettre à l’avenir d’optimiser la resynchronisation.
D’autres systèmes de stimulation biventriculaire sans sonde sont en développement avec une électrode de stimulation déployée dans l’endocarde du VG par voie rétrograde aortique ou via ponction transseptale.
Abréviations
ESV : ExtraSystole Ventriculaire.
FEVG : Fraction d’Ejection du Ventricule Gauche.
VG : Ventricule Gauche.
BBG : Bloc de Branche Gauche.
DTSVG : Diamètre TéléSystolique du Ventricule Gauche.
NYHA : New York Heart Association.
VD : Ventricule Droit.
AV : Atrio-Ventriculaire.
VV : Ventriculo-Ventriculaire.
TSV : Tachycardie Supra-Ventriculaire.
DAI : Défibrillateur Automatique Implantable.
Figure 5 : Box Messages Clés
Références
- Ponikowski P, et al; ESC Scientific Document Group. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC)Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J. 2016;37(27):2129-2200. doi: 10.1093/eurheartj/ ehw128.
- Linde C, et al.; REVERSE (REsynchronization reVErses Remodeling in Systolic left vEntricular dysfunction) Study Group. Randomized trial of cardiac resynchronization in mildly symptomatic heart failure patients and in asymptomatic patients with left ventricular dysfunction and previous heart failure symptoms. J Am Coll Cardiol. 2008;52(23):1834-1843. doi: 10.1016/j.jacc.2008.08.027.
- Gould J, et al. Chronic Right Ventricular Pacing in the Heart Failure Population. Curr Heart Fail Rep. avr 2018;15(2):61‑9.
- Moss AJ, et al. Cardiac-Resynchronization Therapy for the Prevention of Heart-Failure Events. N Engl J Med. 2009;361(14):1329‑38.
- Auricchio A, et al. Non-Responders to Cardiac Resynchronization Therapy. Circ J. 2011;75(3):521‑7.
- Daubert C, et al Avoiding non-responders to cardiac resynchronization therapy: a practical guide.
- Sieniewicz BJ, et al. Understanding non-response to cardiac resynchronisation therapy: common problems and potential solutions. Heart Fail Rev. 2019;24(1):41‑54.
- Lin H, et al. Predictors for Cardiac Resynchronization Therapy Response. Int Heart J. 2014;55(3):256‑63.
- Zacà V, et al. Profiling cardiac resynchronization therapy patients: responders, non-responders and those who cannot respond—The good, the bad and the ugly? Int J Cardiovasc Imaging. 2011;27(1):51‑7.
- Ellims AH, et al. Utility of cardiac magnetic resonance imaging, echocardiography and electrocardiography for the prediction of clinical response and long-term survival following cardiac resynchronisation therapy. Int J Cardiovasc Imaging. 2013;29(6):1303‑11.
Article paru dans la revue “Collèges des Cardiologues en Formation” / CCF N°13

